相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、下列离子方程式正确的是A、氢氧化镁与稀盐酸反应: B、钠与水反应:Na+2H2O=Na++2OH-+H2↑ C、向石灰水中加入足量的碳酸氢钠溶液:Ca2+++OH-=CaCO3↓+H2O D、向次氯酸钙溶液中通入过量
-
2、下列各组物质在溶液中反应,无论少量过量均不可用同一离子方程式表示的是A、Cu(OH)2和硫酸;Cu(OH)2和CH3COOH B、BaCl2和Na2SO4;Ba(OH)2和K2SO4 C、NaHCO3和NaHSO4;NaHCO3和HCl D、NaHSO4和Ba(OH)2;硫酸和Ba(OH)2
-
3、硫酸盐(含、)气溶胶是PM2.5的成分之一、近期科研人员提出了雾霾微颗粒中硫酸盐生成的转化机理,其主要过程示意图如图:
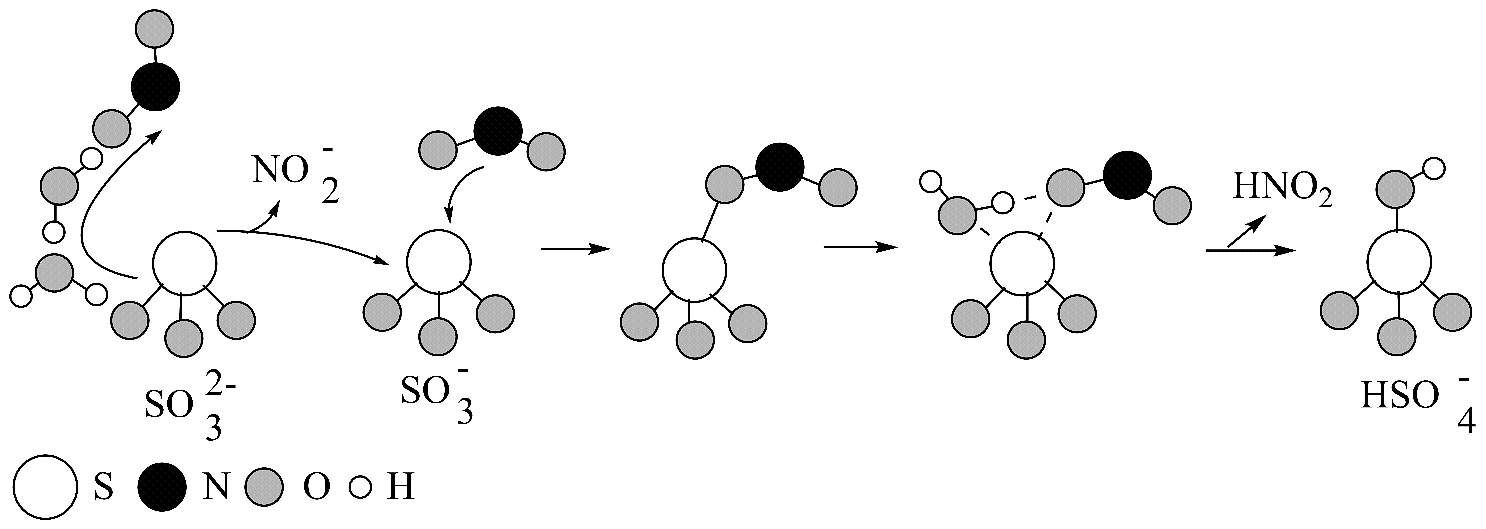
下列说法不正确的是
A、该过程有参与 B、是生成硫酸盐的氧化剂 C、硫酸盐气溶胶呈中性 D、过程中硫元素化合价升高 -
4、下列氧化还原反应中,电子转移的方向和数目均正确的是A、
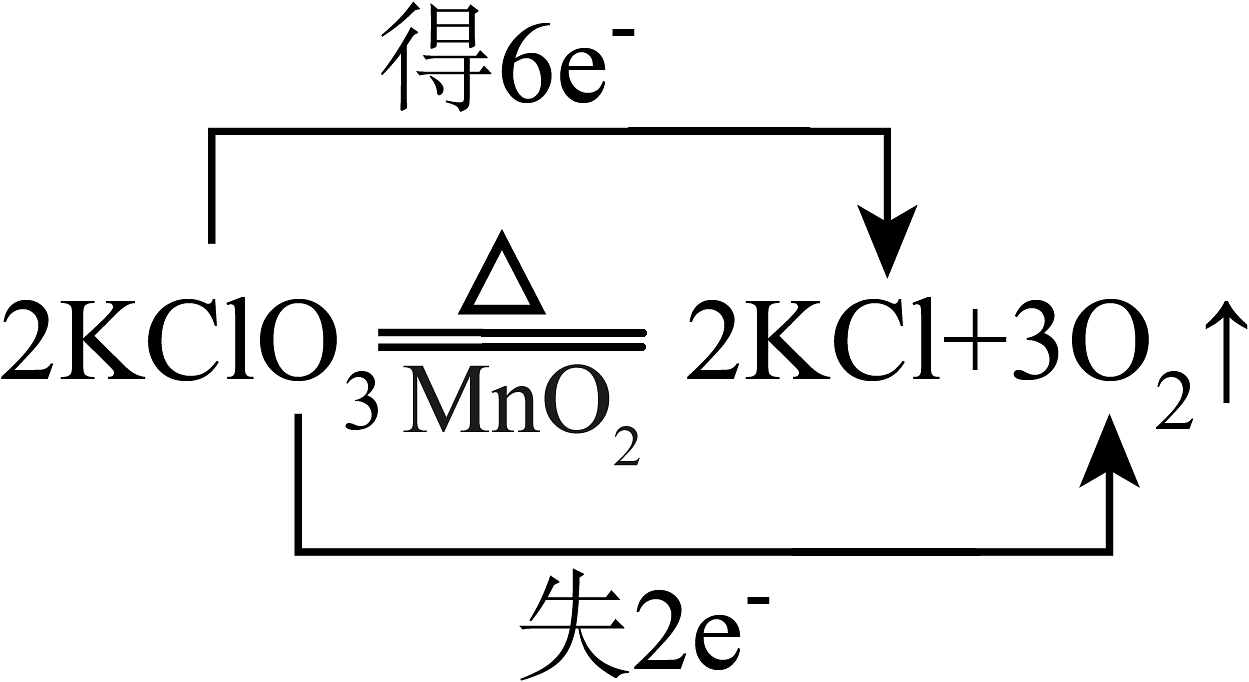 B、
B、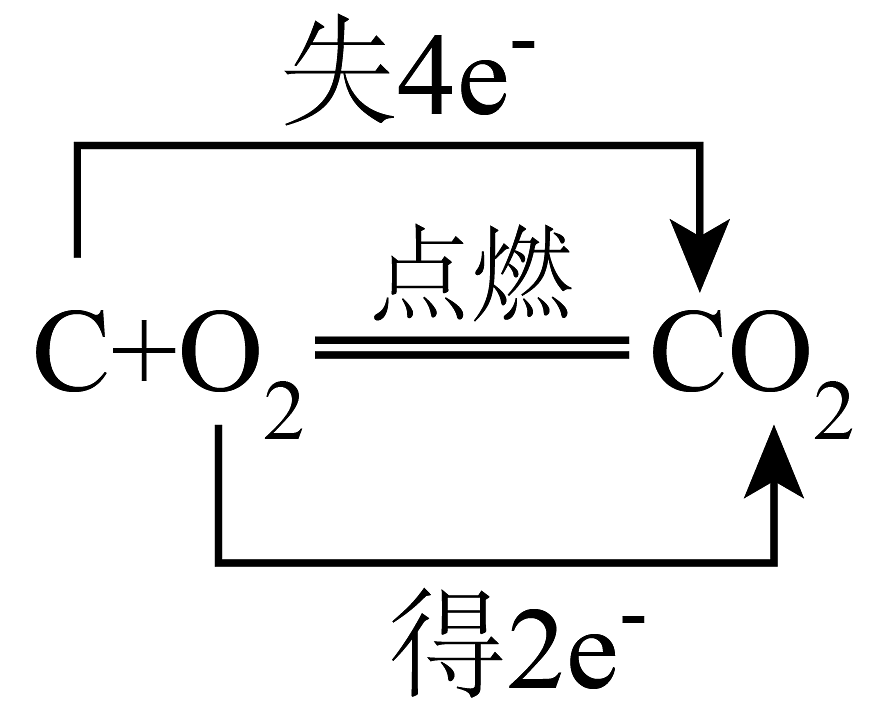 C、
C、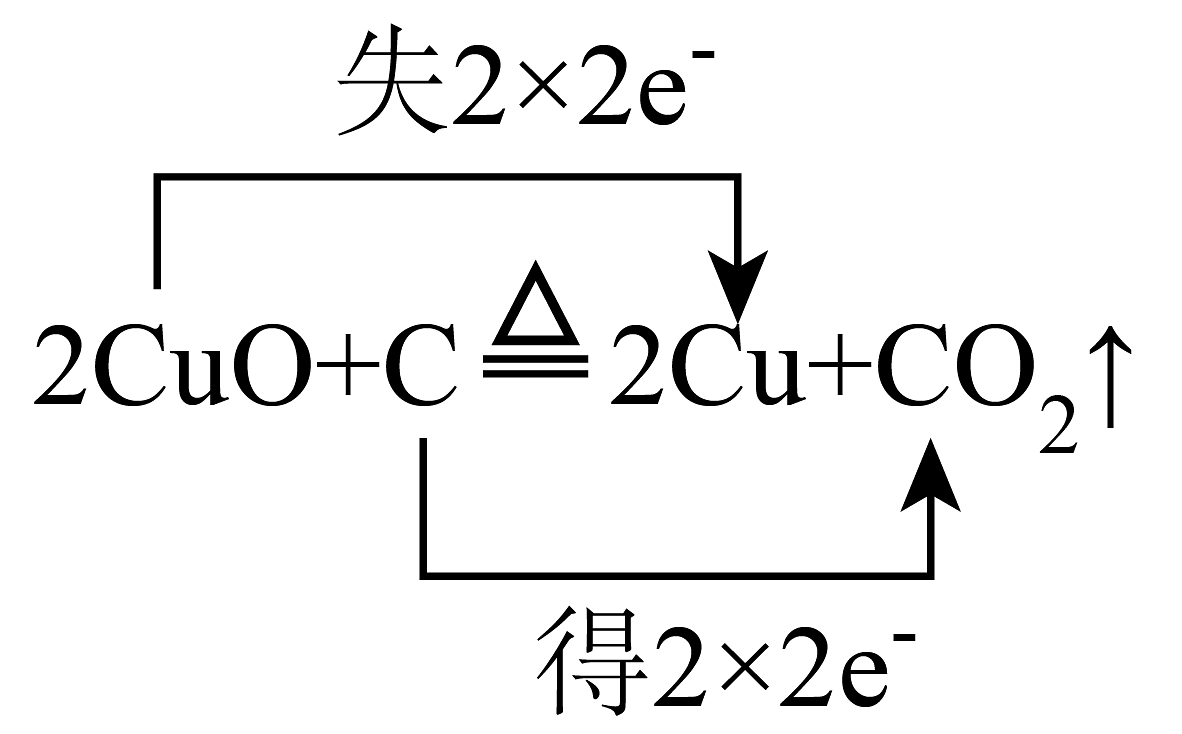 D、
D、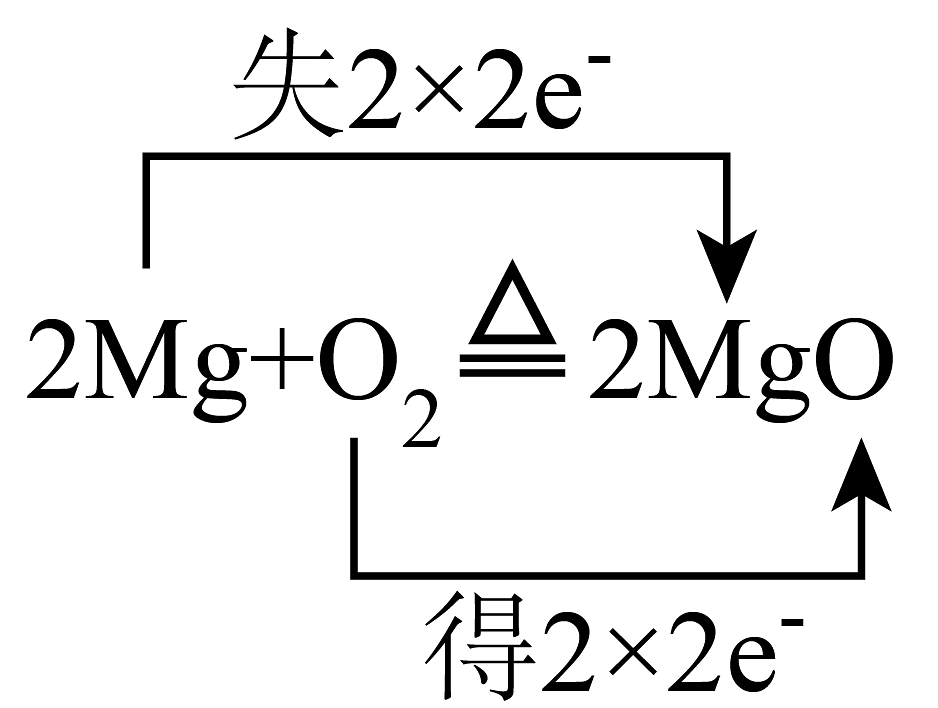
-
5、下列物质的分类正确的是
碱
酸
盐
碱性氧化物
酸性氧化物
A
Na2CO3
HCl
MgO
CO2
B
NaOH
H2SO4
NaCl
Na2O
CO2
C
KOH
HClO
CaCO3
CaO
CO
D
NH3·H2O
CH3COOH
CaCl2
Na2O2
SO2
A、A B、B C、C D、D -
6、根据实验目的,下列实验方法或操作正确的是
选项
实验目的
实验方法或操作
A
比较Fe(OH)3和Mg(OH)2 Ksp的相对大小
向装有1 mL 0.1 mol·L−1 MgCl2溶液的试管中,先滴加1~2滴2 mol·L−1 NaOH溶液,再滴加2滴0.1 mol·L−1 FeCl3溶液
B
探究淀粉的水解程度
将淀粉溶液在酸性条件下加热一段时间后,向水解液中滴加银氨溶液,加热
C
判断久置的亚硫酸钠是否变质
取一定质量的亚硫酸钠固体于试管中,加蒸馏水完全溶解后,滴加BaCl2溶液
D
探究浓度对化学反应速率的影响
取5 mL 0.01 mol·L−1和5 mL 0.02 mol·L−1的酸性高锰酸钾溶液于两支试管中,分别加入2 mL 0.01 mol·L−1的草酸溶液
A、A B、B C、C D、D -
7、下列溶液里离子检验的结论正确的是A、加稀盐酸产生无色无味气体,将气体通入澄清石灰水,石灰水变浑浊,原溶液可能含CO32- B、加BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不溶解,原溶液一定含有SO42- C、加AgNO3溶液有白色沉淀产生,原溶液一定含有Cl- D、加Na2CO3溶液有白色沉淀产生,再加盐酸,沉淀消失,原溶液中一定含有Ba2+
-
8、化学基本概念是学习化学的基础,下列有关化学概念的理解正确的是A、电解质:能导电的物质 B、有机物:含有碳元素的物质 C、酸:能电离出的物质 D、摩尔质量:单位物质的量的物质所具有的质量
-
9、空气中资源的利用具有重要意义。某小组通过电解吸收了CO2的KOH溶液(含碳微粒主要为KHCO3)的实验,得到相应的有机产物的法拉第效率[法拉第效率]随电解电压的变化如图所示。下列说法错误的是
 A、当电解电压为时,阴极主要的还原产物为H2 B、阴极生成的电极反应式为: C、当电解电压为时,电解生成的C2H4和的物质的量之比为3∶1 D、用铅蓄电池作电源电解,当只生成标况下2.24L的CH4时,理论上电源的负极增重38.4g
A、当电解电压为时,阴极主要的还原产物为H2 B、阴极生成的电极反应式为: C、当电解电压为时,电解生成的C2H4和的物质的量之比为3∶1 D、用铅蓄电池作电源电解,当只生成标况下2.24L的CH4时,理论上电源的负极增重38.4g -
10、某同学设计如下图所示实验,探究反应中的能量变化。下列判断正确的是
 A、由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应 B、将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加 C、实验(c)中为了使反应进行完全,可以向盐酸中分几次加入氢氧化钠溶液 D、若用NaOH固体测定中和反应的反应热,则测定结果数值偏高
A、由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应 B、将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加 C、实验(c)中为了使反应进行完全,可以向盐酸中分几次加入氢氧化钠溶液 D、若用NaOH固体测定中和反应的反应热,则测定结果数值偏高 -
11、若能发生如下反应:①;②;③。根据上述反应,判断下列结论中错误的是A、Cl2在反应①③中均作氧化剂 B、Cl2在反应②中既是氧化产物又是还原产物 C、氧化性强弱的顺序为: D、反应③中消耗1个Cl2 , 转移2个电子
-
12、高温下甲醇(CH3OH)分解生成燃料气(CO、H2),反应原理为CH3OH(g)=CO(g)+2H2(g)。表示该反应速率最快的是A、v(CH3OH)=1mol·L-1·s-1 B、v(CO)=1.5mol·L-1·s-1 C、v(H2)=2mol·L-1·s-1 D、v(CO)=1.5mol·L-1·min-1
-
13、下列家务劳动中涉及到的物质所属分类正确的是A、用CH3COOH去除水垢:CH3COOH是强酸 B、用Na2CO3清洗厨房油污:Na2CO3属于碱 C、用NaClO漂白衣物:NaClO属于盐 D、用C2H5OH擦拭物体表面消毒:C2H5OH是电解质
-
14、如图所示,“——”表示相连的物质间在一定条件可以反应,“→”表示在一定条件下丁可以转化为乙;下面四组选项中符合如图要求的是( )

甲
乙
丙
丁
A
H2SO4
Na2SO4
NaOH
NaCl
B
KCl
K2CO3
KOH
HCl
C
O2
CO
C
CuO
D
Fe
CuCl2
Zn
HCl
A、A B、B C、C D、D -
15、钒系催化剂催化脱硝部分机理如图所示。有关该过程的叙述错误的是
 A、反应过程中既有极性键又有非极性键的断裂和形成 B、反应过程中被氧化 C、脱硝反应为 D、是反应中间体
A、反应过程中既有极性键又有非极性键的断裂和形成 B、反应过程中被氧化 C、脱硝反应为 D、是反应中间体 -
16、下列化学用语或化学图谱表述错误的是A、基态硫原子的价层电子轨道表示式:
 B、分子的空间结构模型:
B、分子的空间结构模型: C、的核磁共振氢谱:
C、的核磁共振氢谱: D、聚乙炔的结构简式:
D、聚乙炔的结构简式:
-
17、下列实验装置不能达到实验目的的是
 A、验证Na和水反应是放热反应 B、验证Na2O2能与H2O反应放出O2 C、检验溶液中是否有钠离子 D、比较Na2CO3、NaHCO3的稳定性
A、验证Na和水反应是放热反应 B、验证Na2O2能与H2O反应放出O2 C、检验溶液中是否有钠离子 D、比较Na2CO3、NaHCO3的稳定性 -
18、一定条件下,硝酸铵受热分解的化学方程式(未配平),该反应中,被氧化与被还原的氮原子个数之比为A、5∶3 B、5∶4 C、1∶1 D、3∶5
-
19、
I、已知下列反应:
①Cl2+2NaBr=2NaCl+Br2;②2KI+Br2=2KBr+I2;③Na2S+I2=2NaI+S↓。
(1)Cl-、Br-、I-、S2-四种离子的还原性由强到弱的顺序是________。(2)判断Cl2与Na2S能否反应?________(填“否”或书写离子反应方程式)。(3)判断I2与NaBr能否反应?________(填“否”或书写离子反应方程式)。(4)已知实验室制取氯气反应为:MnO2+4H++2Cl-Mn2++Cl2↑+2H2O ,由此分析:MnO2在反应中________电子,发生________反应。(5)在硫酸溶液中,NaClO3和Na2SO3能按粒子个数比1:2完全反应,生成一种棕黄色气体X,同时Na2SO3被氧化为Na2SO4 , 则X为_______。A. Cl2O7 B. ClO2 C. Cl2O D. Cl2 II.某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知单质X。
(6)已知KBrO3在反应中得到电子,则该反应的还原剂是________。(7)已知2个KBrO3在反应中得到10个电子生成X,则X的化学式为________。(8)根据上述反应可推知_______。A. 氧化性:KBrO3>H3AsO4 B. 氧化性:H3AsO4>KBrO3 C. 还原性:AsH3>X D. 还原性:X>AsH3 -
20、
Ⅰ.海带中含有丰富的碘,从海带中提取碘,某学习小组设计并进行以下实验:

(1)步骤③的实验操作为(填操作名称),此过程使用玻璃棒,玻璃棒的作用是。
(2)步骤④反应的离子方程式为。该离子反应的氧化剂是 , 还原剂是。
(3)向步骤④得到的含碘水溶液中滴加淀粉溶液,溶液呈现色,说明有碘单质产生。
Ⅱ.碘被称为“智力元素”。以前食盐中常加入KI作为加碘剂,但空气中氧气的作用容易引起碘的损失,被氧气氧化成碘单质 , 同时得到强碱性物质。
(4)写出潮湿环境下KI与氧气反应的化学方程式:。
Ⅲ.现在的食盐里改添加性质稳定的 , 以满足人们需要。几种粒子之间有如下所示关系:

(5)四个途径中属于氧化还原反应的是(填序号)。