相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、为降低温室效应,CO2的捕集利用技术成为研究的重点。(1)、一种利用CO2的反应为:CO2(g)+4H2(g)CH4(g)+2H2O(g) H<0。下列措施能使已达到平衡时反应的正反应速率增大,且平衡向正反应方向移动的是___________。A、及时分离出水蒸气 B、适当降低温度 C、增大CO2的浓度 D、缩小体积,增大压强(2)、由CO2制备甲醇过程涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g)CH3OH(g)+H2O(g)
反应Ⅱ:CO2 (g)+H2(g)CO(g)+H2O(g)
反应Ⅲ:CO(g)+2H2(g)CH3OH(g)
已知反应Ⅰ、Ⅱ、Ⅲ的化学平衡常数分别为K1、K2、K3 , 则K3=(用K1、K2表示)。
(3)、CO合成甲醇的反应为CO(g)+2H2(g)CH3OH(g) H,在容积均为2L的甲、乙两个恒容密闭容器中分别充入2molCO、4molH2与4molCO、8molH2 , 在催化剂作用下发生反应,平衡时甲醇的体积分数与温度的关系如图所示。
①能判断甲,乙容器中反应已达到化学平衡状态的依据是。
A.混合气体的密度不变
B.2v正(H2)=v逆(CH3OH)
C.容器中的气体的压强不变
D.c(CO):c(H2):c(CH3OH)=1:2:1
②曲线I代表的是容器(填“甲”或“乙”)中发生的反应。
③该反应的H0(填“>”或“=”、“<”)。
④A、B、C三点的平衡常数KA、KB、KC大小关系是 , KC=。
-
2、研究弱电解质的电离及盐类的水解,有着重要的实际意义。常温下,部分弱电解质的电离在常温下平衡常数如表:
弱电解质
HCOOH
HCN
H2CO3
NH3·H2O
电离平衡常数
Ka=1.8×10-4
Ka=4.9×10-10
Ka1=4.3×10-7
Ka2=5.6×10-11
Kb=1.8×10-5
在常温条件下,请回答以下问题:
(1)、可以证明HCOOH是弱酸的事实是___________(填字母序号)。A、等体积等浓度的HCOOH溶液和盐酸,分别与足量镁粉反应,盐酸产生氢气的速率更快 B、等体积等pH的HCOOH和盐酸分别与足量氢氧化钠溶液充分反应,HCOOH消耗的氢氧化钠更多 C、用甲酸溶液做导电实验,灯泡很暗 D、生活中可用甲酸除水垢(2)、根据上表数据判断,相同条件下,结合H+的能力:CN-(填“大于”或“小于”或“等于”),少量的CO2通入NaCN溶液中,写出该反应离子方程式。(3)、pH=10的氨水溶液中,NH3·H2O的电离平衡常数表达式为 , 此时c(NH3·H2O)c()(填“大于”或“小于”或“等于”)。(4)、H2S、HS-、S2-在水溶液中的物质的量分数随pH的分布曲线如图。
①当pH=8时,含硫废水中最主要的含硫(-2价)微粒是(填一种)。
②通过图中数据可估算得H2S的Ka1约为。
-
3、研究化学反应中的能量变化具有重要价值。定量计算和测量则是常用的研究方法。(1)、已知CO(g)和H2(g)的燃烧热分别为H1、H2.则CO2(g)+H2(g)=CO(g)+H2O(1)的H=kJ/mol(用H1、H2表示)。(2)、利用简单碰撞理论和活化能概念可解释反应过程中的能量变化。下列关于简单碰撞理论的说法正确的是___________(填字母)。A、发生有效碰撞的分子不一定是活化分子 B、某些反应的点燃或加热条件是为了使普通分子获得能量转变为活化分子 C、基元反应的实质是活化分子有合适取向的碰撞 D、反应活化能越大,则反应过程中单位体积内的有效碰撞次数越多(3)、中和反应常伴有热量放出,某兴趣小组设计实验探究中和热的测定。取三只烧杯分别加入50mL0.55mol/L的氢氧化钠溶液(装置如图),然后分别加入50mL0.50mol/L的①稀盐酸、②稀硝酸和③稀醋酸,测量并计算中和热分别为H1、H2、H3。

①图中缺少的仪器名称为。
②H1、H2、H3关系为。
(4)、一种以太阳能为热源分解水的历程,如下图所示:
充当催化剂的是(填化学式)。
(5)、标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O2(g)和Cl2(g)的相对能量为0]
①Cl-Cl键能为。
②历程Ⅰ、历程Ⅱ中速率最快的一步反应化学方程式为。
-
4、某探究性学习小组利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对反应速率的影响,并利用H2C2O4标准液来测定KMnO4溶液的浓度,实验如下:
实验序号
实验温度(K)
酸性KMnO4溶液
H2C2O4溶液
H2O
溶液褪色时间
c(mol/L)
V(mL)
c(mol/L)
V(mL)
V(mL)
t(s)
①
298
0.02
4.0
0.10
4.0
0
t1
②
T
0.02
4.0
0.10
3.0
a
8.0
③
343
0.02
4.0
0.10
3.0
a
t2
(1)、乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a= , T=。(2)、若t1<8s,可以得出的结论是:。(3)、通过比较实验②、③的结果,可以探究变化对化学反应速率的影响。利用实验②中数据计算,用酸性KMnO4的浓度变化表示的反应速率为。(4)、准确移取20.00mL,0.0400mol/L的标准液H2C2O4溶液于锥形瓶中,加入适量H2SO4酸化,起始读数为零,用待标定的酸性KMnO4溶液滴定,直至即为滴定终点。滴定终点的读数如图所示,该读数为mL。 (5)、重复滴定实验两次,消耗高锰酸钾溶液体积的三次实验平均值为20.00mL。计算该高锰酸钾溶液的浓度为mol/L,下列操作会导致测定结果偏高的是。
(5)、重复滴定实验两次,消耗高锰酸钾溶液体积的三次实验平均值为20.00mL。计算该高锰酸钾溶液的浓度为mol/L,下列操作会导致测定结果偏高的是。A.滴定开始时滴定管尖嘴处有气泡,滴定后气泡消失
B.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
C.滴定终点读数时,俯视滴定管的刻度
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
-
5、下列实验方案设计、现象和结论都正确的是
选项
实验目的
方案设计
现象和结论
A
探究生成物浓度对化学平衡的影响
向2mL0.1mol/LFeCl3溶液加入1滴KSCN溶液,再加入少量KCl溶液
若溶液先变血红色,加入KCl溶液后血红色变浅,说明增大生成物浓度,平衡逆向移动
B
探究反应物浓度对化学反应速率的影响
分别取10mL0.1mol/LNa2S2O3溶液和10mL0.05mol/L Na2S2O3溶液于两支试管中,然后同时加入等体积、等浓度的H2SO4溶液
前者出现浑浊的时间更短,说明增大Na2S2O3浓度,可以加快反应速
C
探究压强对化学反应速率的影响
在容积不变的密闭容器中发生反应N2(g)+3H2(g)2NH3(g),向其中通入氩气增大体系压强,反应速率不变
所有化学反应的反应速率不受压强影响
D
探究催化剂对化学反应速率的影响
向两支盛有少量等体积、等浓度H2O2溶液的试管中分别加入5滴0.1mol/LFeCl3溶液和5滴0.01mol/LCuSO4溶液
加入FeCl3溶液的试管生成气体的速率更快,说明FeCl3催化效果更强
A、A B、B C、C D、D -
6、如图所示为工业合成氨的流程图。下列有关说法不正确的是
 A、步骤①中“净化”的目的是防止催化剂中毒 B、步骤②中“加压”既可提高原料的转化率,又可加快反应速率 C、步骤③中“500℃、铁触媒”有利于提高原料的平衡转化率 D、步骤④中“冷却”的目的是将氨液化分离出来,提高原料的转化率
A、步骤①中“净化”的目的是防止催化剂中毒 B、步骤②中“加压”既可提高原料的转化率,又可加快反应速率 C、步骤③中“500℃、铁触媒”有利于提高原料的平衡转化率 D、步骤④中“冷却”的目的是将氨液化分离出来,提高原料的转化率 -
7、对于可逆反应: , 下列各图正确的是A、
 B、
B、 C、
C、 D、
D、
-
8、由A、B、C、D四种金属按下表中装置进行实验。
装置



现象
A上有气体产生
B的质量增加
二价金属A不断溶解
根据实验现象判断下列说法错误的是
A、装置甲中正极的电极反应式是:2H++2e-=H2↑ B、四种金属的活泼性强弱顺序为:C>B>A>D C、装置乙中B为负极 D、装置丙中负极电极反应式为:A-2e-=A2+ -
9、下列装置所示的过程与勒夏特列原理无关的是
 A、加入MnO2时产生气泡速率加快 B、加入CaO时乙烧瓶中气体颜色加深 C、光照时试管中黄绿色变浅 D、加入铁粉时溶液颜色变浅
A、加入MnO2时产生气泡速率加快 B、加入CaO时乙烧瓶中气体颜色加深 C、光照时试管中黄绿色变浅 D、加入铁粉时溶液颜色变浅 -
10、研究化学反应进行的方向对反应设计等具有重要意义,下列说法正确的是A、已知:C(s)+CO2(g)=2CO(g) H>0,则该反应在任何条件都可以自发进行 B、知道了某过程有自发性之后,则可确定该过程是否一定会发生 C、非自发反应就是不可能发生的反应,自发反应就是能较快进行的反应 D、熵增的放热反应一定是自发反应
-
11、化学与生产、生活密切相关。下列叙述不正确的是A、“保暖贴”在发热过程中应用的是原电池的工作原理 B、医学上常采用硫酸钡作为钡餐,因为硫酸钡难被盐酸溶解 C、打开汽水瓶盖时有大量气泡冒出,不可用勒夏特列原理解释 D、纯碱可以用作锅炉除垢时CaSO4的转化剂
-
12、下列各组离子在指定溶液中一定能大量共存的是A、在=106mol/L的溶液中:Al3+、H+、Cl-、 B、使甲基橙变红的溶液中:Fe2+、、Cl-、 C、与Al反应能放出H2的溶液:、Ba2+、、 D、常温下,水电离出的c(H+)=10-13mol/L溶液中:ClO-、K+、Na+、
-
13、下列反应中,属于氧化还原反应且ΔH<0的是A、葡萄糖在体内缓慢氧化 B、碳酸氢钠和稀盐酸反应 C、NaOH溶液与盐酸反应 D、晶体与晶体反应
-
14、下列有关事实,与水解反应无关是A、热的纯碱溶液用于清洗油污 B、氯化铁溶液腐蚀铜制电路板 C、加热蒸干氯化铜溶液,得不到氯化铜纯固体 D、明矾在生活中常用作净水剂
-
15、下列物质的电离方程式中书写正确的是A、H2SO4H++ B、NaHCO3=Na++H++ C、Na2SO4=2Na++ D、H3PO4=H++
-
16、下列物质中属于强电解质,但熔融状态(即液态)却不导电的是A、 B、HCl C、 D、
-
17、第19届亚运会于2023年9月23日~10月8日在杭州举行,“绿色、智能、节俭、文明”的办赛理念深入到场地建设和运营的诸多细节之中。下列有关叙述正确的是A、场馆全部使用绿色能源,打造首届碳中和亚运会,碳中和就是不排放CO2 B、太阳能电池是将太阳能转化为电能 C、开幕式将“实物烟花”改为“数字烟花”,主要目的是减少噪音污染 D、“绿电”全部由单晶双面光伏组件提供,该光伏组件主要材料为SiO2
-
18、如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是
选项
实验现象
解释或结论
A
a处变蓝,b处变红棕色
氧化性:Cl2>Br2>I2
B
c处先变红,后褪色
氯气与水生成了酸性物质
C
d处立即褪色
氯气与水生成了漂白性物质
D
e处变血红色
还原性:Fe2+>Cl-
A、A B、B C、C D、D -
19、一种全锰电池结构如图所示。该电池工作时,下列说法错误的是
 A、正极反应为 B、理论上,每转移 , 两个电极质量改变相差 C、溶液的浓度始终保持不变 D、若更换为阳离子交换膜,会造成Mn电极的腐蚀
A、正极反应为 B、理论上,每转移 , 两个电极质量改变相差 C、溶液的浓度始终保持不变 D、若更换为阳离子交换膜,会造成Mn电极的腐蚀 -
20、
是一种常用的磁性材料。某化学兴趣小组通过实验制备并探究与酸的反应。
实验一、制备
ⅰ.将蒸馏水煮沸后冷却,利用该蒸馏水和固体配制500溶液。
ⅱ.取100溶液,用植物油封住(如图所示),加入溶液,二者恰好反应后,过滤,得到固体。
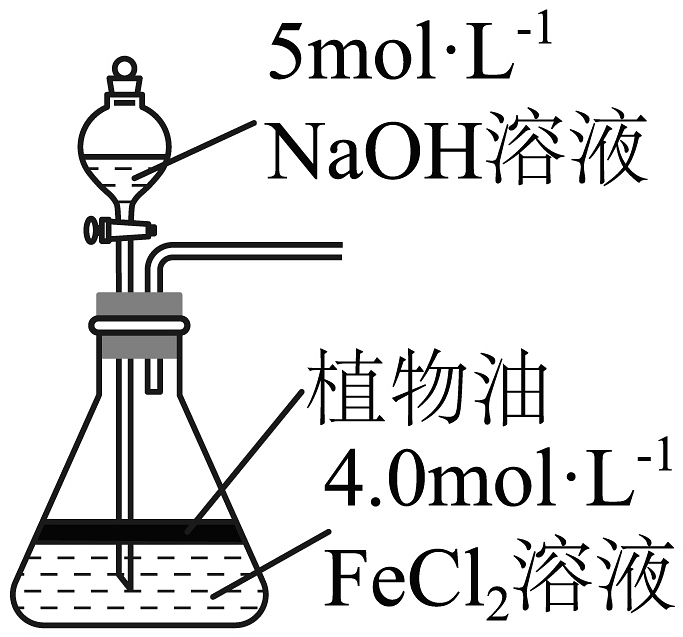
ⅲ.取溶液和分散剂[能使制得的颗粒更小],加入过量溶液并在空气中不断搅拌,二者充分反应后形成红褐色浊液。
ⅳ.将ⅱ中制得的氢氧化亚铁加入中的红褐色浊液中,持续加热和搅拌,充分反应后过滤、洗涤、干燥,最后得到。
(1)ⅰ中蒸馏水煮沸后使用的目的是;。
(2)ⅲ中发生反应的总离子方程式为。
实验二、探究与稀硫酸的反应
甲同学对能否与酸反应提出了猜想:
猜想1:能与酸反应;猜想2:不能与酸反应。
为了验证假设,甲同学进行了如下实验并观察到相应的实验现象:
实验编号
实验操作
实验现象
1
将0.1g , 粉末加入103硫酸溶液中,浸泡5min,取2上层清液于试管①②中,分别加入5滴溶液和溶液,振荡试管
两试管均无明显现象,浸泡一夜后,试管①中溶液变红,试管②中有蓝色沉淀生成
2
将0.1g粉末加入106盐酸中,浸泡5min,取2上层清液于试管③④中,分别加入5滴溶液和溶液,振荡试管
试管③中溶液变红,试管④中有蓝色沉淀生成
已知:与反应会产生蓝色沉淀,可用于检验溶液中是否含有。
(3)甲同学根据实验1得出结论:猜想1正确,且(填离子符号)能促进与酸反应。粉末与稀硫酸反应的离子方程式为。
(4)乙同学认为甲同学的结论不一定完全正确,因此设计实验:用硫酸溶液浸泡粉末时加入适量的 , 取上层清液于两支试管中,分别加入5滴溶液和溶液,振荡试管,观察到 , 证明甲同学的结论正确。