相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、在水溶液中,下列电离方程式正确的是A、Ca(OH)2===Ca2++2(OH-) B、FeCl3===Fe2++3Cl- C、H2SO4===H++ D、Fe2(SO4)3===2Fe3++3
-
2、胶体区别于其他分散系的本质特征是A、稳定透明 B、产生丁达尔现象 C、胶体微粒不能穿透半透膜 D、分散质直径在10-7~10-9m之间
-
3、下列物质间转化关系不能一步实现的是A、CaO→Ca(OH)2→CaCl2 B、Cu→CuO→Cu(OH)2 C、CO2→CaCO3→CaCl2 D、H2SO4→H2→H2O
-
4、实验室常用加热的方法制取少量。下列说法正确的是A、该反应属于氧化还原反应 B、属于非电解质 C、属于酸性氧化物 D、制取后剩余的固体物质为纯净物
-
5、下列有关原电池的说法不正确的是
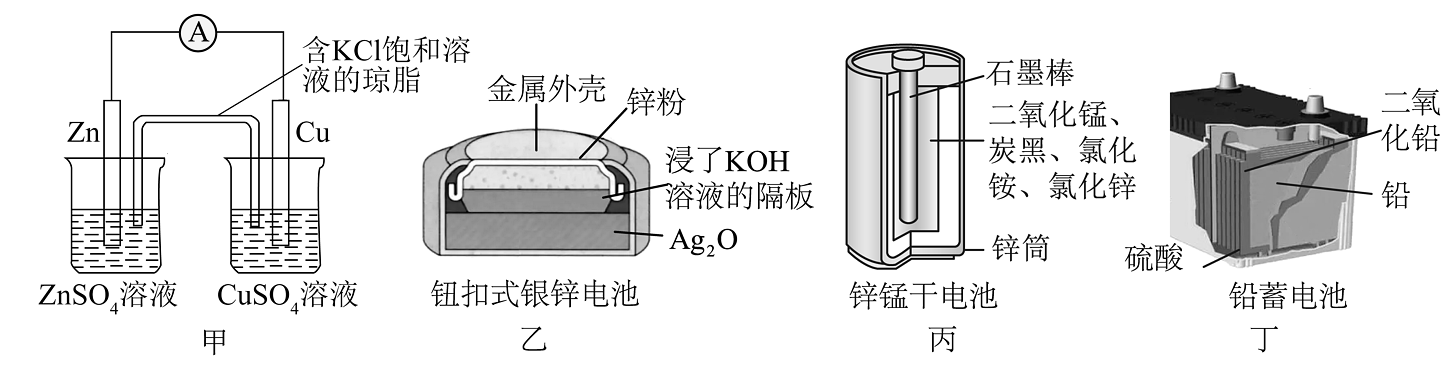 A、图甲所示装置中,盐桥中的向盛有溶液的烧杯中移动 B、图乙所示装置中,正极的电极反应式为 C、图丙所示装置中,使用一段时间后,锌筒会变薄 D、图丁所示装置中,使用一段时间后,电解质溶液的酸性减弱,导电能力下降
A、图甲所示装置中,盐桥中的向盛有溶液的烧杯中移动 B、图乙所示装置中,正极的电极反应式为 C、图丙所示装置中,使用一段时间后,锌筒会变薄 D、图丁所示装置中,使用一段时间后,电解质溶液的酸性减弱,导电能力下降 -
6、
氧化还原反应在工农业生产、日常生活中具有广泛用途。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+ , 故维生素C具有性(填“氧化”或“还原”,下同),在反应过程中维生素C发生反应。
某小组同学学习了氧化还原反应的知识后,欲探究H2O2的性质。
[预测]
(2)聚焦H2O2中的核心元素O,O元素的化合价为 , 预测H2O2既具有氧化性,也具有还原性,理由是。
[实验和观察]

(3)(a)实验①中,观察到KMnO4溶液与H2O2发生了反应,紫红色褪去同时有无色气体产生,经分析知紫红色MnO转变为无色Mn2+ , 该实验证明H2O2具有(填“氧化”或“还原”)性。
(b)实验②,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,是为了验证H2O2的(“氧化”或“还原”)性(已知:淀粉溶液遇I2会变蓝)。
(4)实验室常用MnO2催化H2O2分解制备氧气,写出其化学方程式,并用双线桥标明电子转移:。
[结论]以上实验可得出的结论是:H2O2既具有氧化性,也具有还原性。
(5)该实验也能说明H2O2、KMnO4和I2三者的氧化性由强到弱的顺序为 。
-
7、有一瓶透明澄清的溶液,其中可能含有Na+、H+、NO、Mg2+、CO , 取该溶液进行以下实验:
①取pH试纸检验,测得溶液呈强酸性。
②另取部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,有白色沉淀产生。
请回答下列问题:
(1)、用pH试纸检验,表明溶液呈强酸性,可以排除的存在。(2)、步骤②中产生白色沉淀的离子方程式为。(3)、该溶液中可能存在的离子为。(4)、根据上述实验事实能确定溶液中肯定存在的离子是。 -
8、按要求写出与下列过程或反应相对应的一个化学表达式。(1)、的化学方程式:;(2)、醋酸溶解于水的电离方程式:;(3)、配平以下反应方程式并用单线桥标出电子转移的方向和数目:。
-
(4)、化工生产中常用到“三酸(硝酸、硫酸和盐酸),两碱(烧碱和纯碱)”。①从物质的分类角度看,不恰当的一种物质是。
②上述物质中,可以确定既不是电解质也不是非电解质的是 , 依据是。
-
9、现有下列物质:①KCl晶体 ②液态HCl ③ ④汞 ⑤CaCO3固体 ⑥稀硫酸 ⑦酒精C2H5OH ⑧熔融的NaCl ⑨浓氨水
其中属于混合物的是(填序号,下同);属于电解质的是;属于非电解质的是;能导电的有。
-
10、对于离子反应,下列说法正确的是( )A、参加离子反应的一定都是电解质 B、任何一种离子的浓度在离子反应中一定变小 C、自由离子之间的反应不能在固态中进行 D、没有沉淀、气体、水生成的反应就不是离子反应
-
11、物质M在水中发生电离:M=X2++2Y- , 则下列判断正确的是A、M可能是酸 B、X2+一定是金属离子 C、Y-是OH- D、M一定属于盐
-
12、下列分散系中最不稳定的是A、向NaOH溶液中通入CO2得到的无色溶液 B、向CuSO4溶液中加入NaOH溶液得到的分散系 C、向沸水中逐滴滴入FeCl3饱和溶液得到的红褐色液体 D、向Fe(OH)3固体中加入盐酸得到的棕黄色液体
-
13、下列说法中正确的是A、Na2SO4·10H2O是混合物 B、同种分子构成的物质一定是纯净物 C、混合物肯定由两种以上元素组成 D、含有氧元素的化合物都是氧化物
-
14、下列关于钠的说法中不正确的是A、金属钠着火时,可以用沙土灭火 B、钠长期放置在空气中,最终将变成碳酸钠粉末 C、实验后剩余的钠粒,需要放回盛有煤油的原试剂瓶中 D、将一小块钠投入硫酸铜溶液时,既能产生气体又会出现白色沉淀
-
15、实现下列物质之间的转化,需要加入还原剂才能完成的是A、SO3→H2SO4 B、 C、CO→CO2 D、
-
16、已知某两种物质在一定条件下能发生化学反应,其反应的微观示意图如图所示。下列说法不正确的是

(说明:一种小球代表一种元素的原子)
A、图中的反应物都是化合物 B、该反应属于置换反应 C、该反应属于氧化还原反应 D、该反应一定遵守质量守恒定律 -
17、分类是科学研究的重要方法,下列物质分类不正确的是A、化合物:干冰、冰水混合物、烧碱 B、同素异形体:石墨、C60、金刚石 C、混合物:盐酸、矿泉水、空气 D、电解质:熔融NaCl、硫酸、铜
-
18、高铁酸钾()是高效、绿色的水处理剂,其原理如下图所示,下列说法不正确的是
 A、中铁元素的化合价为+6价 B、在a过程中被细菌还原 C、在b过程中形成的胶体能净水 D、在a过程中细菌发生还原反应
A、中铁元素的化合价为+6价 B、在a过程中被细菌还原 C、在b过程中形成的胶体能净水 D、在a过程中细菌发生还原反应 -
19、某溶液中存在大量的H+、Cl-、 , 该溶液中还可能大量存在的是A、 B、Ba2+ C、Ag+ D、Al3+
-
20、溶液、胶体和浊液这三种分散系的根本区别是A、是否是大量分子或离子的集合体 B、分散质粒子直径的大小 C、是否能透过滤纸 D、是否为均一、稳定、透明的外观