相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、2023年上海科技节以“悦享科技,智创未来”为主题,展示了近年来我国的科技成果。下列说法错误的是A、冬奥火炬“飞扬”使用的碳纤维复合材料具有强度高、耐高温的特点 B、“萌新”机器人的有机高分子材料面罩为纯净物 C、“雪龙号”极地破冰船船身由合金钢材料构成,其抗撞击能力强 D、直径为300mm以上的大硅片首次应用于集成电路,其属于新型无机非金属材料
-
2、室温下,探究溶液的性质。下列实验方案能达到探究目的的是
选项
探究目的
实验方案
A
是否发生电离
向溶液中加入一小块钠,观察溶液中是否有气泡产生
B
是否发生水解
用干燥洁净玻璃棒蘸取溶液,点在干燥的试纸上,测出溶液的
C
溶液中是否存在
取一支洁净的铂丝,蘸取溶液后在煤气灯上灼烧,透过蓝色钴玻璃观察火焰颜色
D
溶液中是否存在
向溶液中滴入几滴澄清石灰水,观察溶液是否变浑浊
A、A B、B C、C D、D -
3、实验室配制一定物质的量浓度NaOH溶液时,下列做法正确的是A、容量瓶检漏时,倒置一次即可 B、NaOH固体放在称量纸上称量 C、NaOH溶液转移到容量瓶中需用玻璃棒引流 D、定容时若加水超过刻度线,立即用胶头滴管吸出多余液体
-
4、脱硫是天然气、电力、石油化工等行业中非常重要的一个环节,其主要目的是去除含硫化合物,以减少环境污染和提高产品质量。(1)、天然气中含有少量 , 在酸性溶液中利用硫杆菌可实现天然气的催化脱硫,其原理如图所示。

①该催化脱硫过程总反应的化学方程式为。
②该催化过程中,要控制反应温度不能过高,原因是。
(2)、钙基脱硫剂常用于工业烟气的干法脱硫。通过添加活性组分可以提高脱硫性能,为筛选出能够更加有效提升脱硫剂脱硫效果的活性组分,进行研究:250℃时,初始浓度、模拟烟气流量相同的条件下,分别添加0.1g及氨基类活性物质进行脱硫实验,结果如图所示。
①反应一段时间后,出口浓度都升高的原因是。
②250℃时,已分解为固体,氨基类活性物质分解产生气态。氨基类活性物质脱硫性能明显优于的原因是。
(3)、石油化工会产生含硫(-2价)废水,碱性条件下,催化氧化废水的机理如图所示。
①步骤Ⅲ可描述为。
②步骤Ⅳ中,化合价发生变化的元素有。
-
5、是一种优良的消毒剂,浓度过高时易发生爆炸,常将其制备成固体以便运输和贮存,高于60℃时分解。实验装置如图所示。
 (1)、装置A产生。将一定量固体与溶液、溶液中的一种配成悬浊液,加入到三颈烧瓶中,通过恒压滴液漏斗缓慢滴加另一种溶液,充分反应。
(1)、装置A产生。将一定量固体与溶液、溶液中的一种配成悬浊液,加入到三颈烧瓶中,通过恒压滴液漏斗缓慢滴加另一种溶液,充分反应。①恒压滴液漏斗中的溶液为。
②制备过程中持续通入空气的目的是。
(2)、装置B制备。①生成的化学方程式为。
②溶液在不同温度时析出的晶体情况如图所示。从溶液中获得固体的操作:(须使用的试剂:无水乙醇)。
 (3)、纯度测定。称取样品1.000g溶于水配制成250mL溶液,取25.00mL于锥形瓶中,再加入足量酸化的KI溶液。充分反应后滴加两滴淀粉溶液作指示剂,用0.2000·L-1的标准溶液反应,至恰好完全反应时消耗溶液20.00mL。测定过程中发生下列反应: , 。
(3)、纯度测定。称取样品1.000g溶于水配制成250mL溶液,取25.00mL于锥形瓶中,再加入足量酸化的KI溶液。充分反应后滴加两滴淀粉溶液作指示剂,用0.2000·L-1的标准溶液反应,至恰好完全反应时消耗溶液20.00mL。测定过程中发生下列反应: , 。①计算该产品的纯度(写出计算过程)。
②配制标准溶液,下列操作将导致测定的纯度偏高的是(填字母)。
a.定容时俯视刻度线 b.摇匀后发现液面下降,补加蒸馏水至刻线
c.未洗涤烧杯和玻璃棒 d.容量瓶洗涤后未干燥直接进行配制
-
6、以菱镁矿渣(主要成分是 , 含少量、FeO、CaO、、、MgO等)为原料制备的流程如下:
 (1)、将稀硫酸加入菱镁矿渣充分反应后过滤。
(1)、将稀硫酸加入菱镁矿渣充分反应后过滤。①为提高“酸浸”效率可以采用的措施是(写出一种措施即可)。
②滤渣的主要成分为、。
(2)、加入将氧化为 , 加入适量MgO调节溶液pH,除去Fe、Al元素。①“氧化”时的离子方程式为。
②pH对硫酸镁粗液中杂质元素去除率以及Mg元素损失率的影响如图所示。应调节pH为。
 (3)、对除钙后的滤液进行蒸发结晶,过滤得到晶体。硫酸镁溶液在不同温度下蒸发结晶得到的产物的XRD图谱如图所示(XRD图谱用于判断某晶态物质是否存在)。要得到晶体应选择的温度为。
(3)、对除钙后的滤液进行蒸发结晶,过滤得到晶体。硫酸镁溶液在不同温度下蒸发结晶得到的产物的XRD图谱如图所示(XRD图谱用于判断某晶态物质是否存在)。要得到晶体应选择的温度为。 (4)、将24.6 g (摩尔质量为246 g·mol-1)焙烧,剩余固体质量随温度变化曲线如图所示。
(4)、将24.6 g (摩尔质量为246 g·mol-1)焙烧,剩余固体质量随温度变化曲线如图所示。
①a→b过程发生反应的化学方程式为。
②e点对应固体成分的化学式为。
-
7、下图是中学常见元素周期表的一部分,参照元素在表中的位置,回答下列问题:
 (1)、元素的排列。
(1)、元素的排列。①元素g在周期表的位置是。
②主族元素在周期表中所处的位置与电子层数和电子数有关。
(2)、元素及其化合物的结构。①f形成的氧化物的电子式为。
②a、d形成的化合物中含有的化学键类型为。
(3)、元素周期律及其应用。①元素b、c形成的简单氢化物热稳定性最强的是(填结构式),元素h、i最高价氧化物对应的水化物酸性最强的是(填化学式)。
②已知:与NaOH生成和。j是门捷列夫预言的“类铝”元素镓(Ga),其最高价氧化物对应的水化物与元素e的最高价氧化物对应的水化物反应的离子方程式为。
-
8、向一定浓度的NaOH溶液中缓慢通入 , 生成物的物质的量和溶液的温度随通入氯气的物质的量的变化如图所示。下列说法不正确的是
 A、a点时溶液中 B、的增加可能是由于温度升高导致的 C、减少的原因可能是: D、参加反应的NaOH与的物质的量之为2:1
A、a点时溶液中 B、的增加可能是由于温度升高导致的 C、减少的原因可能是: D、参加反应的NaOH与的物质的量之为2:1 -
9、室温下,通过下列实验探究一定浓度溶液的性质。
实验1:向溶液中滴几滴酚酞,溶液显红色。
实验2:向实验1所得溶液中缓慢滴加几滴稀盐酸,溶液红色变浅,无气体产生。
实验3:向溶液中通入过量的 , 无明显现象。
实验4:向实验3所得溶液中滴加少量溶液,产生白色沉淀。
下列有关说法正确的是
A、实验1说明可电离出 B、实验2中溶液红色变浅的原因是: C、由实验3可以推测与没有发生反应 D、实验4反应后的溶液中存在大量的、、 -
10、室温下,根据下列实验过程及现象,能验证相应实验结论的是
选项
实验过程及现象
实验结论
A
往某溶液中加入盐酸产生无色气体
该溶液一定含有
B
将湿润的有色布条放入干燥的氯气,布条褪色
氯气具有漂白性
C
向蔗糖中滴加几滴蒸馏水,再加入浓硫酸,产生海绵状黑色物质,并产生刺激性气味气体
浓硫酸体现了吸水性、脱水性和强氧化性
D
用洁净的铂丝蘸取某溶液灼烧,火焰呈黄色
溶液中不含钾元素
A、A B、B C、C D、D -
11、用反萃取原理可从的萃取液中回收 , 流程如图所示。下列说法不正确的是
 A、“反应Ⅰ”的离子方程式为 B、“操作Ⅰ”为分液 C、利用反萃取原理可实现碘单质的重新富集 D、通过升华可将粗碘提纯
A、“反应Ⅰ”的离子方程式为 B、“操作Ⅰ”为分液 C、利用反萃取原理可实现碘单质的重新富集 D、通过升华可将粗碘提纯 -
12、实验室进行制备并验证性质的实验,下列相关原理、装置及操作正确的是
 A、用装置甲制取 B、用装置乙验证漂白性 C、用装置丙收集 D、用装置丁吸收尾气
A、用装置甲制取 B、用装置乙验证漂白性 C、用装置丙收集 D、用装置丁吸收尾气 -
13、硫及其化合物部分转化关系如图所示。下列说法正确的是A、常温下,32gS单质中含1.0molS原子 B、反应①每消耗3.4g , 得到0.4mol电子 C、0.1mol·L-1溶液中,为0.1mol·L-1 D、标准状况下,11.2L中原子总数约为
-
14、阅读下列材料,完成下面小题:
周期表中ⅣA族元素及其化合物应用广泛。石墨烯、碳纳米管、富勒烯等单质是常见的碳纳米材料;能与氢氟酸(HF,弱酸)反应生成(在水中完全电离为和);将硫化锗()与共热制得锗;还原性比还原性强;与浓盐酸反应生成。
(1)、石墨烯结构如图所示。下列有关说法正确的是 A、石墨烯纳米材料属于胶体 B、石墨烯是一种新型化合物 C、石墨烯能导电,石墨烯属于电解质 D、从石墨剥离出石墨烯需克服分子间作用力(2)、碳及其化合物的多样性是构成物质多样性的重要原因。下列说法中正确的是A、乙醇和二甲醚互为同位素 B、富勒烯、金刚石化学性质相似 C、碳纳米管、石墨烯互为同分异构体 D、12C、13C、14C三种核素互为同素异形体(3)、下列化学反应表示正确的是A、与HF溶液反应: B、高温下还原硫化锗: C、强酸溶液中,与反应: D、与浓盐酸反应:(浓)
A、石墨烯纳米材料属于胶体 B、石墨烯是一种新型化合物 C、石墨烯能导电,石墨烯属于电解质 D、从石墨剥离出石墨烯需克服分子间作用力(2)、碳及其化合物的多样性是构成物质多样性的重要原因。下列说法中正确的是A、乙醇和二甲醚互为同位素 B、富勒烯、金刚石化学性质相似 C、碳纳米管、石墨烯互为同分异构体 D、12C、13C、14C三种核素互为同素异形体(3)、下列化学反应表示正确的是A、与HF溶液反应: B、高温下还原硫化锗: C、强酸溶液中,与反应: D、与浓盐酸反应:(浓) -
15、氯及其化合物的转化具有重要应用。下列说法正确的是A、制漂白粉:NaCl溶液漂白粉 B、HCl制备:NaCl溶液和 C、纯碱工业:NaCl溶液 D、金属Mg制备:溶液
-
16、化学创造美好生活。下列有关物质的性质与用途具有对应关系的是A、浓硫酸具有吸水性,可用作干燥剂 B、次氯酸具有弱酸性,可用于杀菌消毒 C、钠具有强还原性,可用于制作高压钠灯 D、受热易分解,可治疗胃酸过多
-
17、反应可作呼吸面具的供氧剂。下列说法正确的是A、的结构示意图为
 B、空间填充模型为
B、空间填充模型为 C、仅含离子键
D、中子数为10的氧原子可表示为
C、仅含离子键
D、中子数为10的氧原子可表示为
-
18、2024年12月26日,我国第六代战机首飞成功。战机中常使用高强度、耐高温的钛合金材料,钛合金材料属于A、分子晶体 B、离子晶体 C、金属晶体 D、共价晶体
-
19、为考查和共存对制氢的影响,在0.1MPa下,的混合气体反应达到平衡时,反应物的转化率、产物的物质的量分数随温度的变化分别如图-1、图-2所示,体系中的反应主要有:
Ⅰ、
Ⅱ、
Ⅲ、

下列说法不正确的是
A、反应 B、图-1中曲线①表示转化率随温度的变化 C、温度700℃时,反应Ⅰ是体系中的主要反应 D、反应Ⅲ的平衡常数:K(400℃)>K(700℃) -
20、工业尾气中的氮氧化物是大气主要污染源之一、消除氮氧化物对环境保护有着重要意义。(1)、SNCRSCR脱硝技术是一种新型除去烟气(含NOx和O2等)中氮氧化物的方法,以NH3作还原剂,其脱硝流程如图1,其中SNCR脱硝效率与体系温度关系如图2所示。
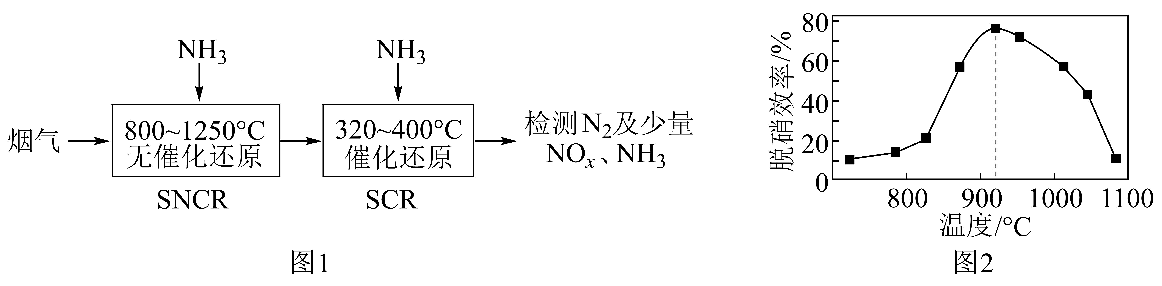
①当体系温度高于950℃时,SNCR脱硝效率明显降低,其可能的原因是;
②SNCR与SCR技术相比,SCR技术的反应温度不能太高,其原因是。
(2)、氢气选择性催化还原(H2-SCR)是一种理想的方法。其相关反应如下:主反应:2NO(g)+2H2(g)=N2(g)+2H2O(g) ΔH1
副反应:2NO(g)+H2(g)=N2O(g)+H2O(g) ΔH2<0
①已知:2H2(g)+O2(g)=2H2O(g) ΔH3=-483.5 kJ·mol-1
N2(g)+O2(g)=2NO(g) ΔH4=+180.5 kJ·mol-1
ΔH1=。
②一定温度下用H2还原NO,测得反应后尾气中NO、N2O、N2的体积分数随H2的体积分数的变化如图3所示。当H2的体积分数大于750×10-6时,N2的体积分数下降的原因是。

③在Pt表面H2、O2和NO会解离成H、O、N,其中H与O生成H2O,而Pt表面的N会与邻位的N反应生成N2 , 与NO反应生成N2O,与邻位的H反应生成NH3 , 过程如图4所示。当Pt的载体酸性增强时,会产生更多的N2 , 原因是。
