相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、化学源于生活又服务于生活。下列应用与所述的化学知识没有关联的是( )
选项
应用
化学知识
A
浓硫酸运输的警示标志为

浓硫酸有腐蚀性
B
用FeCl3腐蚀Cu 刻制印刷电路板
铁比铜还原性强
C
放电影时,放映机到银幕间形成光柱
胶体的丁达尔效应
D
用NaHCO3作膨松剂制作面包
NaHCO3受热分解产生CO2
A、A B、B C、C D、D -
2、“84消毒液”与硫酸溶液反应可以制取氯气,反应方程式为。为探究氯气的性质,某同学设计了如下所示的实验装置。

请回答:
(1)、在该实验中,制取氯气的装置是(填字母)。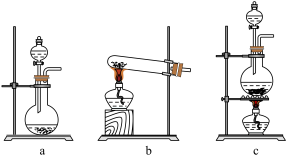 (2)、装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是 , 请提出合理的改进方法。(3)、D中现象是 , 反应的离子方程式为。(4)、写出氯气与NaOH溶液反应的离子方程式。
(2)、装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是 , 请提出合理的改进方法。(3)、D中现象是 , 反应的离子方程式为。(4)、写出氯气与NaOH溶液反应的离子方程式。 -
3、化学是一门以实验为基础的学科,研究小组需要经常做实验。(1)、I.某研究小组甲在探究Na2O2的性质实验时,发现Na2O2样品与过量水反应,待完全反应不再产生氧气后,得溶液M。溶液M可使酸性KMnO4溶液褪色,同时放出氧气。小组成员查阅资料表明,Na2O2与水反应还可生成H2O2。
Na2O2与水反应生成H2O2的反应是否属于氧化还原反应(填是、否)。(2)、完成并配平该反应的离子方程式:+H2O2+H+=+O2↑+
(3)、II.某研究小组乙模拟侯德榜制碱法制取碱,流程如图:
已知:几种盐的溶解度
“侯氏制碱法”誉满全球,其中的“碱”为(填化学式)根据图示装置I中反应的化学方程式为;装置II中反应的化学方程式为。物质 NaCl NH4HCO3 NaHCO3 NH4Cl 溶解度 36.0 21.7 9.6 37.2 (4)、该流程中可循环利用的物质是(填化学式)(5)、下列选项中哪种物质可以鉴别浓度相同的Na2CO3溶液和NaHCO3溶液____。A、澄清石灰水 B、氢氧化钠溶液 C、稀盐酸 D、BaCl2溶液(6)、请写出(5)中能鉴别Na2CO3和NaHCO3两种物质并且能产生悬浊液的离子方程式:。 -
4、回答下列问题:(1)、中国古代著作中有“银针验毒”的记录,其原理为 , 则X的化学式是 , 其中在该反应中(填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)、按如图所示操作,充分反应后:
①II中铜丝上观察到的现象是。
②结合I、II实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为。
(3)、阅读下面一段材料并回答问题。高铁酸钾使用说明书
【化学式】K2FeO4
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
①K2FeO4中铁元素的化合价为。
下列关于K2FeO4的说法中,不正确的是。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快、安全性好、无异味
②制备高铁酸钾时,先制备得到Na2FeO4 , 反应为 , 该反应的氧化产物是;每生成1molNa2FeO4转移mol电子。
-
5、请根据已知信息回答下列各问:(1)、I.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
写出H3PO2溶液与足量NaOH溶液反应的离子方程式。(2)、磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。则Na2HPO4、NaH2PO2、Na2HPO3中属于酸式盐的是(填化学式)。(3)、II.NaHSO4可用作清洁剂、防腐剂等。
下列关于NaHSO4的说法正确的是。a.NaHSO4固体不能导电
b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质
d.NaHSO4溶液显中性
(4)、NaHSO4溶液与NaHCO3溶液反应的离子方程式为。(5)、III.有以下物质:①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
以上物质属于电解质的是。(6)、写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:。(7)、将物质⑥配制成溶液,逐滴加入⑦溶液中至Ba2+恰好沉淀完全,写出离子方程式:。 -
6、“价类二维图”是学习元素及其化合物知识的重要模型。氯元素的“价类二维图”如图所示,下列说法不正确的是( )
 A、物质a可由H2在b点燃得到 B、可溶性e中的阴离子可用AgNO3溶液和稀硝酸检验 C、物质d是漂白粉的有效成分 D、物质b与水反应可以得到d
A、物质a可由H2在b点燃得到 B、可溶性e中的阴离子可用AgNO3溶液和稀硝酸检验 C、物质d是漂白粉的有效成分 D、物质b与水反应可以得到d -
7、下列与“物质的量”相关的计算不正确的是( )A、有CO、CO2、O3三种气体,它们各含有1molO,则三种气体物质的量之比为3∶2∶1 B、两种物质的物质的量相同,则它们在标准状况下的体积不一定相同 C、标准状况下,aL氧气和氮气的混合物含有的分子数约为 D、在同温同体积时,气体的物质的量越大,则压强越大
-
8、对于下列事实和相应解释有错误的是( )
选项
事实
解释
A
钠保存在煤油中
煤油不与钠发生反应,钠的密度比煤油大,煤油可以隔绝空气和水蒸气
B
将一小块儿钠投入饱和NaOH溶液中,恢复到原温度后溶液中数目增多
钠与水反应有NaOH生成,所以溶液中数目增多
C
用无锈铁丝蘸取待测液在酒精灯外焰灼烧,透过蓝色钴玻璃,火焰呈紫色
待测液一定含钾元素,可能含钠元素
D
钠长期暴露在空气中的产物是
是钠与空气中的氧气、水和二氧化碳反应的结果
A、A B、B C、C D、D -
9、用NA表示阿伏加德罗常数,下列叙述正确的是( )A、标准状况下,22.4LH2O中含有的分子数为NA B、标准状况下,22.4L氦气与22.4L氯气所含原子数均为2NA C、18g所含电子数为11NA D、16g氧气和臭氧的混合物中氧原子数为NA
-
10、工业废水中含有的重铬酸根离子()有毒,必须处理达标后才能排放。工业上常用绿矾()作处理剂,该反应的化学方程式为(未配平),下列说法正确的是( )A、还原性: B、该反应的氧化产物为 C、每消耗 , 同时生成2.9gK2SO4 D、若有1mol参与反应生成6mol水
-
11、下列反应的离子方程式书写正确的是( )A、钠与水反应: B、在NaHSO4溶液中滴入溶液至恰好沉淀: C、向溶液中通入: D、84消毒液在使用时可与空气中的:
-
12、某澄清透明溶液中可能含有①Na+②③Cl-④⑤⑥H+⑦OH-⑧Ba2+中的几种,且每种离子的个数均相等,依次进行下列实验,每步所加试剂均过量,观察到的现象如下:
步骤
操作
现象
(1)
向溶液中滴加2~3滴紫色石蕊溶液
溶液变红
(2)
向溶液中滴加BaCl2溶液和稀盐酸
有白色沉淀生成
(3)
将(2)中所得混合物过滤,向滤液中加入AgNO3溶液和稀硝酸
有白色沉淀生成
下列结论不正确的是( )
A、由操作(1)可知溶液中一定不含OH-、、 B、肯定含有的离子是Na+、、Cl-、H+ C、操作(2)和操作(3)中的白色沉淀分别为BaSO4和AgCl D、肯定不含有的离子是Cl-、、、OH-、Ba2+ -
13、下列物质分类的正确组合是( )
选项
混合物
纯净物
单质
电解质
非电解质
A
盐酸
石墨
溶液
(蔗糖)
B
空气
胶体
铁
C
水银
铜
D
氨水
胆矾
A、A B、B C、C D、D -
14、下列各项中两组物质在溶液中的反应,可用同一离子方程式表示的是( )A、: B、: C、: D、:
-
15、常温下,向某浓度的硫酸铜溶液中分别加入硫酸铜固体和Ba(OH)2固体,随着二者的加入,溶液的导电性变化如图所示,下列分析合理的是( )
 A、若将Ba(OH)2固体换成BaCl2固体,图像无变化 B、原硫酸铜溶液可能是饱和溶液 C、N点时CuSO4和Ba(OH)2恰好完全反应 D、M点后曲线表示的是新加入的硫酸铜固体生成了胆矾晶体,使溶液浓度减小
A、若将Ba(OH)2固体换成BaCl2固体,图像无变化 B、原硫酸铜溶液可能是饱和溶液 C、N点时CuSO4和Ba(OH)2恰好完全反应 D、M点后曲线表示的是新加入的硫酸铜固体生成了胆矾晶体,使溶液浓度减小 -
16、“遥遥领先”的华为芯片制造过程用了蚀刻技术。利用NF3进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。该反应微观示意图如下,下列说法不正确的是( )
 A、物质丁是空气中含量最多的气体 B、反应生成的丙和丁微粒数之比为1∶1 C、丙物质为气体 D、上述反应为置换反应
A、物质丁是空气中含量最多的气体 B、反应生成的丙和丁微粒数之比为1∶1 C、丙物质为气体 D、上述反应为置换反应 -
17、用“●”和“○”表示不同元素的原子,下列微观示意图能表示纯净物的是( )A、
 B、
B、 C、
C、 D、
D、
-
18、逻辑推理是化学学习中常用的思维方法。下列推理正确的是( )A、中和反应有盐和水生成,则有盐和水生成的反应一定是中和反应 B、单质是由一种元素组成的纯净物,则由一种元素组成的纯净物一定是单质 C、氧化物中含有氧元素,则含有氧元素的化合物一定是氧化物 D、置换反应有单质生成,则有单质生成的反应一定是置换反应
-
19、朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成种种美景的本质原因是( )A、空气中的小水滴颗粒直径为1~100nm B、空气中的小水滴颗粒的运动 C、雾是一种胶体,胶粒带有电荷 D、光的折射作用
-
20、从CO2捕获技术应用中分离出CO2 , 作原料气体来合成基础化工品是很有前景的方法。(1)、研究表明二氧化碳与氢气在某催化剂作用下可以还原为甲醇,该反应如下:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。反应历程如图所示(吸附在催化剂表面的物质用*标注,如*CO2表示单个CO2分子吸附在催化剂表面;图中*H已省略)。

①上述合成甲醇的反应过程中决定反应速率的步骤是(用化学方程式表示)。
②该过程的热化学反应方程式为。
③有利于提高平衡时CO2转化率的措施有(填字母)。
a.使用催化剂 b.增大压强 c.增大CO2和H2的初始投料比 d.升高温度
(2)、在催化剂(Ni/xMg)作用下二氧化碳与氢气反应还可以还原为甲烷,反应如下CO2(g)+4H2(g) CH4(g)+2H2O(g)。以5 mol H2和1 mol CO2为初始原料,保持总压为P0发生反应,不同温度下在相同时间测得CO2的转化率如图。
①三种催化剂(Ni/xMg)中,催化效果最好的是。使用Ni催化反应1.2 min达到A点,化学反应速率v(H2)=g∙min-1。
②下列表述能说明反应达到平衡的是。
a.v正(H2)=2v逆(H2O) b.气体压强不变 c.气体总质量不变 d.气体总体积不变
③B点的平衡常数Kp计算式为 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)、催化电解吸收CO2的KOH溶液(主要溶质为KHCO3)可将CO2转化为有机物。在相同条件下,随电解电压的变化阴极产物也发生变化。①当电压较低时,电解过程中没有含碳产物生成,阴极主要还原产物为。
②当电压较高时,电解生成C2H4和HCOO-消耗的电量之比为3:1,则C2H4和HCOO-物质的量之比为。