相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、酒石酸是一种二元弱酸,下列关于的说法中不正确的是:( )A、向溶液中加水稀释,增大 B、属于正盐 C、向水中加入固体 , 可促进水的电离 D、溶液中:
-
2、下列有关电极方程式或离子方程式正确的是( )A、铅酸蓄电池充电时的阳极反应: B、用银作电极电解稀盐酸: C、与稀硝酸反应: D、硫化钠溶液中加入少量氯化铁溶液:
-
3、在给定条件下,一定能大量共存的离子组是( )A、加溶液显红色的溶液: B、使酚酞变红色的溶液中: C、与反应能放出的溶液中: D、在的溶液中:
-
4、和在恒容密闭容器中发生反应: . 已知的键能分别为(a、b、c均大于零).下列说法正确的是( )A、 , 则 B、氢原子与溴原子形成分子需吸收能量 C、氢气与溴单质充分反应后,放出的能量总是小于 D、若氢气与溴单质充分反应放出能量,消耗的和均大于
-
5、下列说法正确的是( )
 A、图1可用于稀硫酸和溶液反应的中和热测定 B、图2可用于由制取无水固体 C、图3可用于模拟钢铁的析氢腐蚀 D、图4可用标准溶液测定某醋酸溶液的物质的量浓度
A、图1可用于稀硫酸和溶液反应的中和热测定 B、图2可用于由制取无水固体 C、图3可用于模拟钢铁的析氢腐蚀 D、图4可用标准溶液测定某醋酸溶液的物质的量浓度 -
6、下列化学用语或说法中正确的有( )A、B原子由时,由基态转化为激发态,形成吸收光谱 B、疏原子最外层的电子排布
 违背了泡利原理
C、第三周期基态原子的第一电离能介于铝、磷之间的元素有3种
D、基态原子价层电子排布式为的元素的族序数一定为
违背了泡利原理
C、第三周期基态原子的第一电离能介于铝、磷之间的元素有3种
D、基态原子价层电子排布式为的元素的族序数一定为
-
7、已知是阿伏加德罗常数的值,下列说法中不正确的是( )A、的溶液中数目为 B、常温下的氢氧化钠溶液中由水电离出的的数目为 C、重水中所含质子数为 D、标准状况下将通入足量水中,溶液中数目之和小于
-
8、下列化学用语不正确的是( )A、基态原子最高能级电子云轮廓图:
 B、F-的结构示意图:
B、F-的结构示意图: C、总共含有4个能级的能层符号:N
D、第三周期中未成对电子数最多且中子数为17的元素的原子:
C、总共含有4个能级的能层符号:N
D、第三周期中未成对电子数最多且中子数为17的元素的原子:
-
9、下列水溶液因水解呈酸性的是( )A、 B、 C、 D、
-
10、滴定是分析化学重要的分析方法,根据其原理回答下列问题:(1)、Ⅰ.用0.1000mol/L的盐酸滴定某未知浓度的NaOH溶液(装置如图),某次滴定前、后盛放盐酸的滴定管中液面的位置。
仪器B的名称是。 (2)、此次滴定消耗的盐酸是mL。(3)、由下表可知,三次滴定中,有一次滴定所用标准盐酸体积有明显偏差,可能的原因是。(填写相应的字母)
(2)、此次滴定消耗的盐酸是mL。(3)、由下表可知,三次滴定中,有一次滴定所用标准盐酸体积有明显偏差,可能的原因是。(填写相应的字母)待测NaOH溶液体积(mL)
标准盐酸体积
滴定前的刻度(mL)
滴定后的刻度(mL)
10.00
0.40
20.50
10.00
2.10
24.20
10.00
4.10
24.00
a.锥形瓶用待测液润洗
b.滴定前滴定管尖嘴部分有气泡,滴定结束时气泡消失
c.滴定过程中锥形瓶中溶液溅出瓶外
d.滴定结束时,俯视读数
(4)、Ⅱ.高锰酸钾常用于亚硝酸盐含量的测定。有化学小组测定某样品中的含量,设计如下实验:①称取样品a g,加水溶解,配成100mL溶液
②取25.00mL溶液于锥形瓶中,用标准溶液(酸性)进行滴定,滴定终点时消耗标准溶液V mL。
向滴定管中注入标准溶液之前的一步操作为。
(5)、高锰酸钾溶液应装在如图滴定管中。(填a或b) (6)、达到滴定终点时的现象是。
(6)、达到滴定终点时的现象是。 -
11、已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如表所示
酸
电离平衡常数
醋酸
K=1.75× 10-5
碳酸
K1=4.5×10-7 K2=4.7×10-11
亚硫酸
K1=1.4×10-2 K2=6.0×10-8
(1)、醋酸在水溶液中的电离方程式为: , 根据上表可知,酸性H2CO3H2SO3(填“>”“<”或“=”,下同),在相同条件下,试比较同浓度Na2CO3、Na2SO3溶液的 PH:Na2CO3 Na2SO3(2)、向0.1mol/L的CH3COONa溶液中加入少量下列物质,其水解程度增大的是____(填字母)。
A、NaCl溶液 B、Na2CO3固体 C、NH4Cl溶液 D、CH3COONa固体(3)、NaHSO3是中学化学常见的物质。HSO3- , 在水溶液中存在两个平衡:HSO3—⇋H+SO32- Ka2 , HSO3-+H2O ⇋H2SO3+OH- Kh2
已知25℃时,Ka2>Kh2 , 则0.1mol/L NaHSO3溶液:
①溶液呈(填“酸性”“碱性”或“中性”)。
②溶液中 c(Na+)c(HSO3-)。(填“>”“<”或“=”)
-
12、根据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s),设计的原电池如图所示,其中盐桥内装琼脂-饱和KNO3溶液。请回答下列问题:
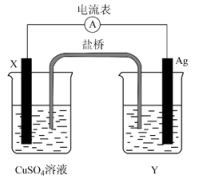 (1)、电极X的材料是;(填化学式,下同)电解质溶液Y是 。(2)、Ag是极。填(“正”或“负”)(3)、写出两电极的电极反应式:
(1)、电极X的材料是;(填化学式,下同)电解质溶液Y是 。(2)、Ag是极。填(“正”或“负”)(3)、写出两电极的电极反应式:银电极:;
X电极:。
(4)、外电路中的电子是从电极流向电极。(填电极材料名称)(5)、盐桥中向CuSO4溶液中迁移的离子是____(填字母)。A、K+ B、NO C、Ag+ D、SO(6)、1 mol Ag生成时,转移电子的物质的量为mol。 -
13、根据原电池的工作原理分析判断(填写“正极”或“负极”)。(1)、由组成原电池的电极材料判断。一般是活动性较强的金属为极,活动性较弱的金属或能导电的非金属为极。(2)、根据电流方向或电子流动方向判断。电流由极流向极;电子由极流向极。(3)、根据原电池中电解质溶液内离子的移动方向判断。在原电池的电解质溶液内,阳离子移向极,阴离子移向极。
-
14、要除去CuCl2溶液中的Fe3+ , 甲同学不知道调整溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38 ,
Cu(OH)2的溶度积Ksp=3×10-20 , 通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0mol•L-1 ,
(1)、则Cu(OH)2开始沉淀时溶液的pH为____A、4 B、4.4 C、5 D、5.5(2)、Fe3+完全沉淀时溶液的pH为____A、2 B、3 C、4 D、5(3)、通过调节溶液PH除去Fe3+而不损失Cu2+ , 调节PH的取值范围A、3≤PH<4 B、3≤PH≤4 C、2<PH≤3 D、2≤PH<3(4)、把a、b、c、d四种金属片浸泡在稀硫酸中,用导线两两相连,可以组成各种原电池。若a、b相连,a为正极;c、d相连,c为负极;a、c相连,c上产生气泡;b、d相连,b质量减小,则四种金属的活动性由强到弱顺序为:____。A、a>b>c>d B、b>c>a>d C、b>a>c>d D、a>c>b>d -
15、工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:(1)、为除去溶液中的Fe2+ , 可先加入____,(从下面四个选项选择)将Fe2+氧化为Fe3+A、CuO B、Cl2 C、Cu(OH)2 D、H2O2(2)、然后加入适量的____,(从下面四个选项选择)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。A、CuO B、Cl2 C、Fe(OH)3 D、H2O2
-
16、已知某温度下: , , 若加入来沉淀和 , 当溶液中和共存时,溶液中的为____。A、105 B、106 C、10-4 D、10-7
-
17、已知:20℃时,Ksp(AgCl)=1.1×10﹣10 , Ksp(AgBr)=2.0×10﹣13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,下列说法正确的是( )A、只有AgBr沉淀生成 B、AgCl与AgBr沉淀等量生成 C、AgCl与AgBr沉淀都有,但是以AgCl为主 D、AgCl与AgBr沉淀都有,但是以AgBr为主
-
18、有关下列装置的说法不正确的是( )
 A、图1所示不能构成原电池 B、图2锌锰干电池属于一次电池,锌作负极 C、图3是“纸电池”,Zn片失去电子,发生氧化反应 D、图4电池Al电极反应式为:Al-3e-+3H2O=Al(OH)3+3H+
A、图1所示不能构成原电池 B、图2锌锰干电池属于一次电池,锌作负极 C、图3是“纸电池”,Zn片失去电子,发生氧化反应 D、图4电池Al电极反应式为:Al-3e-+3H2O=Al(OH)3+3H+ -
19、某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图。下列说法正确的是( )
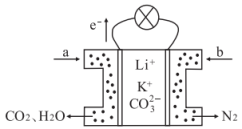 A、此电池在常温时也能工作 B、正极电极反应式为:O2+2CO2+4e-=2 C、向正极移动 D、a为CH4 , b为CO
A、此电池在常温时也能工作 B、正极电极反应式为:O2+2CO2+4e-=2 C、向正极移动 D、a为CH4 , b为CO -
20、将AgCl分别投入下列溶液中:
1. 40mL0.03mol·L-1的HCl溶液
2. 50mL0.03mol·L-1的AgNO3溶液
3. 30mL0.02mol·L-1的CaCl2溶液
4. 10mL蒸馏水
AgCl的溶解度由大到小的顺序是____。
A、1=2>3>4 B、3>1=2>4 C、4>1=2>3 D、4>3>2>1