相关试卷
- 江西省九江市重点高中2016-2017学年高二下学期化学开学考试试卷
- 高中化学人教版选修4 第一章 单元测试卷
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.3化学键
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.2元素周期表和元素周期律的应用
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.2.1原子核外电子的排布
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.3核素
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.2元素的性质与原子结构
- 2017_2018学年高中化学新人教版必修二 第一章物质结构元素周期律1.1.1元素周期表
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.2资源综合利用环境保护
- 2017_2018学年高中化学新人教版必修二 第四章化学与自然资源的开发利用4.1.2海水资源的开发利用
-
1、铜镁合金完全溶解于密度为、质量分数为63%的浓硝酸中,得到和的混合气体(换算为标准状况),向反应后的溶液中加入溶液,当金属离子全部沉淀时,得到沉淀,下列说法不正确的是( )。A、该合金中铜与镁的物质的量之比是 B、该浓硝酸中的物质的量浓度是 C、和的混合气体中,的体积分数是80% D、得到2.54沉淀时,加入溶液的体积是
-
2、如图所示,向密闭容器内可移动活塞的两边分别充入、和的混合气体(已知体积占整个容器体积的),将和的混合气体点燃引爆。活塞先左弹,恢复室温后,活塞右滑并停留于容器的中央。下列说法不正确的是( )。
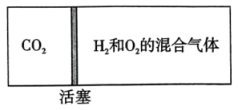 A、活塞移动情况说明、燃烧放热,且该反应气体分子数减少 B、反应前,活塞左右两边气体原子数之比为 C、原来和的体积之比一定是 D、反应后恢复到室温,活塞左右两边气体的物质的量相等
A、活塞移动情况说明、燃烧放热,且该反应气体分子数减少 B、反应前,活塞左右两边气体原子数之比为 C、原来和的体积之比一定是 D、反应后恢复到室温,活塞左右两边气体的物质的量相等 -
3、工业生产中除去电石渣浆(含)中的并制取硫酸盐的一种常用流程如图所示。下列说法正确的是( )。
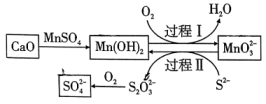 A、碱性条件下,氧化性: B、过程Ⅱ中,反应的离子方程式为 C、将转化为理论上需要的体积为(标准状况) D、该过程中涉及的化学反应均是氧化还原反应
A、碱性条件下,氧化性: B、过程Ⅱ中,反应的离子方程式为 C、将转化为理论上需要的体积为(标准状况) D、该过程中涉及的化学反应均是氧化还原反应 -
4、短周期主族元素W、X、Y、Z、Q原子序数依次增大,形成的化合物是一种重要的食品添加剂,结构如图所示。Z核外最外层电子数与X核外电子总数相等。W的原子半径在周期表中最小。下列有关叙述正确的是( )。
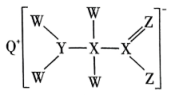 A、原子半径大小:Y>Z>Q B、W、Y、Z三种元素可形成离子化合物 C、该化合物中Y原子不满足8电子稳定结构 D、Z与W可形成 , 其空间结构是直线形
A、原子半径大小:Y>Z>Q B、W、Y、Z三种元素可形成离子化合物 C、该化合物中Y原子不满足8电子稳定结构 D、Z与W可形成 , 其空间结构是直线形 -
5、铝元素是地壳中含量最多的金属元素(约占地壳总量的7.73%),主要以铝土矿形式存在(主要成分是)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
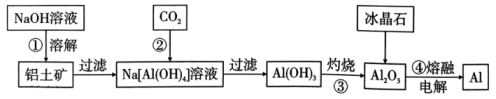
下列说法正确的是( )。
A、碱溶①后,溶液中主要含有的阳离子为和 B、步骤②通入足量反应的离子方程式为 C、灼烧③一般在蒸发皿中进行 D、电解④添加冰晶石的主要作用是降低的熔融温度 -
6、如图所示实验装置及实验结果合理的是( )。
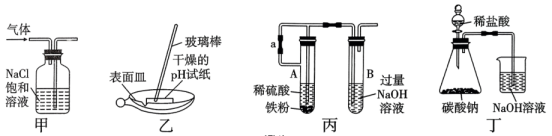 A、实验室用图甲所示装置除去中的少量 B、实验室用图乙所示装置测定氯水的pH C、实验室用图丙所示装置制备少量 , 先打开止水夹a,一段时间后再关闭a D、实验室用图丁所示装置证明非金属性强弱:Cl>C
A、实验室用图甲所示装置除去中的少量 B、实验室用图乙所示装置测定氯水的pH C、实验室用图丙所示装置制备少量 , 先打开止水夹a,一段时间后再关闭a D、实验室用图丁所示装置证明非金属性强弱:Cl>C -
7、下列离子方程式书写正确的是( )。A、向溶液中加入少量溶液: B、二氧化硫使酸性高锰酸钾溶液褪色: C、氢氧化镁与足量稀盐酸反应: D、已知酸性: , 向溶液中通入少量:
-
8、实验室需用硫酸铜溶液,下列有关该溶液的配制说法正确的是( )。A、用托盘天平称取胆矾 B、实验中必须用到的玻璃仪器为:烧杯、量筒、容量瓶、玻璃棒 C、定容时仰视容量瓶的刻度线,会造成所配溶液物质的量浓度偏高 D、定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线
-
9、侯德榜(图乙)是我国近代著名的化学家,他提出的联合制碱法得到世界各国的认可。以粗盐(含、、等杂质)为主要原料,生产纯碱和化肥 , 实验室模拟工艺流程如图甲所示。下列说法不正确的是( )。
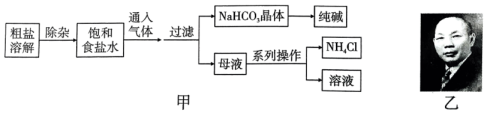 A、对粗盐提纯可依次加入过量、、溶液,过滤后再加入盐酸调pH B、向饱和食盐水中先通 , 再通 , 更有利于析出 C、图甲中析出晶体的总反应可表达为: D、向纯碱溶液中通入过量可以将纯碱溶液转化为溶液
A、对粗盐提纯可依次加入过量、、溶液,过滤后再加入盐酸调pH B、向饱和食盐水中先通 , 再通 , 更有利于析出 C、图甲中析出晶体的总反应可表达为: D、向纯碱溶液中通入过量可以将纯碱溶液转化为溶液 -
10、设为阿伏加德罗常数的值,下列说法正确的是( )。A、标准状况下,含的浓盐酸与足量的反应生成的体积为 B、的溶液中所含阳离子数目为 C、标准状况下,固体中含有的离子总数是 D、单质Fe与足量水蒸气在高温下完全反应,失去个电子
-
11、向两份相同体积、相同物质的量浓度的溶液中,分别滴入物质的量浓度相等的、溶液,其导电能力随滴入溶液体积(V)变化的曲线如图所示。下列说法正确的是( )。
 A、a、d两点对应的溶液均显中性 B、b点时对应的离子方程式为 C、c点时两溶液中的物质的量浓度相同 D、曲线①代表滴加溶液的变化曲线
A、a、d两点对应的溶液均显中性 B、b点时对应的离子方程式为 C、c点时两溶液中的物质的量浓度相同 D、曲线①代表滴加溶液的变化曲线 -
12、下列各组离子在指定溶液中一定能大量共存的是( )。A、常温下,的透明溶液中:、、、 B、与铝反应放出氢气的溶液中:、、、 C、使酚酞变红的溶液中:、、、 D、新制氯水中:、、、
-
13、下列有关周期表、周期律的叙述,正确的是( )。A、第ⅠA族除H外均为碱金属元素,对应单质均需要保存于煤油中 B、第ⅦA族卤素单质与水反应均可以用:来表示 C、同周期简单离子半径随原子序数增大而递减 D、锑(Sb)元素位于第五周期第ⅤA族,原子序数为51
-
14、下列各组物质的转化中,不是通过一步反应实现的是( )。A、 B、 C、 D、
-
15、下列叙述正确的有( )。
①酸性氧化物一定是非金属氧化物
②、都能溶于水生成碱,它们都属于碱性氧化物
③和互为同素异形体
④、、、均可通过化合反应制得
⑤已知: , 则不是电解质
⑥冰中水分子间以氢键结合成排列规整的晶体,体积膨胀密度减小,所以冰浮在水面上
A、1项 B、2项 C、3项 D、4项 -
16、下列关于化学键的说法正确的是( )。A、有化学键断裂的变化一定是化学变化 B、中含有极性键和非极性键 C、受热分解既破坏了离子键,又破坏了极性共价键 D、共价化合物中不可能含有金属元素
-
17、下列化学用语不正确的是( )。A、中子数为18的氯离子: B、的结构式: C、Rb的原子结构示意图:
 D、的电子式:
D、的电子式:
-
18、下列实验操作描述正确的是( )。A、制备氢氧化铁胶体实验时,用玻璃棒搅拌可加快反应速率 B、进行焰色试验时如无铂丝,可以用洁净的铁丝代替 C、实验剩余的药品都不可以放回原瓶 D、坩埚不可以用明火直接加热
-
19、化学与生活、社会发展息息相关,下列说法正确的是( )。A、“食物腐败,胶体净水,金属的冶炼”都涉及氧化还原反应 B、铁粉常作脱氧剂,生石灰、浓硫酸常作干燥剂 C、苏打可用于治疗胃酸过多 D、从石墨中剥离出的石墨烯薄片能导电,是一种电解质
-
20、无水四氯化锡()常用作媒染剂和部分有机合成的催化剂。某化学兴趣小组利用如图装置(部分加热装置略)制备并测定产品中含量。
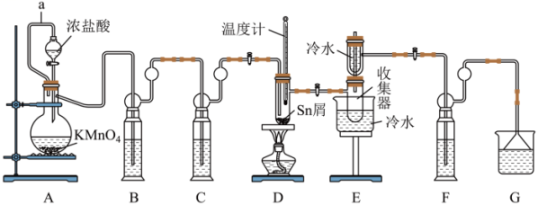
已知:①熔点为-33℃,沸点为114.1℃,在潮湿空气中极易潮解(水解生成),且熔融Sn与反应生成时放出大量的热。
②Sn熔点为232℃,无水熔点为246℃、沸点为652℃。
回答下列问题:
(1)、a管的作用是。(2)、装置B、C中的试剂分别为、(填名称)。(3)、为了获得较纯的产品,当D处具支试管中时,再点燃D处酒精灯。反应制得的产品中可能会含有杂质 , 为加快反应速率并防止产品中混有 , 除了通入过量外,还应控制反应的最佳温度范围为。(4)、甲同学欲证明装置A产生的气体中含有HCl,设计如图装置进行实验。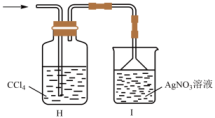
乙同学认为,不能确定进入装置I的气体只有一种,为证明最终进入装置I的气体只有一种,乙同学提出再加一个装置,即可完成论证。请给出改进方案:。
(5)、碘氧化法滴定分析产品中Sn2+的含量。准确称取ag产品于锥形瓶中,用蒸馏水溶解,淀粉溶液做指示剂,用b mol·L-1碘标准溶液滴定,发生反应:Sn2++I2=Sn4++2I-。滴定终点消耗碘标准溶液V mL,则产品中Sn2+的质量分数为(用含a、b、V的代数式表示)。