-
1、下列化学用语正确的是( )A、的电离方程式: B、的结构示意图:
 C、的电子式:
C、的电子式: D、与互为同分异构体
D、与互为同分异构体
-
2、“宏观辨识—微观探析—符号表征”是化学学习的重要方法。某化学反应的微观示意图如图,下列分析错误的是( )
 A、该反应属于氧化还原反应 B、上述示意图涉及的物质中有两种是电解质 C、上述示意图表示的反应对应的化学方程式: D、该反应实现了无机物向有机物的转化
A、该反应属于氧化还原反应 B、上述示意图涉及的物质中有两种是电解质 C、上述示意图表示的反应对应的化学方程式: D、该反应实现了无机物向有机物的转化 -
3、某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。(已知:C+2H2SO4(浓)CO2+2SO2↑+2H2O)(1)、有同学认为制得的SO2中可能混有杂质,其化学式为。(2)、为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。

①为验证并吸收SO2 , 装置B中加入的试剂为;装置C中品红溶液的作用是。
②装置H的作用为。
(3)、兴趣小组设计如图装置验证二氧化硫的化学性质。
①能验证SO2具有氧化性的实验现象为;
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是(填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为。
-
4、综合利用废弃物,对资源利用和环境保护具有现实意义。以废铁屑(含少量等杂质)为原料,制备硫酸亚铁晶体(),流程示意图如下。
 (1)、酸浸过程中,的作用是、、(用离子方程式表示)。(2)、酸浸时间对所得溶液的成分影响如下表所示。
(1)、酸浸过程中,的作用是、、(用离子方程式表示)。(2)、酸浸时间对所得溶液的成分影响如下表所示。酸浸时间
用溶液检验
变红
未变红
变红
①时检验,溶液变红,写出离子方程式
②时检验,用离子方程式表示溶液未变红的原因。
③时检验,溶液复又变红,用文字说明原因。
(3)、已知:受热易失水。操作X为: 。(4)、测定所得硫酸亚铁晶体中的含量,步骤如下:Ⅰ.称取硫酸亚铁晶体样品,配制成溶液。
Ⅱ.取出溶液,加入适量稀硫酸,滴入的溶液,至反应完全共消耗溶液。
①依题意完善Ⅱ中氧化的离子方程式
②计算硫酸亚铁晶体样品中的质量分数。
-
5、元素周期表是20世纪科学技术发展的重要理论依据之一,是我们学习化学的重要工具。为纪念元素周期表诞生150周年,等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。我国学者雷晓光、姜雪峰、刘庄分别成为“N、S、”元素的代言人。回答下列问题:(1)、汞的原子结构示意图如图所示,汞在周期表中位于第周期。氮、氧、硫3种元素对应的最简单氢化物,其中最稳定的是(填化学式)。
 (2)、下列有关性质的比较能用元素周期律解释的是____(填字母,下同)。A、酸性: B、非金属性: C、碱性: D、热稳定性:(3)、分别写出H2S、NH4Cl的电子式、。用电子式表示Na2S的形成过程。(4)、第三周期元素X,其最外层电子数与电子层数相同,该元素单质与氢氧化钠溶液反应的化学方程式为。(5)、短周期元素Y,其最高正化合价与最低负化合价的代数和为6,该元素单质与氢氧化钠溶液反应的离子方程式为。(6)、短周期元素Y,其最高正化合价与最低负化合价的代数和为4,该元素单质与氢氧化钠溶液加热条件下反应的离子方程式为。
(2)、下列有关性质的比较能用元素周期律解释的是____(填字母,下同)。A、酸性: B、非金属性: C、碱性: D、热稳定性:(3)、分别写出H2S、NH4Cl的电子式、。用电子式表示Na2S的形成过程。(4)、第三周期元素X,其最外层电子数与电子层数相同,该元素单质与氢氧化钠溶液反应的化学方程式为。(5)、短周期元素Y,其最高正化合价与最低负化合价的代数和为6,该元素单质与氢氧化钠溶液反应的离子方程式为。(6)、短周期元素Y,其最高正化合价与最低负化合价的代数和为4,该元素单质与氢氧化钠溶液加热条件下反应的离子方程式为。 -
6、三氯化六氨合钴(Ⅲ)是钴化合物合成中的重要原料,实验室以为原料制备。其中可以通过钴和纯净氯气反应制得,实验室制备可用下图实验装置实现。
已知:①钴单质
 以上易被氧气氧化,易潮解
以上易被氧气氧化,易潮解 (1)、写出A装置的化学方程式(2)、反应开始前应先打开A中盛放浓盐酸仪器的活塞,再点燃D中酒精灯,其目的是。(3)、新制氯水中,含有氯元素的微粒有(填微粒符号)。(4)、把氯气溶于水得到新制氯水,把该氯水加入滴有酚酞的溶液中,发现溶液红色褪去。为探究褪色的原因,有同学提出三种猜想:
(1)、写出A装置的化学方程式(2)、反应开始前应先打开A中盛放浓盐酸仪器的活塞,再点燃D中酒精灯,其目的是。(3)、新制氯水中,含有氯元素的微粒有(填微粒符号)。(4)、把氯气溶于水得到新制氯水,把该氯水加入滴有酚酞的溶液中,发现溶液红色褪去。为探究褪色的原因,有同学提出三种猜想:猜想1:氯水消耗了;
猜想2:氯水消耗了酚酞;
猜想3:氯水同时消耗了和酚酞。
为验证上述猜想,该同学取上述褪色后的溶液于甲、乙两只试管中。向甲试管中滴加足量溶液,向乙试管中滴加足量酚酞溶液,如果观察到(填实验现象),则猜想3成立。
(5)、该同学为了完成上述实验探究,在实验室配制氢氧化钠溶液。①配置该溶液需要称量氢氧化钠固体的质量是g。
②关于配制过程的说法正确的是(填字母)。
A.将称好的固体直接在容量瓶中加水溶解
B.将溶解后的溶液转移到容量瓶时,有少量的溶液溅出,会使所配溶液浓度偏低
C.容量瓶不干燥,含有少量蒸馏水,会使所配溶液浓度偏低
D.溶液未冷却到室温就移入容量瓶定容,会使所配溶液浓度偏高
-
7、工业上以铝土矿(主要成分是氧化铝,含氧化铁杂质)为原料冶炼铝的工艺流程如下,下列叙述正确的是( )
 A、反应①中试剂X是氢氧化钠溶液 B、试剂Y是 , 它与反应生成氢氧化铝 C、图中所示转化反应中包含2个氧化还原反应 D、将X与Y试剂进行对换,最终可以达到相同结果
A、反应①中试剂X是氢氧化钠溶液 B、试剂Y是 , 它与反应生成氢氧化铝 C、图中所示转化反应中包含2个氧化还原反应 D、将X与Y试剂进行对换,最终可以达到相同结果 -
8、下列关于性质实验的说法错误的是( )
 A、用如图装置可以制备 B、配制溶液,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度 C、可用溶液检验溶液中是否存在 D、向溶液中加入少量铁粉是为了防止被氧化
A、用如图装置可以制备 B、配制溶液,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度 C、可用溶液检验溶液中是否存在 D、向溶液中加入少量铁粉是为了防止被氧化 -
9、“侯氏制碱法是我国化工专家侯德榜为世界制碱工业作出的突出贡献。“侯氏制碱法”是将二氧化碳通入含有氨气的饱和溶液中,结晶、过滤得到晶体,加热分解制得。下列关于和说法不正确的是( )A、用澄清石灰水鉴别和 B、相同温度下,向同浓度和溶液中分别滴加几滴酚酞,溶液的红色较深 C、相同温度下,相同浓度和溶液分别与的稀盐酸反应,较剧烈 D、固体中含有少量杂质,可通过加热的方法除去
-
10、关于以下实验装置,说法不正确的是( )
 A、用装置A盛装NH4Cl粉末来制取氨气,并用向下排气法收集 B、装置B既可以防止倒吸,又可以检查实验时装置B后的装置是否发生堵塞 C、装置C、F中盛装的试剂分别为浓硫酸、碱石灰,装置C用来除去Cl2中的水蒸气,装置F用来防止空气中的水蒸气进入装置E D、装置D中的产物受热易升华,最好用粗短导管连接装置D、E
A、用装置A盛装NH4Cl粉末来制取氨气,并用向下排气法收集 B、装置B既可以防止倒吸,又可以检查实验时装置B后的装置是否发生堵塞 C、装置C、F中盛装的试剂分别为浓硫酸、碱石灰,装置C用来除去Cl2中的水蒸气,装置F用来防止空气中的水蒸气进入装置E D、装置D中的产物受热易升华,最好用粗短导管连接装置D、E -
11、下表是各物质及其所含的少量杂质,以及除去这些杂质所选用的试剂或操作方法,其中不正确的是( )
选项
物质
杂质
除杂试剂或操作方法
A
FeCl2溶液
FeCl3
加入过量铁粉,再过滤
B
NaHCO3溶液
Na2CO3
通入过量的CO2气体
C
NaNO3溶液
Na2SO4
加入适量的BaCl2溶液,再过滤
D
MgO固体
Al2O3
加入过量的NaOH溶液,再过滤
A、A B、B C、C D、D -
12、下图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系,下列说法正确的是( )
 A、铁与高温水蒸气的反应可实现上述转化① B、不稳定,在空气中受热,迅速发生转化② C、中加稀(强氧化剂)可实现转化⑦ D、加热发生转化⑥,但加水不能转化为
A、铁与高温水蒸气的反应可实现上述转化① B、不稳定,在空气中受热,迅速发生转化② C、中加稀(强氧化剂)可实现转化⑦ D、加热发生转化⑥,但加水不能转化为 -
13、一种用作锂离子电池电解液的锂盐的阴离子结构如图所示,X、Y、Z、W为原子序数依次增大的短周期主族元素,W的核外电子中有3个未成对电子。下列说法正确的是( )
 A、W元素最高价氧化物对应的水化物是强酸 B、该阴离子中不存在非极性键 C、X的氢化物沸点可能高于Z的氢化物 D、该离子中所有原子最外层均为8电子结构
A、W元素最高价氧化物对应的水化物是强酸 B、该阴离子中不存在非极性键 C、X的氢化物沸点可能高于Z的氢化物 D、该离子中所有原子最外层均为8电子结构 -
14、如图所示为元素周期表的一部分,其中X、Y、Z、W为四种短周期元素。Z元素原子核外K层与M层上的电子数相等。下列说法中正确的是( )
 A、Y元素的最高价氧化物对应的水化物的化学式为 B、最高价氧化物对应水化物的酸性: C、原子半径由小到大的顺序为 D、X、Z两种元素的氧化物中所含化学键的类型相同
A、Y元素的最高价氧化物对应的水化物的化学式为 B、最高价氧化物对应水化物的酸性: C、原子半径由小到大的顺序为 D、X、Z两种元素的氧化物中所含化学键的类型相同 -
15、实验室配制的溶液,下列说法错误的是( )A、称量时,若将固体置于托盘天平右盘,将导致所配溶液浓度偏小 B、将固体置于烧杯中溶解,冷却至室温后转移到容量瓶中 C、定容时仰视刻度线,会使所配溶液浓度偏小 D、定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线
-
16、表示阿伏加德罗常数的值,下列说法正确的是( )A、金属镁变成镁离子时失去的电子数为 B、物质的量浓度为的溶液中,含有个数为 C、常温常压下,氯气所含原子数目为 D、中含有的电子数为
-
17、下列有关化学用语表示正确的是( )A、氯化镁的电子式:
 B、溶于水的电离方程式:
C、次氯酸的结构式:
D、氧离子(O2-)结构示意图:
B、溶于水的电离方程式:
C、次氯酸的结构式:
D、氧离子(O2-)结构示意图:
-
18、金属钛对人体体液无毒且能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关和的说法正确的是( )A、和的质子数相同,互为同位素 B、和的质量数不同,属于两种元素 C、和的质子数相同,是同一种核素 D、和的质子数相同,中子数不同,互为同素异形体
-
19、关于一些重要的化学概念,下列叙述错误的个数是( )
①CO2、CO、SO2均为酸性氧化物
②盐酸、NaOH溶液、NaCl固体均能导电
③能电离出H+的物质不一定是酸,酸的元数不一定等于所含的氢原子个数
④需要通电才可进行的有:电解、电泳、电离
⑤盐酸、亚硫酸、氯气分别为强电解质、弱电解质和非电解质
A、2个 B、3个 C、4个 D、5个 -
20、某含锰废料中主要含MnCO3及少量的FeCO3、SiO2、Cu2(OH)2CO3 , 以此为原料制备MnO2的流程如下:
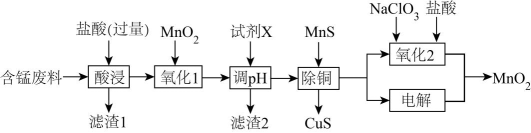
Ⅰ.氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物
Mn(OH)2
Fe(OH)2
Fe(OH)3
Cu(OH)2
开始沉淀时pH
8.3
6.3
2.7
4.7
完全沉淀时pH
9.8
8.3
3.7
6.7
Ⅱ.常温下Ksp(MnS)=2.0×10-10、Ksp(CuS)=6.0×10-36。
回答下列问题:
(1)、滤渣1的主要成分是(填化学式)。(2)、“氧化1”的目的是(用离子方程式表示)。(3)、“调pH”时,试剂X为(任写一种),pH的调节范围为。(4)、“除铜”时,当溶液中c(Mn2+)=12mol·L-1 , 溶液中c(Cu2+)=。(5)、“氧化2”制备MnO2 (恰好完全反应)时,n(Mn2+):n(ClO)=( ClO→Cl-);“电解”制备MnO2的阳极电极反应式为。