相关试卷
- 江苏省扬州市江都区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市高新区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省常州市2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市工业园区2017-2018学年九年级上学期化学12月调研考试试卷
- 江苏省扬州市江都区五校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省扬州市邗江区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省泰州市医药高新区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省常州市金坛区2017-2018学年九年级上学期化学期中质量调研考试试卷
- 江苏省扬州实验学校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省苏州市相城区2015-2016学年九年级化学一模考试试卷(4月)
-
1、为了防止铁制品锈蚀,下列做法不恰当的是A、在脸盆、杯子等表面烧涂搪瓷 B、将使用后的菜刀用布擦干 C、在铁制品表面涂油漆 D、要经常用钢刷擦洗铝锅上的污垢
-
2、现有X、Y、Z三种金属,放入稀硫酸中只有Y表面有气泡产生,如果把X、Z放入硝酸银溶液中,在Z表面有银析出,而X表面没有明显变化,则三种金属的活动性顺序为A、 B、 C、 D、
-
3、生活处处即化学,对下列生活现象解释合理的是A、煤粉比煤块燃烧更旺——增大与氧气的接触面积 B、消防员用高压水枪灭火——隔绝空气 C、油锅着火放入青菜后熄灭——降低油的着火点 D、移除炉灶内木柴后灶火熄灭——隔绝空气
-
4、构建化学基本观念是学好化学的基础。下列对化学基本观念的认识错误的是A、守恒观:镁条在空气中燃烧前后质量对比,发现质量增加,不符合质量守恒定律 B、微粒观:保持一氧化碳化学性质的最小粒子是一氧化碳分子 C、转化观:在一定条件下,二氧化碳和一氧化碳可以相互转化 D、元素观:金刚石和石墨都是由碳元素组成的
-
5、我国高铁列车依靠车顶的受电弓滑板与接触网持续摩擦获取电力,从而维持高速运行。石墨可用于制造受电弓滑板,这一应用主要与石墨的下列性质无关的是A、滑腻感 B、可燃性 C、导电性 D、熔点高
-
6、立信化学兴趣小组的同学将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如下表,下列说法错误的是
物质
甲
乙
丙
丁
反应前质量/g
30
20
5
0
反应后质量/g
14
16
a
20
A、 B、甲、乙参加反应的质量比为 C、该反应属于化合反应 D、丙一定是催化剂 -
7、实验现象的正确描述和记录是学好化学的关键之一。下列实验现象描述正确的是A、红磷在空气中燃烧,产生大量白色烟雾 B、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体物质 C、硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成有刺激性气味的气体 D、木炭在氧气中燃烧,发出白光,生成二氧化碳
-
8、2024年世界地球日的主题是“珍爱地球,人与自然和谐共生”。下列做法不符合这一主题的是A、增大绿化面积,改善空气质量 B、露天焚烧秸秆,增强土壤肥性 C、减少燃煤发电,推广新型能源 D、采用绿色工艺,处理工业废水
-
9、下列实验操作正确的是A、
 滴加液体
B、
滴加液体
B、 读取液体体积
C、
读取液体体积
C、 闻试剂气味
D、
闻试剂气味
D、 倾倒液体
倾倒液体
-
10、下列过程中发生化学变化的是A、冰雪消融 B、铁钉生锈 C、沙里淘金 D、铁杵磨针
-
11、下列实验操作中,“先”与“后”的顺序错误的是A、制备气体时,先装药品,后检查装置的气密性 B、给试管中的药品加热时,先预热,再对着试管中药品部位集中加热 C、将玻璃管插入带孔橡胶塞时,先把管口用水湿润,后对准橡胶塞上的孔转动插入 D、检查气密性时,先把导管一端浸入水中,再双手紧握试管外壁
-
12、建立模型是学习化学的重要方法。下列模型正确的是A、
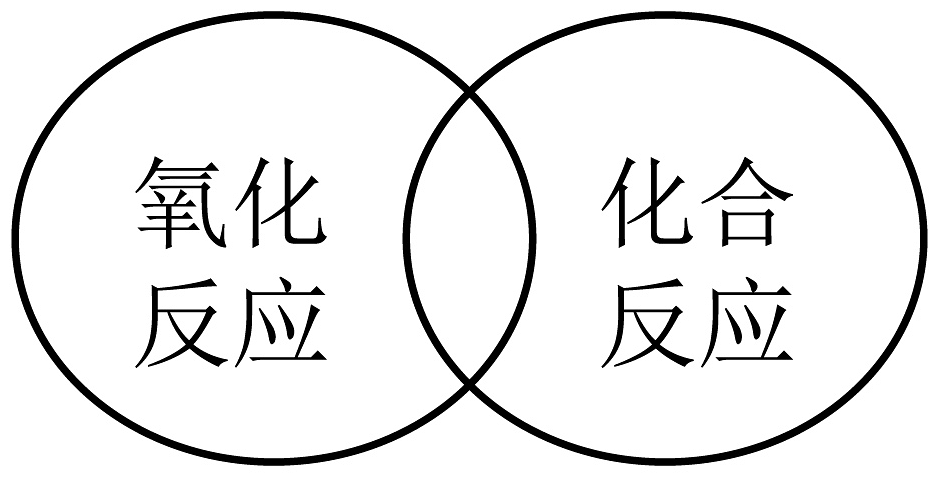 化学反应分类
B、
化学反应分类
B、 物质的分类
C、
物质的分类
C、 空气的成分
D、
空气的成分
D、 可加热仪器分类
可加热仪器分类
-
13、项目小组利用如图所示装置电解水并收集干燥的氢气和氧气。
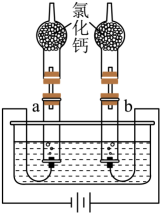 (1)、接通电源,收集a气体,靠近火焰,观察到气体燃烧,发出淡蓝色火焰,说明该气体是(填“氢气”或“氧气”)。(2)、一段时间后断开电源,实验前后整个装置的质量减少了0.9g,写出通电过程中反应的化学方程式并计算生成氧气的质量(不考虑水的蒸发)。
(1)、接通电源,收集a气体,靠近火焰,观察到气体燃烧,发出淡蓝色火焰,说明该气体是(填“氢气”或“氧气”)。(2)、一段时间后断开电源,实验前后整个装置的质量减少了0.9g,写出通电过程中反应的化学方程式并计算生成氧气的质量(不考虑水的蒸发)。 -
14、一氧化碳与氧化铜反应除生成二氧化碳外,还生成铜、氧化亚铜中的一种或两种。项目小组取4.00g氧化铜,对一氧化碳还原氧化铜的反应展开系列探究。
Ⅰ.利用下图所示装置制取一氧化碳并还原氧化铜
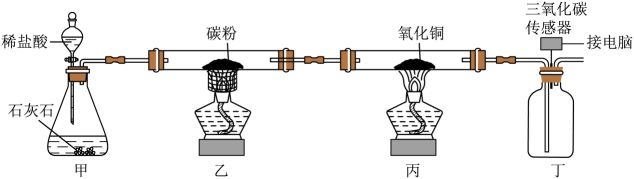 (1)、以下为与实验有关的图标,其中提示实验中会用到加热操作的是____(填标号)。A、
(1)、以下为与实验有关的图标,其中提示实验中会用到加热操作的是____(填标号)。A、 B、
B、 C、
C、 (2)、装置甲锥形瓶内反应的化学方程式为。(3)、实验中部分操作及现象如下:
(2)、装置甲锥形瓶内反应的化学方程式为。(3)、实验中部分操作及现象如下:a.加入稀盐酸,观察到二氧化碳传感器示数不断增大至稳定;
b.点燃酒精灯;加热碳粉;
c.点燃酒精灯,加热氧化铜;
d.观察到氧化铜处黑色粉末全部变红;停止加热,收集尾气。
①从安全环保的角度考虑,以上操作正确的顺序为:(填标号)。
②二氧化碳传感器示数不断增大至稳定,说明装置内已充满二氧化碳。若无二氧化碳传感器,检验装置内已充满二氧化碳的实验方法是(简述实验操作和现象)。
Ⅱ.探究装置丙硬质玻璃管内剩余固体的性质并测定其组成
查阅资料:氧化亚铜为红色粉末,可与稀硫酸反应生成铜、硫酸铜和水。
实验Ⅰ结束后将装置丙硬质玻璃管内的剩余固体全部移至烧杯中,加入足量稀硫酸,充分反应,滤出烧杯中的红色固体,洗涤、干燥、称量,其质量为2.56g。
(4)、装置丙硬质玻璃管内剩余固体中铜单质的质量分数为(结果精确到0.1%)。 -
15、氯化镁产品大多数是黄褐色或白色固体,习惯称为卤片。某卤片的主要成分为 , 还含少量、NaCl和 , 以该卤片为原料生产的工艺流程示意图如下所示。
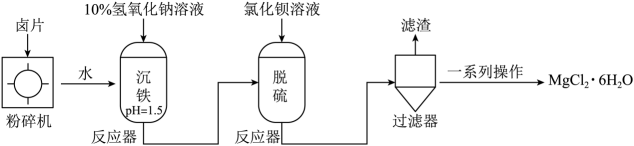
已知:①。
②时,氢氧化铁开始沉淀;时,氢氧化铁沉淀完全。
③时,氢氧化镁开始沉淀;时,氢氧化镁沉淀完全。
(1)、配制50g质量分数为10%的氢氧化钠溶液,下图中的仪器不会用到的是____(填标号)。A、 B、
B、 C、
C、 (2)、“沉铁”时,调节溶液 , 该溶液呈性。(3)、加入适量氯化钡溶液可实现“脱硫”,反应的化学方程式为。(4)、“滤渣”的成分为。(5)、为制备 , “一系列操作”中宜采用降温结晶,而不宜采用蒸发结晶,其原因是(答两点)。
(2)、“沉铁”时,调节溶液 , 该溶液呈性。(3)、加入适量氯化钡溶液可实现“脱硫”,反应的化学方程式为。(4)、“滤渣”的成分为。(5)、为制备 , “一系列操作”中宜采用降温结晶,而不宜采用蒸发结晶,其原因是(答两点)。 -
16、是配制无土栽培营养液常用的三种物质,它们在不同温度时的溶解度如下表所示。
温度/℃
0
20
40
60
80
100
溶解度/g
29.4
37.2
45.8
55.2
65.6
77.3
41.6
53.8
70.5
75.4
71.1
60.5
13.3
31.6
63.9
110
169
246
(1)、的溶解度随温度的升高而(填“增大”“减小”或“不变”)。(2)、配制营养液时,为加快在水中的溶解,可采用的一种方法是。(3)、配制某无土栽培营养液需补充钾元素195g,则需的质量为。(4)、对上表中某一种物质的溶液进行如图所示实验。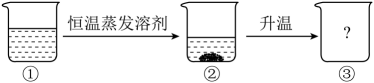
编号①、②、③的溶液中溶质质量分数的大小关系可能是____(填标号)。
A、①<②<③ B、①=②=③ C、①>②>③ D、③<①<② -
17、便携式供氧器广泛用于医疗急救、航空航天、水下作业等领域。某项目小组从制氧剂选择和装置优化等方面开展简易供氧器设计和制作的跨学科实践活动。
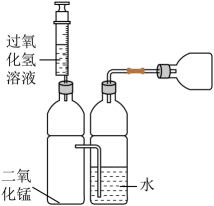
制氧剂
制氧原理
生产1kg氧气所需成本
30%过氧化氢溶液
约13元
氯酸钠
约11元
高锰酸钾
约148元
回答下列问题:
(1)、上表中生产1kg氧气所需成本最低的制氧剂是____(填标号)。A、30%过氧化氢溶液 B、氯酸钠 C、高锰酸钾(2)、某同学设计的简易供氧器如图所示,制取氧气的化学方程式为。(3)、上表中三种制氧原理均属于(填基本反应类型)。 -
18、项目小组为探究金属的化学性质进行图1所示实验,充分反应后,甲试管内的溶液只含一种溶质。然后将甲、乙两支试管内的物质倒入烧杯,如图2所示。充分反应后过滤,得到滤渣和滤液。
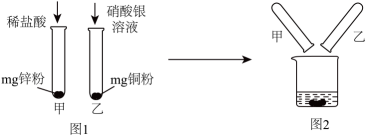
下列说法错误的是( )
A、若滤液呈无色,则滤渣中可能存在3种物质 B、若滤液呈蓝色,则滤渣中可能存在2种物质 C、若滤渣为混合物,则其质量可能小于2mg D、若滤渣为纯净物,则滤液中可能存在3种金属离子 -
19、将可燃物与过量氧气在密闭容器中用电火花引燃,除生成二氧化碳外,还可能生成水。充分反应后,容器内氧气减少了。实验过程中生成二氧化碳的质量随时间的变化关系如图所示。下列说法正确的是( )
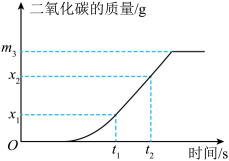 A、图中时刻,容器内氧气的质量为 B、图中时刻,容器内碳元素的质量为 C、若 , 则该可燃物一定含有碳、氧元素 D、若 , 则该可燃物一定含有碳、氢、氧元素
A、图中时刻,容器内氧气的质量为 B、图中时刻,容器内碳元素的质量为 C、若 , 则该可燃物一定含有碳、氧元素 D、若 , 则该可燃物一定含有碳、氢、氧元素 -
20、某同学绘制了物质的转化关系如图所示(图中“→”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去)。下列说法错误的是( )
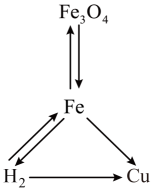 A、Fe能在空气中剧烈燃烧生成红色的 B、转化为Fe的反应可以是置换反应 C、可与CuO反应生成Cu,也可与反应生成Fe D、将Cu浸入溶液中可比较Fe和Cu的金属活动性
A、Fe能在空气中剧烈燃烧生成红色的 B、转化为Fe的反应可以是置换反应 C、可与CuO反应生成Cu,也可与反应生成Fe D、将Cu浸入溶液中可比较Fe和Cu的金属活动性