相关试卷
- 江苏省扬州市江都区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市高新区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省常州市2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市工业园区2017-2018学年九年级上学期化学12月调研考试试卷
- 江苏省扬州市江都区五校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省扬州市邗江区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省泰州市医药高新区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省常州市金坛区2017-2018学年九年级上学期化学期中质量调研考试试卷
- 江苏省扬州实验学校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省苏州市相城区2015-2016学年九年级化学一模考试试卷(4月)
-
1、 小柯同学进行如图1实验,其中Na2CO3溶液的质量与KCl溶液的质量相等,加入冰块后,观察到Na2CO3溶液析出的晶体比KCl溶液多,实验过程中溶质质分数的变化趋势如图2。下列说法不正确的是( )
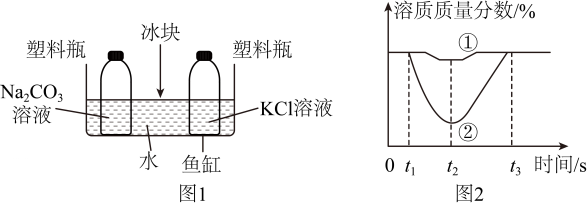 A、加入冰块前Na2CO3溶液和KCl溶液中的溶质质量一定相等 B、曲线①表示的是 KCl溶液 C、t2时Na2CO3溶液的质量小于 KCl溶液的质量 D、t3时、鱼缸中水的温度等于加入冰块前的温度
A、加入冰块前Na2CO3溶液和KCl溶液中的溶质质量一定相等 B、曲线①表示的是 KCl溶液 C、t2时Na2CO3溶液的质量小于 KCl溶液的质量 D、t3时、鱼缸中水的温度等于加入冰块前的温度 -
2、下列各项改变后的实验方案,仍能达到实验目的的是( )
实验目的
测定空气中氧气含量
验证分子在不断地运动
验证镁和铁的金属活动性序
除去氯化钠的溶液中混有的氧化镁
实验方案




选项
A.将红磷改为木炭
B.将浓氨水改为浓盐酸
C、将硫酸铝溶液改为硫酸锌溶液
D、将氢复化钠溶液改为氢氧化钙溶液
A、A B、B C、C D、D -
3、中国科学家研发出一种新型假化剂,能够将二氧化碳选择性的转化为一氧化碳,其反应的微观示意图如下所示。下列说法正确的是( )
 A、该反应属于置换反应 B、反应前后催化剂的质量和性质不变 C、参加反应的甲和乙的分子个数比为1:1 D、该方法有助于减少环污染
A、该反应属于置换反应 B、反应前后催化剂的质量和性质不变 C、参加反应的甲和乙的分子个数比为1:1 D、该方法有助于减少环污染 -
4、对下列事实或做法的解释不正确的是( )A、将铅笔芯连人闭合回路中,通电后灯泡发光——石墨具有导电性 B、验证羊毛大衣直伪时取样点燃——羊毛纤维和合成纤维燃烧的气味不同 C、适量食用海带、紫菜可以预防甲状腺肿大——海带、紫菜中富含碘元素 D、打开可乐瓶盖后可乐溢出——气体的溶解度随温度升高而减小
-
5、欲配制100g溶质质量分数为6%的NaCl液。下列相关操作正确的是( )A、取出NaCl
 B、称量NaCl
B、称量NaCl C、量取水
C、量取水 D、溶解NaCl
D、溶解NaCl
-
6、增强安全意识,提升安全素养。运输浓硫酸的车俩应张贴的警示标志是( )A、爆炸性物质
 B、腐蚀性物质
B、腐蚀性物质 C、毒性物质
C、毒性物质 D、易燃气体
D、易燃气体
-
7、化学符号具有独特的学科内涵。下列化学符号正确的是( )A、Na:钠原子 B、N:氮气 C、Zu+2:锌离子 D、AICl:氯化铝
-
8、肉夹馍是院西的特色美食。下列制作内夹模的部分过程中主要涉及化学变化的是( )A、加水和面 B、发醉面团 C、剃碎肉块 D、切慎夹肉
-
9、水是生命之源。下列“水”中只含两种元素的是( )A、冰糖水 B、矿泉水 C、泥沙水 D、蒸水
-
10、黄铜是铜锌合金,又称假黄金。立信中学化学兴趣小组同学做了如下实验:取黄铜,向其中加入稀盐酸恰好完全反应,待不再产生气体后称量剩余物质质量为(不包含容器质量),试计算:(1)、产生气体g;(2)、反应后溶液中溶质质量分数。
-
11、
金属及金属材料广泛应用于生产、生活及科学实验,其应用推动了社会的发展。

探究一:金属生锈的探究
立信中学化学兴趣小组设计了如图甲所示的数字化实验指导同学们对铁锈蚀进行探究。用铁粉和碳粉的均匀混合物模拟铁钉成分,用传感器测定试剂瓶内气体的相关数据。
可供选择的药品如下表:
组别
药品
铁粉/g
碳粉/g
水/滴
食盐/g
其他
一
5.0
0.1
0
0
干燥剂
二
a
0.1
10
0
无
三
5.0
0.1
10
1.0
无
四
5.0
0.1
0
1.0
无
(1)第二组中,a的值为。
(2)在A、B两个试剂瓶中依次加入第一组和第二组药品进行实验。
①内A瓶中含量几乎不变,B瓶中不断减少。
②将第二组药品中的水改为迅速冷却的沸水,且用量增多至足以完全浸没固体混合物。内B瓶中含量也略有减少,主要原因是。
(3)为探究食盐对钢铁锈蚀速率的影响,应选择的药品组别是。
(4)在两个试剂瓶中均加入第二组药品,分别用不同传感器测得装置内两种变化量如图乙所示,其中N表示湿度的百分含量。瓶内湿度随时间增大(即水蒸气含量增大)的根本原因是。
探究二:从X、银、铜、锌四种金属的混合物中分离某贵重金属(已知X在化合物中显价)。流程如下:

(5)气体Q的化学式为。
(6)四种金属的活动性顺序由强到弱是。
(7)滤液A中溶质成分为。
-
12、根据如图所示的实验装置回答问题。
 (1)、仪器①的名称为。(2)、实验室制取应选择的收集装置是(填序号,从中选取)。(3)、一种洗气装置如图G所示,为了检验一氧化碳中是否混有 , 气体应从(填“a”或“b”)端导管口通入。
(1)、仪器①的名称为。(2)、实验室制取应选择的收集装置是(填序号,从中选取)。(3)、一种洗气装置如图G所示,为了检验一氧化碳中是否混有 , 气体应从(填“a”或“b”)端导管口通入。 -
13、利用海水提取粗盐,提纯氯化钠的过程如图所示,回答有关问题:
 (1)、氯化钠在海水中的分散微粒是(填微粒符号);(2)、从储水池到蒸发池,氯化钠的质量分数填(“变大”“变小”或“不变”);(3)、根据海水晒盐的原理,下列说法中正确的是_____________(填相应的字母)。A、海水进入储水池,海水的成分基本不变 B、在蒸发池中,海水中水的质量逐渐增加 C、析出晶体后的母液是氯化钠的饱和溶液
(1)、氯化钠在海水中的分散微粒是(填微粒符号);(2)、从储水池到蒸发池,氯化钠的质量分数填(“变大”“变小”或“不变”);(3)、根据海水晒盐的原理,下列说法中正确的是_____________(填相应的字母)。A、海水进入储水池,海水的成分基本不变 B、在蒸发池中,海水中水的质量逐渐增加 C、析出晶体后的母液是氯化钠的饱和溶液 -
14、成语“百炼成钢”的化学含义是将反复烧红的生铁在空气中不断锤打,从而降低生铁中的的含量,转化为钢。请写出该过程中的化学方程式:。
-
15、湿法炼铜的原理是铁与溶液反应,请写出该反应的化学方程式 , 该反应的基本反应类型是反应。
-
16、认真阅读下列材料,回答有关问题。
“五金”是指金、银、铜、铁、锡五种金属。金、银是贵金属,古人常把金银用于货币、装饰及宗教仪式。三星堆遗址出土的黄金面具金光灿灿、十分夺目。铜是人类最早使用的金属之一。在我国古代铜的冶金史上,有一项重大的发明,就是湿法炼铜,即用铁锅熬胆水(硫酸铜溶液)炼铜,此法炼铜到宋朝时发展到顶峰。铁是最常见的金属之一,工业炼铁的原理是用还原的方法把铁从铁矿石中提炼出来,常见的铁矿石有赤铁矿(主要成分是氧化铁)、磁铁矿(主要成分是)。锡在自然界中主要以氧化物(如锡石,主要成分为)和硫化物(如黄锡矿,主要成分为)的形式存在,锡制成的锡箔常用于包装香烟、糖果等。
(1)、三星堆遗址中的黄金制品能保存完好且未被腐蚀,说明金的化学性质(填“活泼”或“不活泼”)。(2)、锡制成的锡箔常用于包装香烟、糖果等,是利用了金属的性。(3)、铁生锈的过程,实际上是铁与空气中的氧气和发生化学反应的过程。(4)、赤铁矿中的氧化铁用化学式表示为。 -
17、如图是a、b、c三种固体物质的溶解度曲线。下列说法正确的是
 A、将时c的饱和溶液升温到 , 其溶质质量分数不变 B、P点表示在时,a、c两物质溶解度相同 C、时,将的a加入到水中充分搅拌可得到的a的饱和溶液 D、时,分别将a、b、c的饱和溶液恒温蒸发相同质量的水,a析出固体的质量最大
A、将时c的饱和溶液升温到 , 其溶质质量分数不变 B、P点表示在时,a、c两物质溶解度相同 C、时,将的a加入到水中充分搅拌可得到的a的饱和溶液 D、时,分别将a、b、c的饱和溶液恒温蒸发相同质量的水,a析出固体的质量最大 -
18、向盛有和混合溶液的试管中加入一定量镁粉和银粉充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。下列说法正确的是A、滤渣中一定有铜和银,一定没有镁 B、滤渣中一定有银,一定没有镁和铜 C、滤液中一定含有和 , 可能含有 D、滤液中一定含有 , 可能含有和
-
19、下列除杂操作不能达到实验目的的是
选项
实验目的
实验操作
A
除去二氧化碳中的少量一氧化碳
将气体点燃
B
除去生石灰中的少量石灰石
加水后过滤
C
除去溶液中的
加入足量的铁粉,充分反应后过滤
D
除去铜粉中的铁粉
加入足量的稀盐酸,充分反应后过滤、洗涤、干燥
A、A B、B C、C D、D -
20、下列各组物质中,前者为化合物,后者为溶液的一组是A、氯化氢气体、稀盐酸 B、铁水、双氧水 C、铁矿石、乙醇 D、澄清的石灰水、干冰