-
1、根据下图回答问题。
 (1)、仪器a的名称是。(2)、加热制取氧气的化学方程式为。(3)、实验1,收集完氧气后的正确操作是_____(填序号)。A、熄灭酒精灯后,将导管移出水面 B、将导管移出水面后,熄灭酒精灯(4)、实验2,木炭在氧气中燃烧的现象是剧烈燃烧, , 放出热量。
(1)、仪器a的名称是。(2)、加热制取氧气的化学方程式为。(3)、实验1,收集完氧气后的正确操作是_____(填序号)。A、熄灭酒精灯后,将导管移出水面 B、将导管移出水面后,熄灭酒精灯(4)、实验2,木炭在氧气中燃烧的现象是剧烈燃烧, , 放出热量。 -
2、阅读下面科普短文。
过碳酸钠俗称固体双氧水,化学式为 , 常温为白色、无臭固体,遇高温、潮湿易分解。
制备:在时,将过氧化氢溶液、纯碱溶液和稳定剂充分混合,待反应结束后通过抽滤、洗涤、干燥得到过碳酸钠。过碳酸钠在潮湿环境中不稳定,研究人员通过实验比较了未添加稳定剂、添加氯化镁稳定剂、有机膦酸稳定剂对过碳酸钠稳定性的影响,其结果如图1.(湿度稳定性数值越大,湿度稳定性越强)

用途:很多除茶渍、咖啡渍的产品,其有效成分均为过碳酸钠,使用时将产品粉末倒入盛有温水的杯子中,迅速产生大量气泡,静止片刻后即可清除茶垢。其原理为过碳酸钠遇水生成碳酸钠和过氧化氢,过氧化氨分解的过程中产物深入微小的缝隙,使茶垢分解、脱落。过碳酸钠还可用于急救供氧、医疗杀菌消毒和纺织品洗涤漂白等方面。依据文章内容回答下列问题。
(1)、过碳酸钠的物理性质有(填一条即可)。(2)、过碳酸钠保存时需注意(填一条即可)。(3)、制备过碳酸钠过程中需使用过氧化氢溶液,过氧化氢()属于_____(填序号)。A、纯净物 B、混合物 C、氧化物(4)、判断下列说法是否正确(填“对”或“错”)。①除茶垢时使用温水,可能的原因是升温能加快过碳酸钠与水的反应。
②过碳酸钠可用作急数供氧剂,主要原因是其遇水产生的分解出氧气。
(5)、对比图1中的三条曲线,得出的结论是:在其他条件相同时,在0-48小时范围内,当放置时间相同时,。 -
3、一种甲醇汽车,可循环使用空气驱动。汽车行驶中物质的主要转化过程如下:
 (1)、甲醇(CH4O)中碳、氢元素的质量比为。(2)、Ⅰ中反应的化学方程式为。(3)、与传统燃油汽车相比,这种汽车的优点是(写出一点即可)。
(1)、甲醇(CH4O)中碳、氢元素的质量比为。(2)、Ⅰ中反应的化学方程式为。(3)、与传统燃油汽车相比,这种汽车的优点是(写出一点即可)。 -
4、水是生命之源。“生命吸管”(如图)可直接将污水净化为饮用水。
 (1)、“生命吸管”的塑料外壳在空气中完全燃烧后生成水和二氧化碳,则塑料中一定含有的元素为。(2)、活性炭的作用是。
(1)、“生命吸管”的塑料外壳在空气中完全燃烧后生成水和二氧化碳,则塑料中一定含有的元素为。(2)、活性炭的作用是。 -
5、我国提出2060年前实现碳中和,这对全球应对气候变化产生了积极影响。(1)、现阶段的能源仍以化石燃料为主,化石燃料包括煤、和天然气。(2)、碳中和是指通过一定途径实现“零排放”。下列燃料在中燃烧时,不会产生的是_____(填序号)。A、氢气() B、一氧化碳() C、氨()(3)、为应对能源短缺问题,人类正在开发和利用新能源,下列属于新能源的是_____(填序号)。A、太阳能 B、石油 C、风能
-
6、下面是生活中常见的食品保存方法。(1)、干冰保存冰激凌,利用了干冰的性质(填“物理”或“化学”)。(2)、膨化食品包装内充入氮气,是因为氮气的化学性质。(3)、熟食用真空包可减少食品保存环境中的含量,防止熟食变质。(4)、通常自热食品利用的是氧化钙与水发生化学反应,该反应过程中会(填“放出”或“吸收”)热量。
-
7、利用如图装置进行实验。下列说法不正确的是
 A、浓氨水有挥发性 B、滴有酚酞溶液的棉球变红 C、能证明分子在不断运动 D、能证明分子运动速率与温度有关
A、浓氨水有挥发性 B、滴有酚酞溶液的棉球变红 C、能证明分子在不断运动 D、能证明分子运动速率与温度有关 -
8、放射化学家杨承宗成功从含铀万分之几的轴矿石中制备核纯轴。铀在元素周期表中的信息如图,下列有关铀元素的说法正确的是
 A、原子序数为92 B、质子数为146 C、中子数为92 D、相对原子质量为
A、原子序数为92 B、质子数为146 C、中子数为92 D、相对原子质量为 -
9、下列反应属于化合反应的是A、H2SO4+2NaOH=Na2SO4+2H2O B、Mg+2HCl=MgCl2+H2 ↑ C、2KClO32KCl+ 3O2↑ D、CO2+C2CO
-
10、检验集气瓶中某无色气体是否为二氧化碳,常用的方法是A、观察颜色 B、闻气味 C、将带火星的木条放在集气瓶口 D、倒入澄清石灰水
-
11、下列关于和的说法中,正确的是A、组成元素相同 B、化学性质相同 C、构成分子相同 D、都是有毒气体
-
12、甲烷()是常见的温室气体。下列关于的说法不正确的是A、由两种元素组成 B、1个甲烷分子由5个原子构成 C、相对分子质量为 D、氢元素的质量分数计算式为
-
13、垃圾分类利国利民,香蕉皮属于A、厨余垃圾 B、可回收物 C、有害垃圾 D、其他垃圾
-
14、铁元素有、两种常见化合价,下列氧化铁(铁元素)的化学式书写正确的是A、 B、 C、 D、
-
15、下列安全图标中,表示“禁止吸烟”的是A、
 B、
B、 C、
C、 D、
D、
-
16、“发现青蒿素,开创疟疾治疗新方法”的科学家是A、道尔顿 B、拉瓦锡 C、侯德榜 D、屠呦呦
-
17、下列属于非金属元素的是A、H B、 C、 D、
-
18、某化学兴趣小组欲测定粗盐样品中氯化钠的质量分数(杂质为),进行如下实验。100g粗盐样品置于烧杯中,向其中加入一定量的水,使其完全溶解,将250g一定溶质质量分数的氢氧化钠溶液均分成5等份,依次加入上述溶液中,生成沉淀的质量与加入氢氧化钠溶液的质量关系如下
次数
第一次
第二次
第三次
第四次
第五次
氢氧化钠溶液质量/g
50
50
50
50
50
产生沉淀质量/g
1.45
2.9
m
5.8
5.8
(1)、m的值为;(2)、计算该粗盐样品中氯化钠的质量分数。(写出计算过程) -
19、
化学兴趣小组的同学在实验室发现一瓶久置的氢氧化钠固体,对其是否变质及变质程度展开探究。
【定性分析】
(1)为检测久置空气中氢氧化钠是否变质,设计并进行如下实验:

I.久置空气中的氢氧化钠固体变质的原因是(用化学方程式表示)
II.能达到实验目的的是试管中的实验(填1或2)。
【定量测定】为了测定ag变质氢氧化钠样品中氢氧化钠的质量分数,设计了如下的实验方案:
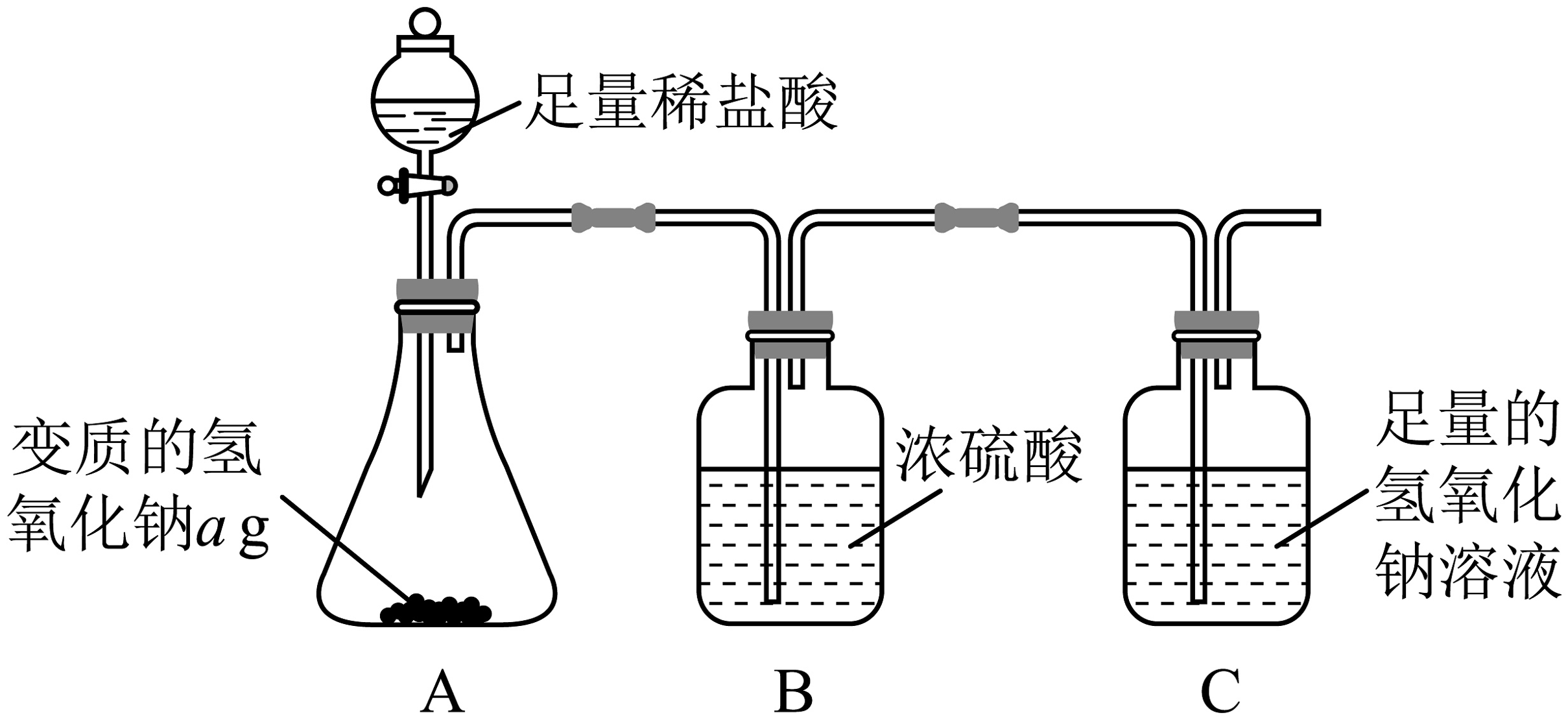
①组装装置,检查气密性良好;②加入药品,称量处装置质量为 , 滴入足量稀盐酸;③完全反应后称量处装置质量为;④后续处理。
【实验分析】
(2)I.判断变质的氢氧化钠中杂质已完全反应的实验现象;
II.B处装置中浓硫酸的作用是;
III.利用实验数据,变质氢氧化钠中氢氧化钠的质量分数为(用字母列式表达)。
-
20、下图是实验室制取气体的装置图,请回答下列问题:
 (1)、仪器a的名称是。(2)、实验室高锰酸钾制取较纯净的氧气,可选用的发生装置和收集装置是(填字母序号)。(3)、实验室制取二氧化碳的化学方程式为 , 若用装置收集二氧化碳,气体应从(填b或c)导管进。(4)、用如图所示装置,完成实验探究。其中、为干燥的紫色石蕊小花,o、p为湿润的紫色石蕊小花。可以说明的密度比空气大的实验现象为_____(填序号)。
(1)、仪器a的名称是。(2)、实验室高锰酸钾制取较纯净的氧气,可选用的发生装置和收集装置是(填字母序号)。(3)、实验室制取二氧化碳的化学方程式为 , 若用装置收集二氧化碳,气体应从(填b或c)导管进。(4)、用如图所示装置,完成实验探究。其中、为干燥的紫色石蕊小花,o、p为湿润的紫色石蕊小花。可以说明的密度比空气大的实验现象为_____(填序号)。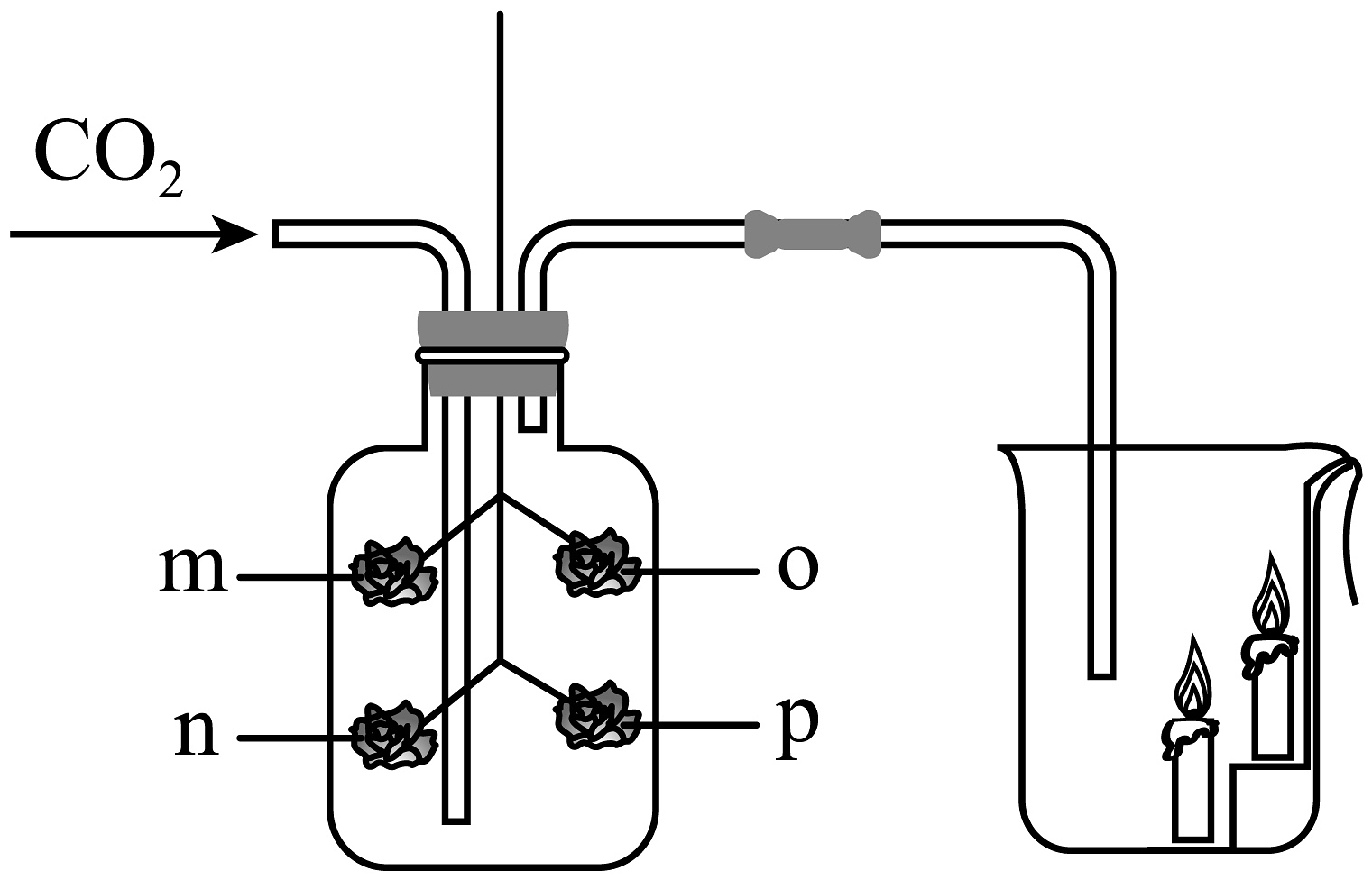 A、烧杯中蜡烛由低到高依次熄灭 B、p比o先变红
A、烧杯中蜡烛由低到高依次熄灭 B、p比o先变红