-
1、图示回答问题。
 (1)、图中仪器①的名称是;(2)、实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为;加热时试管口应略向下倾斜的原因是。(3)、实验室用B装置制取二氧化碳的优点:通常情况下,硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,密度比空气大,能溶于水,其水溶液叫氢硫酸(H2S).实验室用硫化亚铁固体与稀硫酸反应制取硫化氢气体时,应选择的发生装置为(填字母),若用D装置收集该气体,气体应从(填“a”或“b”)端通入。为了防止中毒和污染空气,多余的硫化氢气体可用氢氧化钠溶液吸收,其反应的化学方程式为(氢硫酸跟稀盐酸一样,能与碱发生中和反应)。
(1)、图中仪器①的名称是;(2)、实验室用氯酸钾和二氧化锰的固体混合物制取氧气,反应的化学方程式为;加热时试管口应略向下倾斜的原因是。(3)、实验室用B装置制取二氧化碳的优点:通常情况下,硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,密度比空气大,能溶于水,其水溶液叫氢硫酸(H2S).实验室用硫化亚铁固体与稀硫酸反应制取硫化氢气体时,应选择的发生装置为(填字母),若用D装置收集该气体,气体应从(填“a”或“b”)端通入。为了防止中毒和污染空气,多余的硫化氢气体可用氢氧化钠溶液吸收,其反应的化学方程式为(氢硫酸跟稀盐酸一样,能与碱发生中和反应)。 -
2、请结合下图实验回答有关问题:
 (1)、上图中操作a的名称是 , 该操作中所需的玻璃仪器有烧杯、玻璃棒和。(2)、上图中x的值为。(3)、检验上述实验中产生气体的方法是。(4)、计算参加反应的过氧化氢质量是多少?(写出计算过程)。
(1)、上图中操作a的名称是 , 该操作中所需的玻璃仪器有烧杯、玻璃棒和。(2)、上图中x的值为。(3)、检验上述实验中产生气体的方法是。(4)、计算参加反应的过氧化氢质量是多少?(写出计算过程)。 -
3、通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图所示:
 (1)、步骤①中玻璃棒的作用是 , 溶解粗盐时所加水的质量不宜过多,也不宜过少,过多会造成。(2)、第④步加入Na2CO3除去的杂质离子是 , 第⑥步操作的目的是除去滤液中的。(3)、第②步与第④步不能颠倒顺序,理由是。(4)、在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是。(5)、实验所得精盐质量粗盐中氯化钠质量(选填“大于”、“小于”或“等于”)。(6)、工业上用电解饱和食盐水的方法可制取氢氧化钠,同时还生成两种气体单质。写出此反应的化学方程式。
(1)、步骤①中玻璃棒的作用是 , 溶解粗盐时所加水的质量不宜过多,也不宜过少,过多会造成。(2)、第④步加入Na2CO3除去的杂质离子是 , 第⑥步操作的目的是除去滤液中的。(3)、第②步与第④步不能颠倒顺序,理由是。(4)、在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是。(5)、实验所得精盐质量粗盐中氯化钠质量(选填“大于”、“小于”或“等于”)。(6)、工业上用电解饱和食盐水的方法可制取氢氧化钠,同时还生成两种气体单质。写出此反应的化学方程式。 -
4、下列实验能达到实验目的是A、
 测定空气中氧气含量
B、
测定空气中氧气含量
B、 探究分子运动
C、
探究分子运动
C、 探究燃烧条件
D、
探究燃烧条件
D、 探究铁锈蚀条件
探究铁锈蚀条件
-
5、甲、乙两种物质的溶解度曲线如图所示,下列说法中不正确的是( )
 A、30℃时,125g甲的饱和溶液中有25g甲 B、升温能使乙物质的不饱和溶液变为饱和溶液 C、10℃时,乙物质的溶解度比甲物质的大 D、两种饱和溶液从30℃降到20℃时,甲乙物质的溶质质量分数相同
A、30℃时,125g甲的饱和溶液中有25g甲 B、升温能使乙物质的不饱和溶液变为饱和溶液 C、10℃时,乙物质的溶解度比甲物质的大 D、两种饱和溶液从30℃降到20℃时,甲乙物质的溶质质量分数相同 -
6、春耕时节,化肥是农作物生长的重要养料。某品牌化肥的包装袋上部分信息如图所示(化肥中杂质不含氮元素),下列说法错误的是
 A、该化肥属于氮肥 B、氯化铵中氮元素的化合价为-3价 C、该化肥的含氮量可能高达30% D、该化肥不能与熟石灰混合使用
A、该化肥属于氮肥 B、氯化铵中氮元素的化合价为-3价 C、该化肥的含氮量可能高达30% D、该化肥不能与熟石灰混合使用 -
7、如图是两个关于水的实验,有关说法正确的是
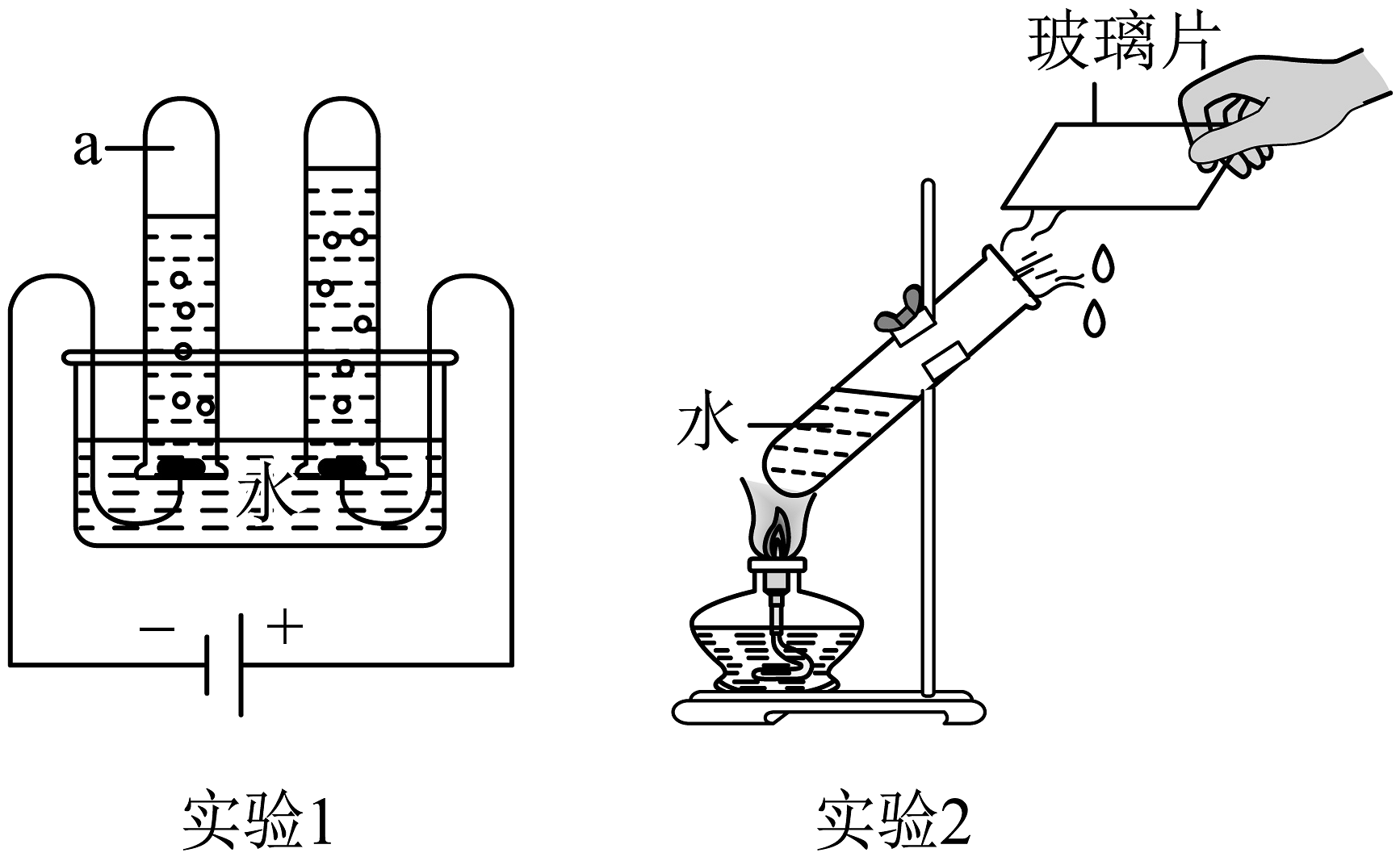 A、实验1,试管a中收集到的气体能够燃烧,产生淡蓝色火焰 B、实验2,水变化前后分子的种类和分子间间隔均不改变 C、实验1、2都遵守质量守恒定律 D、实验1、2均能验证水的组成
A、实验1,试管a中收集到的气体能够燃烧,产生淡蓝色火焰 B、实验2,水变化前后分子的种类和分子间间隔均不改变 C、实验1、2都遵守质量守恒定律 D、实验1、2均能验证水的组成 -
8、如图是“抗癌大王”——硒元素的有关信息,下列说法正确的是
 A、硒属于金属元素 B、硒的原子核内有34个质子 C、硒的相对原子质量是78.96g D、硒的原子结构示意图中x=4
A、硒属于金属元素 B、硒的原子核内有34个质子 C、硒的相对原子质量是78.96g D、硒的原子结构示意图中x=4 -
9、物质世界充满了变化。下列过程中,只发生了物理变化的是A、光合作用
 B、冰川融化
B、冰川融化 C、燃放烟花
C、燃放烟花 D、葡萄酿酒
D、葡萄酿酒
-
10、一种“贴身暖宝宝”的使用说明书如图,某化学兴趣小组围绕袋内物质展开探究。品名:XX牌贴身暖

【提出问题】袋内是否含有铁粉?
【进行实验】①取出袋内粉末于滤纸上,与磁铁充分接触。②将少量磁铁吸出的粉末加入足量稀硫酸中。
【收集证据】磁铁吸出的粉末与稀硫酸剧烈反应得到浅绿色溶液、同时。
【得出结论】袋内含有铁粉。
【做出猜想】被磁铁吸出的铁粉能在空气中燃烧。
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧、火星四射。
【反思交流】铁粉燃烧反应的化学方程式为。铁丝不能而铁粉能在空气中燃烧的原因是。
【拓展探究】用不同燃料测定空气里氧气的含量:分别在图甲所示装置的燃烧匙内放置铁粉、红磷(均足量),电加热引燃。氧气含量随时间变化情况如图乙、图丙:

(1)温度传感器显示,实验过程中瓶内温度均(填“升高”或“降低”)。
(2)待铁粉熄灭并恢复至室温后,打开弹簧夹,进入瓶内的水约占原水面上方空间体积的。
(3)分析图乙、图丙可知,实验中消耗氧气更彻底的是(填“铁粉”或“红磷”,下同),消耗氧气速率更快的是。
-
11、酸、碱、盐在工农业生产、生活中应用广泛。请回答相关问题:
(1)硫酸是一种重要的酸,在稀释浓硫酸时。盐酸、硫酸等酸具有相似的化学性质,是因为它们在水中都能够解离出酸根离子和H+ , 写出硫酸在水中解离的化学表达式。
(2)酸和碱的中和反应在实际中应用广泛。我市某校化学实验室废液呈酸性,应选用试剂(指示剂)检验该废液。若直接排放会导致环境污染,从经济可行的角度考虑,选用处理该废液。
(3)小苏打是焙制糕点所用的发酵粉的主要成分之一;在医疗上,它是治疗胃酸过多症的一种药剂, 请写出该反应的化学方程式。
(4)现有Ba(NO3)2溶液、稀硫酸、Na2CO3溶液、KOH溶液和CuSO4溶液。 请从下列选项中选择能够与上述物质发生复分解反应、并有沉淀生成的物质。
A稀盐酸 B烧碱溶液 C硝酸铵溶液
写出上述反应的化学方程式。
-
12、根据下列图示实验装置。回答有关问题。

(1)写出标有字母a的仪器名称。
(2)实验室用大理石制取CO2的反应原理(用化学方程式表示),选择(填字母)装置制取二氧化碳。
(3)从图E观察到的现象说明CO2具有性质是 , 写出检验CO2气体的方法(用化学方程式表示)。
(4)写出实验室选用A装置制取氧气的反应方程式 , 实验室要得到比较纯净的氧气通常选用(填字母)装置收集。
-
13、拥有丰厚绿色生态资源、多彩民族文化资源的贵州,正成为越来越多的国内外游客向往的心灵栖息之地。这些美不胜收的自然资源、人文资源中,蕴藏着无穷的化学奥秘。请回答下列问题。
(1)在生态理念深入人心的贵阳享美食。写出保护空气的一条措施。卤猪脚、酸汤、鱼和丝娃娃等美食中所含的营养素有(写一种)。
(2)丰富的水资源成就了黄果树大瀑布美丽的景观。请写出保护水资源的一条建议。“安顺蜡染”工序中的脱蜡,把染布放入沸水中,石蜡固体熔化为液体的过程属于 (填“化学”或“物理”)变化。
(3)游加榜梯田,在美丽乡村感受脱贫致富奔小康的巨变。农作物生长要合理施肥。硫酸钾(K2SO4)和氯化铵(NH4Cl)是常用的化肥,其中是钾肥,是氮肥。
-
14、化学与社会进步息息相关。(1)、2022年6月5日,搭载着“神舟十四号”载人飞船的“长征2F”运载火箭发射成功。液氢、液氧是常用的火箭推进剂,电解水可获得氢气和氧气,氢气在与直流电源极相连的电极上产生。氢能是未来最理想的能源,但目前应用并不广泛的原因是。(答一条即可)。(2)、“神舟十四号”轨道舱太阳能光伏发电板的主要材料是硅。单质硅由石英固体(SiO2)和单质碳在高温下反应制得,同时产生一种可燃性气体,该反应的化学方程式是。(3)、我国月球探测器“嫦娥五号”采回的月壤含CaAl2Si2O8 , 其中各种元素的质量比为。(4)、测体温用的额温枪内置的红外温度传感器所用材料含有钽酸锂(LiTaO3)。钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为价。在惰性气体氛围中制取钽的原理为:5Na+K2TaF7Ta+2KF+5R,则R的化学式为。
-
15、化学在能源、材料、医药、生命科学等领域有着其他学科所不能替代的重要作用,请根据要求填空∶(1)、在能源上,开发新能源缓解能源危机。请列举一种新能源。(2)、在生活上,洗涤剂能除去油污是利用了洗涤剂的作用。(3)、在工业上,焊接金属时常用氮气作保护气,是利用了氮气的。(4)、在农业上,可用与硫酸铜等配置农药波尔多液。(5)、在安全上,小丹妈妈在家炒菜时,油锅突然起火,将火扑灭。
-
16、食醋、KNO3、加碘食盐、尿素[CO (NH2)2]、棉花、干冰等是生活中常见物质,请用所学的化学知识选择上述物质完成下列问题:
(1)能有效预防大脖子病的是。
(2)能使石蕊溶液变红的是。
(3)属于天然高分子化合物的是。
(4)用于人工降雨的物质是。
(5)化肥对提高农作物的产量具有重要作用,属于复合肥料的是。
-
17、对“桂花十里飘香”的下列解释正确的是A、分子在不断运动 B、分子间有间隔 C、分子体积很小 D、分子质量很小
-
18、同学们用石灰石和过量稀盐酸制取二氧化碳,实验结束后,取反应后的溶液50.0g,滴加质量分数26.5%的Na2CO3溶液,溶液pH的变化如图所示。(已知CaCl2溶液呈中性)
 (1)、与CaCl2反应的碳酸钠溶液的质量为g。(2)、请计算该溶液中CaCl2的质量分数。(写出具体计算过程)
(1)、与CaCl2反应的碳酸钠溶液的质量为g。(2)、请计算该溶液中CaCl2的质量分数。(写出具体计算过程) -
19、
面包、蛋糕之所以松软是因为在制作过程中使用了膨松剂,已知某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,化学兴趣小组对该膨松剂进行如下探究:
查阅资料:①碳酸氢铵受热分解
②碳酸氢钠受热分解
③碱石灰(NaOH和CaO混合物)可用于干燥氨气。
④氨气能与硫酸反应。
【实验一】定性检验膨松剂成分:
【猜想】猜想一:;猜想二:;猜想三:、
在玻璃管中加入该膨松剂,按如图1所示连接好装置(铁架台略去,下同),点燃酒精灯:
 (1)关闭铁夹2,打开铁夹1,观察到澄清石灰水变浑浊,反应的化学方程式为 , 说明产物中有二氧化碳;打开铁夹2,关闭铁夹1,观察到的现象: , 说明产物中有氨气。(2)充分加热后,玻璃管中仍有固体。结论:猜想成立。
(1)关闭铁夹2,打开铁夹1,观察到澄清石灰水变浑浊,反应的化学方程式为 , 说明产物中有二氧化碳;打开铁夹2,关闭铁夹1,观察到的现象: , 说明产物中有氨气。(2)充分加热后,玻璃管中仍有固体。结论:猜想成立。【实验二】定量测定膨松剂受热产生气体的质量:
用如图2所示装置测定该膨松剂样品产生的二氧化碳气体的质量(整套装置气密性良好,各装置中气体吸收剂足量)。
 (3)测定二氧化碳的质量:将ag膨松剂装入装置B中,通过测定实验前后装置D的质量,其质量差即为样品产生的二氧化碳气体的质量。正确的操作顺序为(可以重复使用操作)。
(3)测定二氧化碳的质量:将ag膨松剂装入装置B中,通过测定实验前后装置D的质量,其质量差即为样品产生的二氧化碳气体的质量。正确的操作顺序为(可以重复使用操作)。①点燃酒精灯 ②熄灭酒精灯 ③通入一段时间空气 ④称量装置D的质量
(4)实验二中,装置E的目的是。(5)测定氨气的质量:另取ag膨松剂装入装置B中,将图2中装置C和装置D的连接顺序对调,(填“能”或“不能”)测定出样品产生的氨气的质量。(6)实验中测量得出生成的二氧化碳质量为8.8g,氨气质量为1.7g,则a值为。 -
20、如图是实验室制取与收集气体的装置图,请回答
 (1)、仪器①的名称是。(2)、若用氯酸钾制取较纯净的氧气,应选择的制取装置是 , 化学方程式是。(3)、实验室利用F装置收集H2时,气体应从(“a”或“b”)端通入。(4)、实验室常用大理石制CO2 , 某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥CO2 , 需对发生装置中产生的气体进行除杂,实验装置如图:
(1)、仪器①的名称是。(2)、若用氯酸钾制取较纯净的氧气,应选择的制取装置是 , 化学方程式是。(3)、实验室利用F装置收集H2时,气体应从(“a”或“b”)端通入。(4)、实验室常用大理石制CO2 , 某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥CO2 , 需对发生装置中产生的气体进行除杂,实验装置如图:
查阅资料:H2S能与NaOH等碱溶液、CuSO4溶液反应,其中,
①装置甲中所盛试剂应选用(填字母序号)。
A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液
②装置乙的作用是。
③装置丙中所盛药品是。