-
1、长沙作为美食之城吸引了大量游客。以下小吃和饮品的制作过程中涉及化学变化的是A、酱板鸭切块包装 B、奶茶中加冰块 C、豆腐发酵制作臭豆腐 D、甘蔗鲜榨成汁
-
2、下列生活垃圾属于可回收物的是A、瓜果皮 B、塑料瓶 C、餐巾纸 D、废电池
-
3、我国空间站长期有航天员入住,空间站中“人造空气”的成分和含量非常接近我们身边的空气,其中含量最多的气体是A、氢气 B、氧气 C、氮气 D、二氧化碳
-
4、化学兴趣小组为测定某小苏打样品(含杂质)中碳酸氢钠的含量,进行以下实验:称取样品,放入锥形瓶中,加水溶解。向该溶液中分两次加入稀盐酸,发生反应 , 锥形瓶及溶液质量变化如图所示(忽略在水中的溶解)。请计算:
 (1)、当第一次加入稀盐酸时,产生二氧化碳的质量是g。(2)、求样品中碳酸氢钠的质量分数。
(1)、当第一次加入稀盐酸时,产生二氧化碳的质量是g。(2)、求样品中碳酸氢钠的质量分数。 -
5、
化学学科致力于探索物质的组成与性质,并应用物质在不同条件下的变化规律。某兴趣小组对某品牌的食品脱氧剂的成分展开如下探究。
查阅资料:食品脱氧剂可以吸收食品包装内的氧气,“脱氧”一词由此而来;
食品脱氧剂的主要成分——铁粉、活性炭、食盐(其中食盐易溶于水)。
铁、钴、镍、四氧化三铁等物质有磁性
按下图所示进行探究实验(设步骤中所有过程都完全进行)

(1)①步骤Ⅰ中过滤时玻璃棒的作用是。
②固体C能被磁铁吸引,由此可知固体C为(填化学式)。
③小组同学进一步对气体E的成分进行探究。
【提出问题】步骤Ⅲ灼烧后生成的气体含有什么成分?
【猜想与假设】
(2)猜想一:;猜想二:CO和;猜想三:。
【实验探究】将气体E通入如图2的实验装置进行探究【现象与结论】
(3)装置A中澄清石灰水变浑浊,说明气体E中含有;该反应方程式为。装置B的作用是 , 右侧导管排出的气体可燃,说明猜想(填“一、二”或“三”)正确。
-
6、如图所示为实验室常用的实验装置,据图回答下列问题:
 (1)、仪器D的名称是。(2)、实验室制取的发生装置是(填字母序号),该反应方程式为。(3)、若实验室用高锰酸钾制取氧气,该装置需要改进地方是。(4)、装置C可以用来收集气体,还可以防倒吸。请你推测该气体的密度空气的密度(填“大于”或“小于”),该气体在水中的溶解性是(填“极易溶”或“难溶”)。
(1)、仪器D的名称是。(2)、实验室制取的发生装置是(填字母序号),该反应方程式为。(3)、若实验室用高锰酸钾制取氧气,该装置需要改进地方是。(4)、装置C可以用来收集气体,还可以防倒吸。请你推测该气体的密度空气的密度(填“大于”或“小于”),该气体在水中的溶解性是(填“极易溶”或“难溶”)。 -
7、电解水制氢联合碳酸钙分解制备氧化钙能减少碳排放,助力碳中和。该方法的示意图如图所示。
 (1)、大气中含量不断上升会加剧。(2)、反应器1中,与在一定条件下反应生成CaO、CO和 , 生成的CO与的分子个数比为。
(1)、大气中含量不断上升会加剧。(2)、反应器1中,与在一定条件下反应生成CaO、CO和 , 生成的CO与的分子个数比为。 -
8、阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与共熔后产生 , 才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对的选择性吸附性能越好。随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。

依据文章内容回答下列问题:
(1)、金刚石属于______(填序号)。A、无定形碳 B、过渡态碳 C、晶形碳(2)、石墨与共熔,能发生如下反应,配平该反应的化学方程式:+2+。(3)、由图2可知,我国碳纤维复合材料应用占比最高的领域是。(4)、对比图3中三条曲线,得到的实验结论是。 -
9、“从生活走进化学,从化学走向社会。”请用化学知识回答以下生活中的问题:(1)、含较多可溶性钙、镁化合物的水叫硬水,生活中通过的方法可以降低水的硬度;(2)、湿衣服在夏天比冬天干得快,其原因是;(3)、生活垃圾提倡分类处理。分类的目的是提高垃圾的资源价值和经济价值,力争物尽其用。下图所示标志属于塑料包装制品回收标志的是______。A、
 B、
B、 C、
C、 D、
D、
-
10、实验室用大理石和稀盐酸制备二氧化碳的发生装置如下图所示,下列说法正确的是
 A、打开旋塞之后,试管中稀盐酸体积减小 B、打开旋塞之后,有气体从长颈漏斗中逸出 C、闭合旋塞后,试管内气压减小 D、闭合旋塞后,漏斗内液面上升
A、打开旋塞之后,试管中稀盐酸体积减小 B、打开旋塞之后,有气体从长颈漏斗中逸出 C、闭合旋塞后,试管内气压减小 D、闭合旋塞后,漏斗内液面上升 -
11、用Pt-Rh合金催化氧化NH3制NO,其反应过程中含氮生成物的转化率随反应温度变化曲线如图所示,下列分析错误的是
 A、制备NO的适宜温度为800℃ B、400℃时,反应产物只有水和氮气 C、化学反应前后Pt-Rh合金的质量和化学性质均不变 D、温度超过800℃,NO的转化率呈逐渐下降的趋势
A、制备NO的适宜温度为800℃ B、400℃时,反应产物只有水和氮气 C、化学反应前后Pt-Rh合金的质量和化学性质均不变 D、温度超过800℃,NO的转化率呈逐渐下降的趋势 -
12、2024年诺贝尔化学奖授予美国生物化学家和英国人工智能科学家,以表彰他们在计算蛋白质设计和结构预测方面的贡献。氨基酸是构成蛋白质的基本结构单元,已知甘氨酸分子式为 , 下列关于甘氨酸的说法不正确的是A、相对分子质量为75 B、氢元素质量分数最小 C、C、H、N、O四种元素质量比为 D、甘氨酸是由2个碳原子、5个氢原子、1个氮原子和2个氧原子构成
-
13、构建化学基本观念是学好化学的基础,下列说法错误的是A、变化观:氢气在空气中燃烧生成水 B、微粒观:分子、原子和离子都可构成物质 C、守恒观:镁条在空气中燃烧前后质量对比,发现固体质量增加,不符合质量守恒定律 D、结构观:和电子层结构不同,化学性质不同
-
14、下列化学用语及名称表示不相符的是A、2个氯原子: B、铁离子: C、氧化铝: D、硫酸铵:
-
15、《千里江山图》是我国传世名画之一,宋代画家王希孟创造性地将炭黑、赭(主要成分为)、孔雀石[主要成分为]等矿物颜料用在不同的画层。其中中铜元素的化合价为A、 B、0 C、 D、
-
16、21世纪以来,化学研究和应用更加重视绿色、循环、低碳发展。以下做法符合“绿色、循环、低碳发展”要求的是A、将垃圾浇上油焚烧 B、开发风能、太阳能等新能源 C、将工业废水直接排入江河 D、治理污染点,深埋污染物
-
17、4g氢气完全燃烧生成水的质量为多少克?
-
18、请根据下列装置图,回答有关问题。
 (1)、写出图中仪器a的名称:;(2)、用A装置制取氧气,发生反应的化学方程式为;属于反应(填基本反应类型);若要收集一瓶纯净的氧气,则应选择的收集装置是(填字母);(3)、若用过氧化氢溶液制取氧气则反应的化学方程式为;(4)、实验室在常温下用块状电石与水反应制取微溶于水,密度比空气小的乙炔气体,该反应必须严格控制加水的速度,以免剧烈反应放热引起发生装置炸裂。上图中最适合制取乙炔的发生装置是(填字母);若用G装置收集乙炔气体,则气体应从(填“b”或“c”)端通入。
(1)、写出图中仪器a的名称:;(2)、用A装置制取氧气,发生反应的化学方程式为;属于反应(填基本反应类型);若要收集一瓶纯净的氧气,则应选择的收集装置是(填字母);(3)、若用过氧化氢溶液制取氧气则反应的化学方程式为;(4)、实验室在常温下用块状电石与水反应制取微溶于水,密度比空气小的乙炔气体,该反应必须严格控制加水的速度,以免剧烈反应放热引起发生装置炸裂。上图中最适合制取乙炔的发生装置是(填字母);若用G装置收集乙炔气体,则气体应从(填“b”或“c”)端通入。 -
19、下图为验证质量守恒定律的三个实验,请回答下列问题。
 (1)、实验一中观察到的实验现象是 , 该反应的化学方程式是(2)、实验二结束后天平指针会向(填“左”或“右”)偏转,原因是(3)、从原子的角度分析化学变化遵循质量守恒定律的原因是(4)、实验三在一根用细铜丝吊着的长玻璃棒两端分别绕上粗铜丝,并使玻璃棒保持水平。用酒精灯给a端粗铜丝加热数分钟,停止加热后冷却。观察到的现象是 , 发生反应的化学方程式为。(5)、某物质R完全燃烧需要12.8g氧气,可生成13.2g二氧化碳和5.4g水。则该物质的化学式为。
(1)、实验一中观察到的实验现象是 , 该反应的化学方程式是(2)、实验二结束后天平指针会向(填“左”或“右”)偏转,原因是(3)、从原子的角度分析化学变化遵循质量守恒定律的原因是(4)、实验三在一根用细铜丝吊着的长玻璃棒两端分别绕上粗铜丝,并使玻璃棒保持水平。用酒精灯给a端粗铜丝加热数分钟,停止加热后冷却。观察到的现象是 , 发生反应的化学方程式为。(5)、某物质R完全燃烧需要12.8g氧气,可生成13.2g二氧化碳和5.4g水。则该物质的化学式为。 -
20、如图为A、B、C、D四种粒子的结构示意图,E是硒元素在元素周期表中的信息,F是硒原子的结构示意图,请回答下列问题。
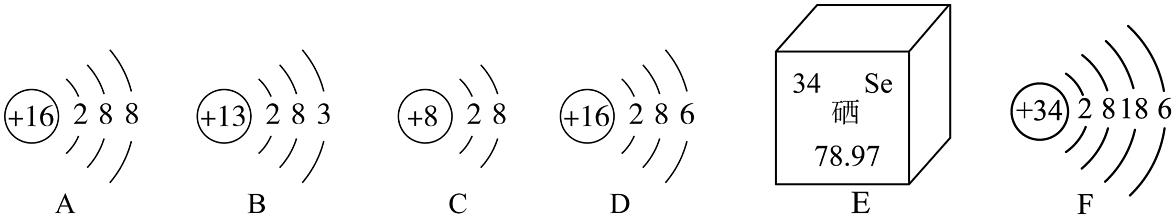 (1)、A、B、C、D四种粒子中,属于同种元素的是(填字母);C粒子的符号为;与C粒子结构相同的阳离子是。(2)、硒元素属于(“金属”或“非金属”)元素;D粒子与硒原子化学性质相似的原因。
(1)、A、B、C、D四种粒子中,属于同种元素的是(填字母);C粒子的符号为;与C粒子结构相同的阳离子是。(2)、硒元素属于(“金属”或“非金属”)元素;D粒子与硒原子化学性质相似的原因。