-
1、为了测定10.0g某石灰石(主要成分为碳酸钙)中碳酸钙的质量,某同学进行了如下实验:称取10.0g石灰石样品高温煅烧,石灰石在高温条件下可生成氧化钙和二氧化碳(杂质不参与反应),不同时间内实验数据记录如下表:
操作序号
1
2
3
4
剩余固体质量/g
8.6
7.3
6.7
6.7
请计算:
(1)、完全反应后生成的CO2质量是g。(2)、10.0g石灰石样品中碳酸钙的质量。 -
2、为测定某过氧化氢溶液中过氧化氢的质量,小新取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验。请计算:
 (1)、反应后产生气体的质量为g。(2)、参加反应的过氧化氢的质量。
(1)、反应后产生气体的质量为g。(2)、参加反应的过氧化氢的质量。 -
3、
保定博物馆内许多铜制展品表面有一层绿色物质。通过查阅资料得知,这是由于铜在空气中长时间生锈而生成铜绿的缘故,铜绿的化学式为Cu2(OH)2CO3。同学们对铜生锈的条件进行了如下探究活动。
【提出猜想】
(1)根据铜锈的组成推测,铜生锈是铜与、H2O和O2发生反应。
【进行实验】实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了下表所示的实验并持续观察。
序号
①
②
③
④
实验




现象
无明显现象
无明显现象
铜丝表面有绿色物质
无明显现象
【分析与解释】
(2)实验②中使用“煮沸并迅速冷却的蒸馏水”,其目的是。
(3)实验中③中现象最明显的位置是(选填“a”或“b”)。
(4)得出“铜生锈一定与O2有关”的结论,依据的两个实验是(填序号)。
(5)对比实验①和③,得出的结论是。
(6)为验证猜想,实验④广口瓶中除铜丝外,还应有的物质是。
【得出结论】由上述实验可推知,猜想正确。
【反思与应用】
(7)结合上述实验,你对保存铜制品的建议是。
-
4、实验室用如图所示装置制取二氧化碳,并研究二氧化碳的性质。
 (1)、装置A中长颈漏斗的下端插入液面以下的原因是。(2)、装置B观察到的实验现象是。(3)、若用装置C检验二氧化碳,则C中应加入的试剂为 , C中反应的化学方程式是。(4)、实验室制取CO2时,组装好仪器后,下列操作的正确顺序是。
(1)、装置A中长颈漏斗的下端插入液面以下的原因是。(2)、装置B观察到的实验现象是。(3)、若用装置C检验二氧化碳,则C中应加入的试剂为 , C中反应的化学方程式是。(4)、实验室制取CO2时,组装好仪器后,下列操作的正确顺序是。
①检查装置气密性
②收集气体并验满
③向长颈漏斗注入稀盐酸
④向锥形瓶加入石灰石
-
5、CaCl2•2H2O(二水合氯化钙)可用于食品加工、制药等领域。工业上生产(CaCl2•2H2O)的主要流程示意图如图所示。
 (1)、石灰石的主要成分是(填化学式)。(2)、反应器中发生的反应的化学方程式为。(3)、粉碎机中把石灰石进行粉碎、搅拌器进行搅拌的作用是。(4)、实验室进行过滤操作时,用到的玻璃仪器有烧杯、、。
(1)、石灰石的主要成分是(填化学式)。(2)、反应器中发生的反应的化学方程式为。(3)、粉碎机中把石灰石进行粉碎、搅拌器进行搅拌的作用是。(4)、实验室进行过滤操作时,用到的玻璃仪器有烧杯、、。 -
6、中科院团队在常温、常压和可见光条件下,基于LDH(一种固体催化剂)可合成氨气(NH3)。微观示意图如图:

请回答下列问题:
(1)、该反应前后种类和数目不变的是(选填“分子”或“原子”)。(2)、该反应的化学方程式为。(3)、该反应属于反应。(基本反应类型)(4)、催化剂在反应前后的和不变。(5)、由图可知,是保持物质化学性质的最小粒子。 -
7、填空:(1)、某同学想要量取27mL液体,读数视线如图所示。则量筒内液体的实际体积27mL(填“<”或“>”或“=”)。
 (2)、检查图1装置气密性的操作是 , 进行该操作时伸入水中的导管末端可能会出现如图2所示的现象。如果装置的气密性良好,很快会出现的是(填字母,下同),冷却后出现的是;如果装置的气密性不好,最有可能出现的是。
(2)、检查图1装置气密性的操作是 , 进行该操作时伸入水中的导管末端可能会出现如图2所示的现象。如果装置的气密性良好,很快会出现的是(填字母,下同),冷却后出现的是;如果装置的气密性不好,最有可能出现的是。
-
8、中华优秀传统文化中蕴含着许多化学知识。(1)、王安石在《梅花》中写下了“遥知不是雪,为有暗香来”的诗句,从微观的视角来看,“暗香来”的主要原因是分子很小且。(2)、早在距今约六千年的半坡文化时期,陶制品上便出现了彩绘。彩绘颜料种类多样,有红彩、黑彩和白彩等。白彩的主要成分为硫酸钙(CaSO4),其中硫元素的化合价为。(3)、《天工开物》中有我国古代炼铁的记载。炼铁的主要原理是一氧化碳与氧化铁反应,其化学方程式为。
-
9、2024年10月30日,神舟十九号载人飞船发射取得圆满成功。氢气作为一种高能燃料,已应用于航天、交通等领域。(1)、实验室可用锌与稀硫酸反应制取氢气,该反应的化学方程式为 , 收集方法和实验室收集(填“氧气”或“二氧化碳”)可相同。(2)、氢气作燃料的优点是。(答出一条即可)。(3)、航天员在空间站中呼吸所需的氧气部分来自循环水电解制氧系统。电解水反应生成的氧气和氢气的分子个数之比为。
-
10、如图为铁与硫酸铜溶液反应的实验。下列有关说法不正确的是
 A、铁丝上附着红色的铜 B、反应后溶液质量增加 C、金属活动性:Fe>Cu D、该反应为置换反应
A、铁丝上附着红色的铜 B、反应后溶液质量增加 C、金属活动性:Fe>Cu D、该反应为置换反应 -
11、荧光灯内的白色粉末涂层是一种叫钨酸钙(CaWO4)的化合物,下图为钨元素在元素周期表中的部分信息。下列分析正确的是
 A、钨原子中的核电荷数为74 B、钨原子中的中子数为74 C、一个钨原子的质量为183.8 D、CaWO4中非金属元素有两种
A、钨原子中的核电荷数为74 B、钨原子中的中子数为74 C、一个钨原子的质量为183.8 D、CaWO4中非金属元素有两种 -
12、规范的操作方法是实验安全和成功的重要保证。下列实验操作中正确的是A、加热液体
 B、量筒读数
B、量筒读数 C、闻药品气味
C、闻药品气味 D、取用固体药品
D、取用固体药品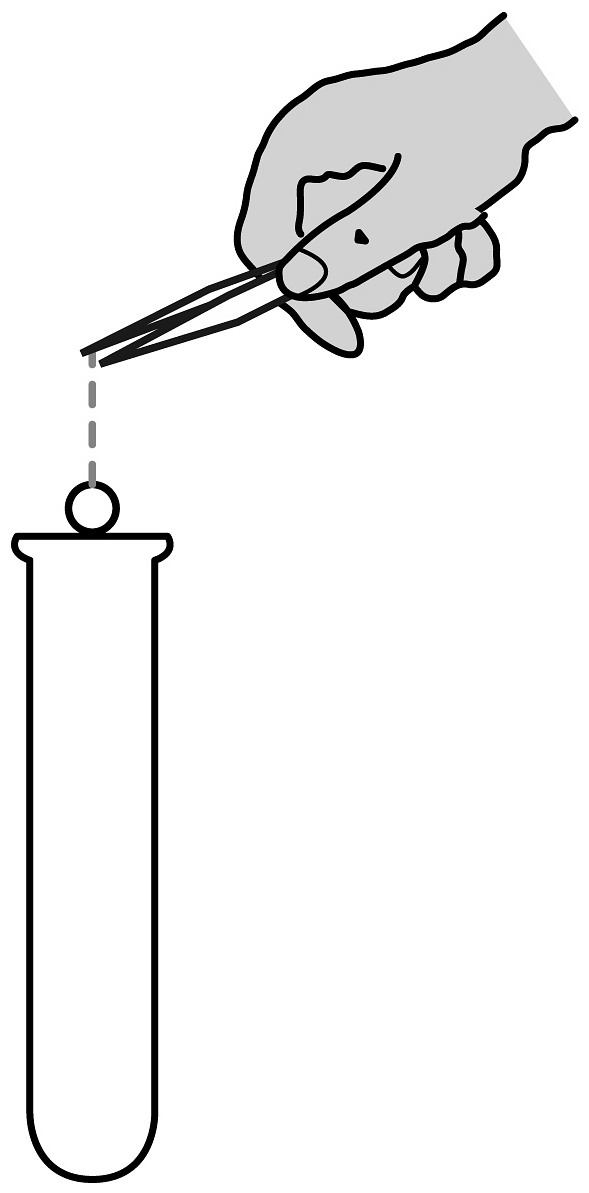
-
13、下列科学家与所作出的贡献对应错误的是A、拉瓦锡——原子论和分子学说 B、闵恩泽——石油化工生产的催化剂 C、徐寿——与他人合译《化学鉴原》 D、门捷列夫——元素周期表
-
14、党的二十大报告提出要“积极稳妥推进碳达峰碳中和”,落实双碳行动,共建美丽家园。下列做法与该理念不相符的是A、植树造林 B、大量使用化石燃料 C、乘坐公交出行 D、推广光伏发电
-
15、一种新型“人造树叶”可吸收二氧化碳并转化为乙醇(C2H5OH)燃料,化学方程式为2CO2+3H2O
 C2H5OH +3O2。研究显示,一升“人造树叶”每天可从空气中吸收968gCO2。
C2H5OH +3O2。研究显示,一升“人造树叶”每天可从空气中吸收968gCO2。(1)一升“人造树叶”工作一天可得到乙醇的质量是________?
(2)若每天一棵树平均可吸收48.4gCO2 , 则一升“人造树叶”吸收的CO2相当于_______棵树吸收的CO2。
-
16、下表是、在不同温度时的溶解度。
温度/℃
0
20
40
60
80
溶解度/g
35.7
36.0
36.6
37.3
38.4
29.4
37.2
45.8
55.2
65.6
(1)、以上两种物质的饱和溶液中,可用降低温度的方法得到晶体的是。(2)、40℃时将向盛有加入水中充分溶解,所得溶液的质量为。(3)、20℃时,的饱和溶液中溶质的质量分数约为。(保留一位小数) -
17、
燃烧不仅可以帮助人们创造美好生活,同时也促进了工业的发展和人类文明的进步。某项目小组的同学以“家用燃料”为主题开展了项目化学习的探究之旅。
【项目一】燃烧发生的条件

同学们设计了如图所示装置的探究实验。
已知:白磷的着火点为40℃,红磷的着火点为240℃,白磷的燃烧产物有毒。
(1)实验能得出可燃物燃烧需要的条件是。
(2)该装置进行实验的优点是。
【项目二】家用燃料的合理使用
(3)同学们经过走访调查,了解到家用燃料通常会将煤球制成蜂窝煤,请分析原因是。
(4)含碳燃料燃烧必须保持室内通风及烟囱通畅,否则会发生一氧化碳中毒,请用化学方程式解释生成一氧化碳的原因:。
【项目三】家用燃料的变迁
查阅资料
燃料
调控
主要成分
热值
煤
需提前点燃,过程复杂
碳、氢、硫、氮等元素
5500大卡/kg
煤气
随用随开
一氧化碳和氮气
3800-5700大卡
天然气
随用随开
甲烷
8000-90000大卡
【交流讨论】
(5)根据上表分析家用天然气代替其他燃料的原因是(至少写出两点)。
(6)写出天然气完全燃烧的化学方程式:。
【成果分享】通过研究家用燃料的更新历程,同学们预测未来燃料的发展方向是开发和利用清洁而又高效的能源。
-
18、根据下图的实验装置回答问题。
 (1)、仪器a的名称是。(2)、实验室制取发生装置B选择用分液漏斗添加液体,优点是。收集选用的装置是。(3)、用A装置制取 , 发生反应的化学方程式为 , 试管口略向下的原因是。(4)、已知:是一种黄绿色有刺激性气味的气体,密度比空气大,能溶于水,可使湿润的淀粉碘化钾试纸变蓝。实验室制取的反应原理: , 从上图中选择的发生装置是(填字母),若用D装置收集,验满的方法是将湿润的淀粉碘化钾试纸靠近管口(选填“b”或“c”),若试纸变蓝,则收集满。(5)、下列对制取、和这三种气体的分析中正确的是(填序号)。
(1)、仪器a的名称是。(2)、实验室制取发生装置B选择用分液漏斗添加液体,优点是。收集选用的装置是。(3)、用A装置制取 , 发生反应的化学方程式为 , 试管口略向下的原因是。(4)、已知:是一种黄绿色有刺激性气味的气体,密度比空气大,能溶于水,可使湿润的淀粉碘化钾试纸变蓝。实验室制取的反应原理: , 从上图中选择的发生装置是(填字母),若用D装置收集,验满的方法是将湿润的淀粉碘化钾试纸靠近管口(选填“b”或“c”),若试纸变蓝,则收集满。(5)、下列对制取、和这三种气体的分析中正确的是(填序号)。①制取和的发生装置相同
②和都不适宜用排水法收集气体
③制取和的反应中的作用是不同的
④和可用向上排空气法收集
-
19、人体缺乏维生素C会引起坏血病,下图是维生素C的说明书部分信息。计算:
某品牌维生素C(片剂)
化学式:
相对分子质量:176
规格:每片含维生素C
用法与用量:一日3次,成人每次2片……
(1)、维生素C的化学式为。(2)、维生素C中碳、氢、氧元素的质量比为(写最简比)。(3)、维生素C中碳元素的质量分数是(结果精确到)。(4)、若成人按说明书用量服用,则每日从该片剂中摄入的维生素C的质量为。 -
20、化学小组的同学们开展了以“生命之源——水”为主题的项目式学习。活动:参观直饮水机
 (1)、步骤①炭罐是用活性炭的性去除杂质。步骤③对应的作用是。(2)、可直接饮用的水(选填“是”或“不是”)纯水。
(1)、步骤①炭罐是用活性炭的性去除杂质。步骤③对应的作用是。(2)、可直接饮用的水(选填“是”或“不是”)纯水。