-
1、2024年4月25日,神舟十八号飞船成功发射。“天宫空间站”采用了众多先进科技,如形状记忆金属钛镍合金天线,由碳纤维和环氧树脂复合而成的防热夹层等。下列有关说法不正确的是A、天宫空间站钛镍合金天线属于合成材料 B、防热夹层的材料属于复合材料 C、宇航服的制作材料聚酯纤维薄膜是合成材料 D、空间站的外壳为钛合金,具有耐高温、强度高的特点
-
2、湖南物产丰富,下列食材或食品中富含蛋白质的是A、常德香米 B、炎陵黄桃 C、邵阳茶油 D、永州血鸭
-
3、下列关于金属和金属材料的说法中正确的是A、工业炼铁可用一氧化碳将铁的氧化物还原成铁 B、大多数金属在自然界中以单质形式存在 C、常温下,所有金属单质均有固体 D、废旧铁制品应该直接填埋处理
-
4、水是宝贵的自然资源。下列有关水的说法正确的是A、地球上的淡水资源取之不尽用之不竭 B、用活性炭吸附可除去水中的所有杂质 C、蒸馏法是净化程度较高的净水方法 D、生活污水和工业废水可随意排入河流
-
5、空气是人类生产活动的重要资源。下列关于空气的说法正确的是A、空气中含有氧气,因此空气可直接用于医疗急救 B、将氮气充入食品包装袋中可起到防腐作用 C、人呼吸空气时呼出的气体中只含有二氧化碳 D、倡导“低碳”生活有利于防治酸雨
-
6、《天工开物》记载了锡的冶炼方法:入砂(指锡砂)数百斤,丛架木炭亦数百斤,鼓鞲(指鼓入空气)熔化,用铅少许,(锡)沛然流注。其反应原理为。(1)、基本反应类型属于。(2)、现有含的锡砂,理论上可以炼出锡的质量是多少?(写出计算过程)
-
7、
同学们为提升化学实验操作技能,在实验室练习如下实验:

(1)实验时,小明观察到A试管中现象是;写出试管B中反应的化学方程式:。
实验完毕后,小明误将试管中的物质倒入试管中,充分振荡后,观察到混合后溶液为无色。小明对该无色溶液的成分产生兴趣并展开探究。
【提出问题】混合后无色溶液的溶质除酚酞外还有什么?
【查阅资料】溶液、溶液显中性。
【猜想与假设】猜想一:、;猜想二:、、;猜想三:、、;
(2)经分析猜想三错误,其理由是。
【设计并进行实验】
(3)为了验证其余猜想,小明进行了如下实验:
实验操作
实验现象
解释与结论
取少量混合后的无色溶液于试管中,加入锌粒
解释现象:(用化学方程式表示)得出实验结论:猜想二正确
【反思与拓展】
(4)I、有同学提议将上表操作中的锌粒换成另一种药品或用品:(除金属外),也可得出猜想二正确的实验结论。
II、小明误倒后,如果观察到试管底部有白色沉淀,上层清液为红色,则上层清液中一定有的阴离子是(填写离子符号)。
-
8、硫酸铁铵是一种重要的铁盐,常用作分析试剂。在实验室中采用废铁屑来制备硫酸铁铵晶体 , 具体流程如图所示:
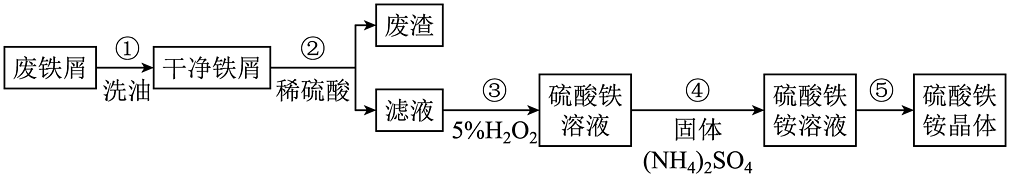
回答下列问题:
(1)、中铁元素的化合价为 , 与其类似的物质的名称为。(2)、步骤②中主要反应的化学方程式为。(3)、步骤③发生的反应是 , 为。(4)、硫酸铁铵的溶解度随温度的升高而增大且变化较大,步骤⑤可采用的操作是。(5)、下列三种物质中含氮量从高到低依次排列顺序为(用序号表示)。① ②(相对分子质量266) ③
-
9、“端午时节,粽叶飘香”。包粽子的主要食材包括糯米、瘦肉、植物油等。(1)、从分子的角度分析,“端午时节,粽叶飘香”的原因是;从营养角度考虑,除水、食盐等无机物外,上述食材未涉及的营养素是。(2)、食盐的主要成分是氯化钠,氯化钠以离子的形式分散在水中,其中带正电荷的离子是(填离子符号)。(3)、若煮粽子用的燃料是天然气,天然气的主要成分完全燃烧的化学方程式是。(4)、二氧化碳与水参与光合作用合成葡萄糖:。其能量转化形式是太阳能转化为能。此外,二氧化碳还能与水反应生成碳酸,同样是二氧化碳和水反应,产物却不相同,原因是。
-
10、当前,氨气()的能源化应用逐渐成为研究热点。工业上常用氮气和氢气合成氨气,一定条件下,在密闭容器中加入反应物和催化剂进行该反应,反应前后各物质的质量如图所示,图中有两处被墨迹遮盖。下列说法正确的是
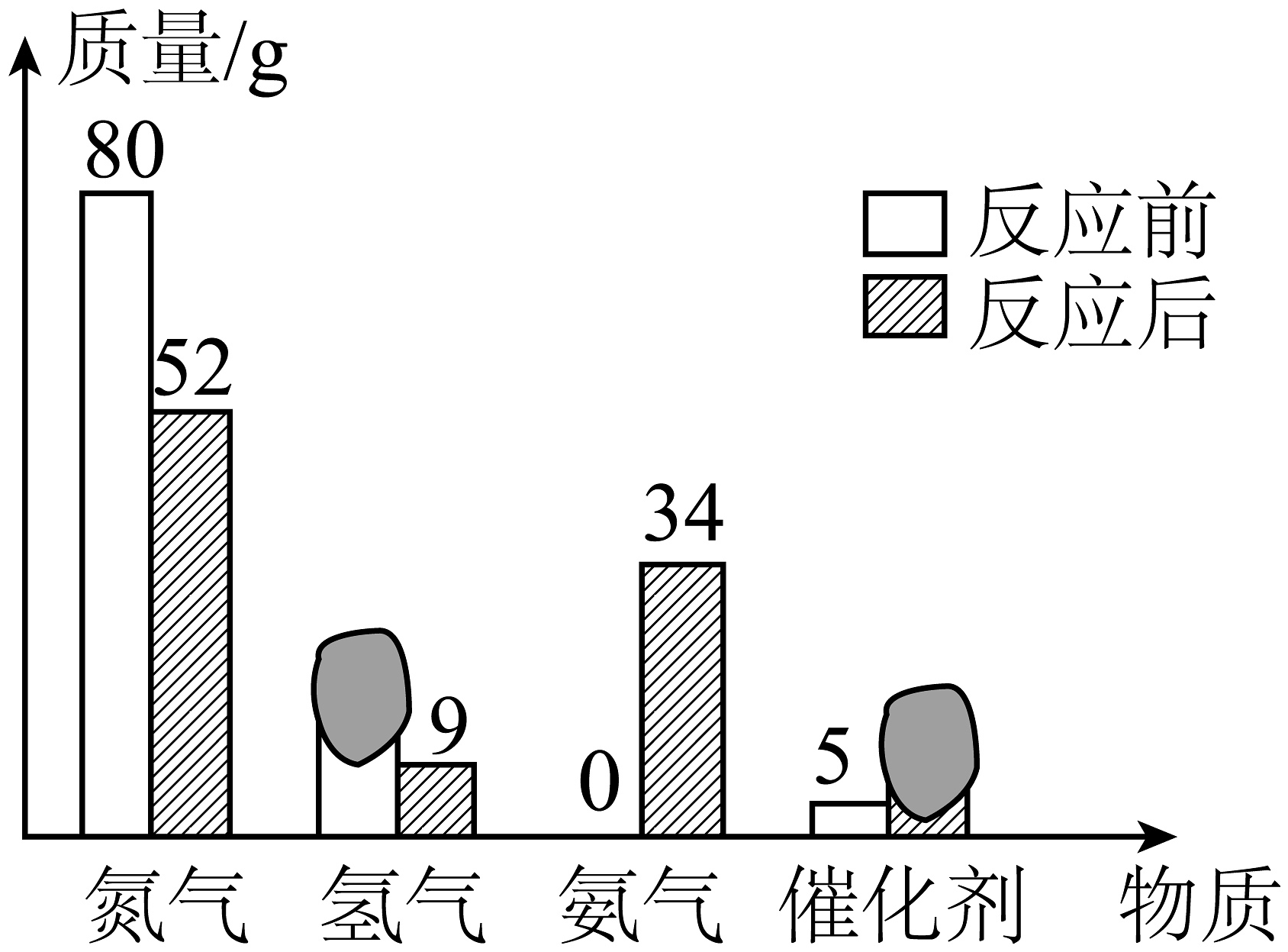 A、参加反应的氢气质量为6g B、反应后催化剂的质量为8g C、氨气分子的微观示意图为
A、参加反应的氢气质量为6g B、反应后催化剂的质量为8g C、氨气分子的微观示意图为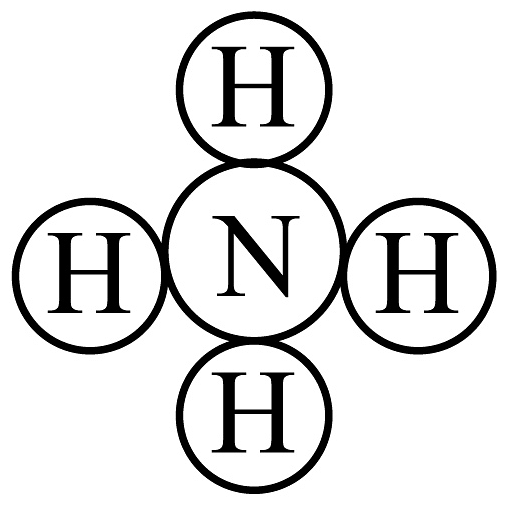 D、参加反应的氮气和生成的氨气分子个数比为4:1
D、参加反应的氮气和生成的氨气分子个数比为4:1
-
11、我国科研团队在二氧化碳合成乙醇方面取得了重大突破,其反应的微观过程如图。
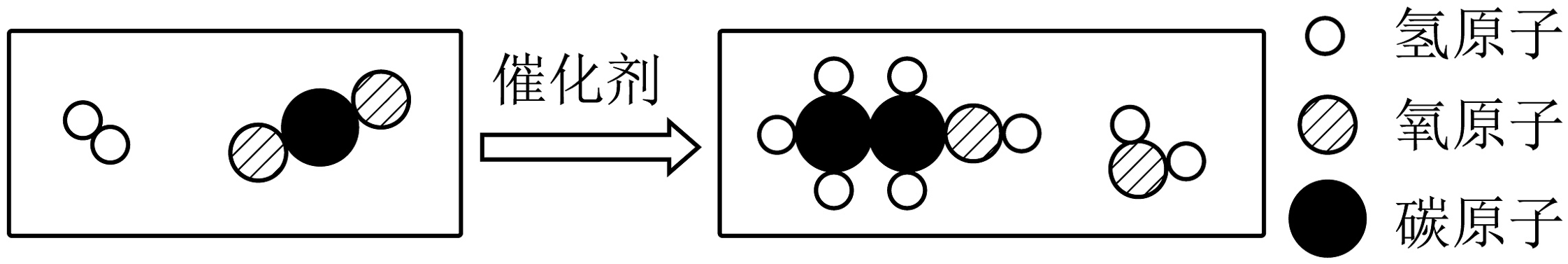
下列说法正确的是
A、此反应涉及3种氧化物 B、反应中原子种类发生改变 C、发生反应物质的分子个数比是1:1 D、该项研究有助于实现“碳中和” -
12、“清明插柳,端午插艾。”艾草含有丰富的黄酮素 , 它具有较高的药用价值。下列有关黄酮素的叙述正确的是A、该分子中含有 B、黄酮素完全燃烧生成和 C、黄酮素中氧元素质量分数最小 D、黄酮素中碳、氧元素的质量比为15:2
-
13、钛被称为“航空金属”,国产C919大飞机的钛合金用量达到9.3%。钛原子结构示意图及在元素周期表中的信息如图所示,下列有关钛说法不正确的是
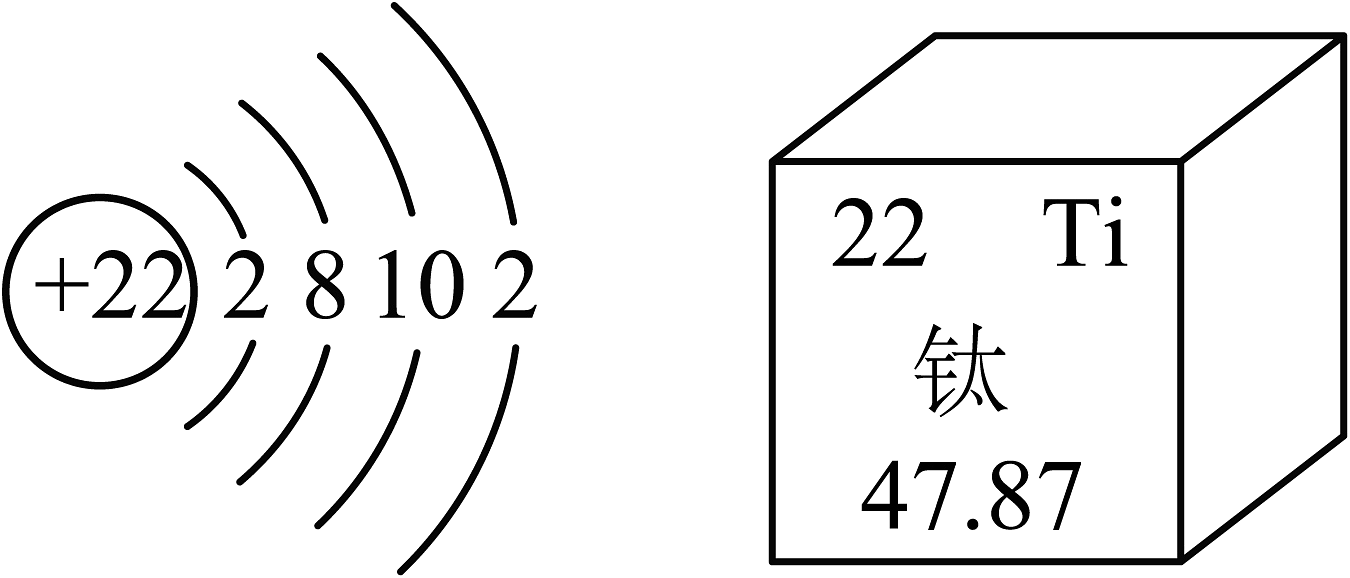 A、相对原子质量为47.87 B、原子核外电子数为22 C、钛原子位于第四周期 D、钛原子在化学变化中易得到2个电子
A、相对原子质量为47.87 B、原子核外电子数为22 C、钛原子位于第四周期 D、钛原子在化学变化中易得到2个电子 -
14、化学源于生活,应用于生活。下列描述错误的是A、二氧化碳过多会引起全球变暖 B、长期食用亚硝酸钠腌制的食品对健康有害 C、合金、合成纤维、合成橡胶都属于合成材料 D、打开汽水瓶盖时,由于压强减小,气体的溶解度变小,汽水会喷出
-
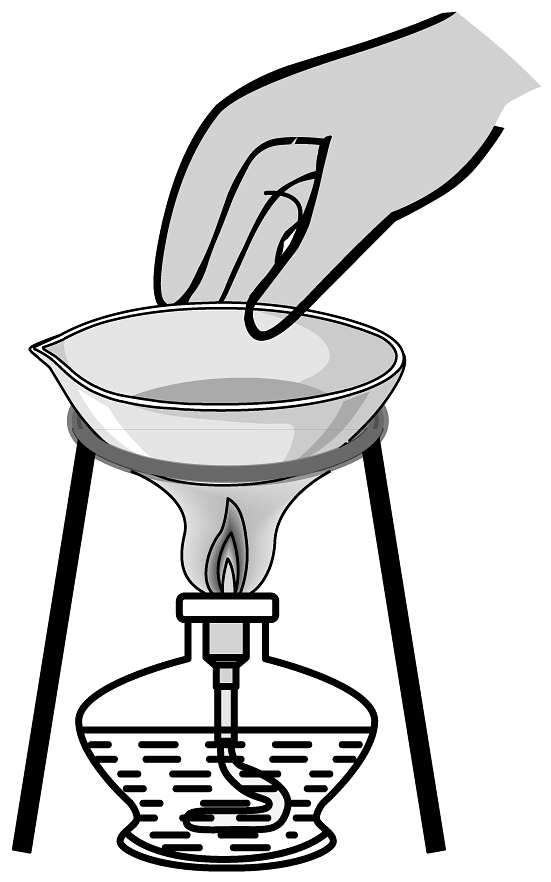
15、下列图示的实验操作正确的是A、移走蒸发皿
 B、读取液体体积
B、读取液体体积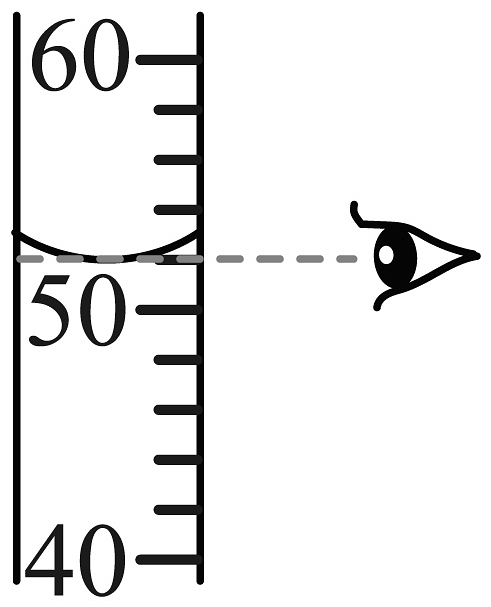 C、倾倒液体
C、倾倒液体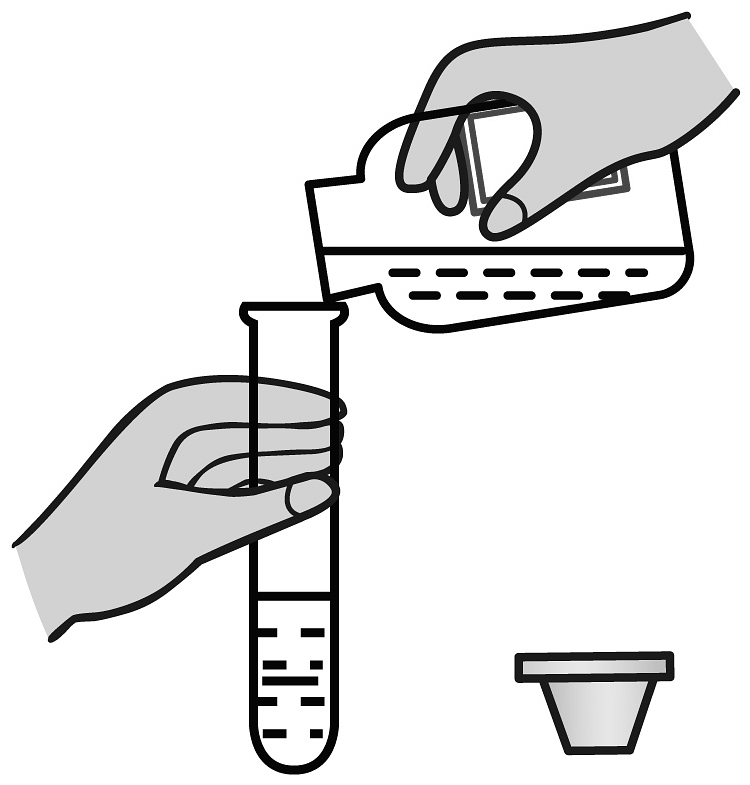 D、过滤
D、过滤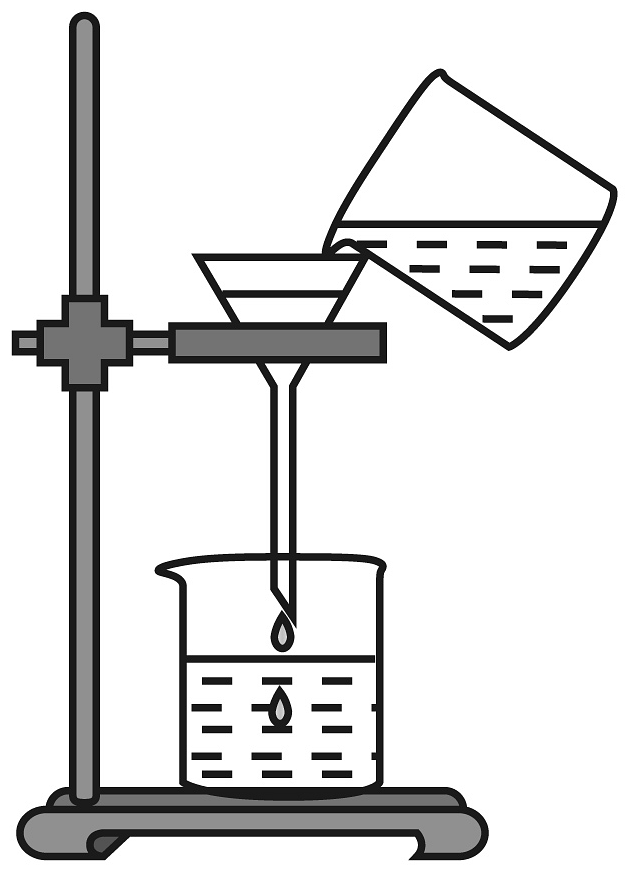
-
16、为打破国外技术封锁,潜心研究制碱技术,发明“联合制碱法”的科学家是A、闵恩泽 B、徐光宪 C、侯德榜 D、屠呦呦
-
17、《吕氏春秋》中记载“金(铜单质)柔锡(锡单质)柔,合两柔则刚”。这句话说明合金具有的特性是A、熔点一般比其组成金属的低 B、硬度一般比其组成金属的大 C、抗腐蚀性一般比其组成金属的强 D、耐磨性一般比其组成金属的好
-
18、根据下列粒子结构示意图,回答问题。
 (1)、A、B、C、E所示粒子中属于阳离子的是(填序号),若D为离子,其化学符号为。(2)、C所示粒子在化学反应中容易(填“得到”或“失去”)电子形成离子。(3)、A、B、C、E中具有相对稳定结构的粒子是(填序号)。(4)、由E粒子的结构示意图可知,E粒子的符号是。
(1)、A、B、C、E所示粒子中属于阳离子的是(填序号),若D为离子,其化学符号为。(2)、C所示粒子在化学反应中容易(填“得到”或“失去”)电子形成离子。(3)、A、B、C、E中具有相对稳定结构的粒子是(填序号)。(4)、由E粒子的结构示意图可知,E粒子的符号是。 -
19、
实验小组在跨学科实践活动中探究了水培生菜的最佳生长条件。
【查阅资料】
水培营养液原液的配制:将和固体溶于水形成原液,原液呈酸性。
【进行实验】
选择生长周期相同、长势相似的生菜苗,在相同光照和温度条件下,使用一定浓度和的水培营养液进行培养,定期更换营养液,观察生长情况。
实验一:稀释原液,得到一定浓度的水培营养液。实验记录如下表。
序号
水培营养液浓度
培养18天,生菜生长情况
①
1:200
叶片边缘焦黄,发蔫;根须较稀疏
②
1:500
叶片发绿,挺立;根须发达
③
1:800
叶片发黄,颜色淡,发蔫;根须稀疏
实验二:调节稀释后营养液的。实验记录如下表。
序号
水培营养液浓度
pH
培养18天,生菜生长情况
④
1:500
4
枯死
⑤
1:500
6
叶片发绿,多而舒展
⑥
1:500
8
叶片较多,发黄,稍发蔫
⑦
1:500
10
叶片较多,发黄,发蔫
【解释与结论】
(1)下列配制营养液原液的三种固体中,属于氮肥的是_______(填序号,下同)。A. B. C. (2)实验二中,欲使酸性的水培营养液呈碱性,应加入的物质是_______。A. 稀硫酸 B. 氢氧化钠溶液 C. 水 (3)由实验一和实验二得出:水培生菜的最佳生长条件是________。【反思与评价】
(4)除上述实验研究的因素外,水培生菜的生长会受到其他因素的影响。请你提出一种猜想,并设计实验方案:________。 -
20、完成实验报告。
实验
1
2
3
目的
配制质量分数为的溶液
验证钛、铜两种金属的活动性顺序
验证的性质
操作



现象
白色固体全部溶解
钛片上有红色固体产生
A中溶液变浑浊;B中紫色溶液变红
(1)、实验1,加入的质量为。(2)、由实验2可知,钛、铜两种金属活动性由强到弱的顺序为。(3)、实验3,中发生反应的化学方程式为。中的现象不能证明能与水反应,理由是。