-
1、用分子、原子的相关知识加以解释,其中不正确的是
现象或事实
解释
A
闻到花香
主要是分子不断运动的结果
B
物质热胀冷缩
分子原子的体积随温度改变而改变
C
氧气和臭氧()化学性质不相同
构成物质的分子不同
D
水通电分解生成氢气和氧气
在化学变化中分子可以再分
A、A B、B C、C D、D -
2、某校907班沈妮同学收集的××药品说明书上这样写道:本品每片主要成分及含量为: Ca 40mg、P 31mg、K 7.5mg、Mg 100mg、Cl 7.5mg、Fe 27mg。这里的成分及含量是指 ( )A、原子 B、离子 C、分子 D、元素
-
3、
水是生命之源,人类从未停止对水的研究。某化学兴趣小组以“生命之源___________水”为主题开展项目式探究。
Ⅰ.认识水的净化
(1)如图1所示自来水厂净水过程示意图中,主要经过沉淀、过滤、________、消毒等步骤除去杂质。输送到用户的自来水是________(选填“混合物”或“纯净物”)。

(2)如图2自制净水器,从上至下,放置下列三种物质的正确顺序是________(填字母代号)。
a.石英砂 b.活性炭 c.小卵石

Ⅱ.探究水的组成
(3)利用图3装置进行电解水实验,实验中所用电源是________(填“交流电”或“直流电”),a极产生的气体是________(填化学式)。

(4)某化学兴趣小组的同学在老师指导下,利用如图4装置探究铁与水蒸气的反应。

①装好药品、连好装置(夹持仪器已略去)。其中装置A对装置B中反应的作用是________。
②加热一段时间后,装置B中固体仍为黑色,吹泡器连续吹出气泡,且气泡向上飞起,用燃着的木条靠近气泡,能产生爆鸣声,说明该气体的性质有________。
③铁与水蒸气在高温时发生反应,生成上述气体与一种黑色固体(四氧化三铁),该反应的化学符号表达式为________。
(5)根据电解水的实验和氢气燃烧产物的确定,能够得出水的组成是________。
Ⅲ.水的应用
(6)为实现节能环保,我国大力推进新能源汽车。已知2kg氢气大约可供某款氢能源汽车行驶200km。若用电解水的方法制取氢气(生成氢气的质量等于电解的水中氢元素的质量),至少需要电解多少千克的水才能得到2kg氢气?(写出计算过程)
-
4、从微观的角度认识生活中的变化与现象是化学学科的特有思维方式。(1)、如图-1所示,用甲、乙两支大小相同的注射器,分别吸取等体积的空气和水,用手指顶住注射器末端的小孔,用相同大小的力,将栓塞慢慢推入。
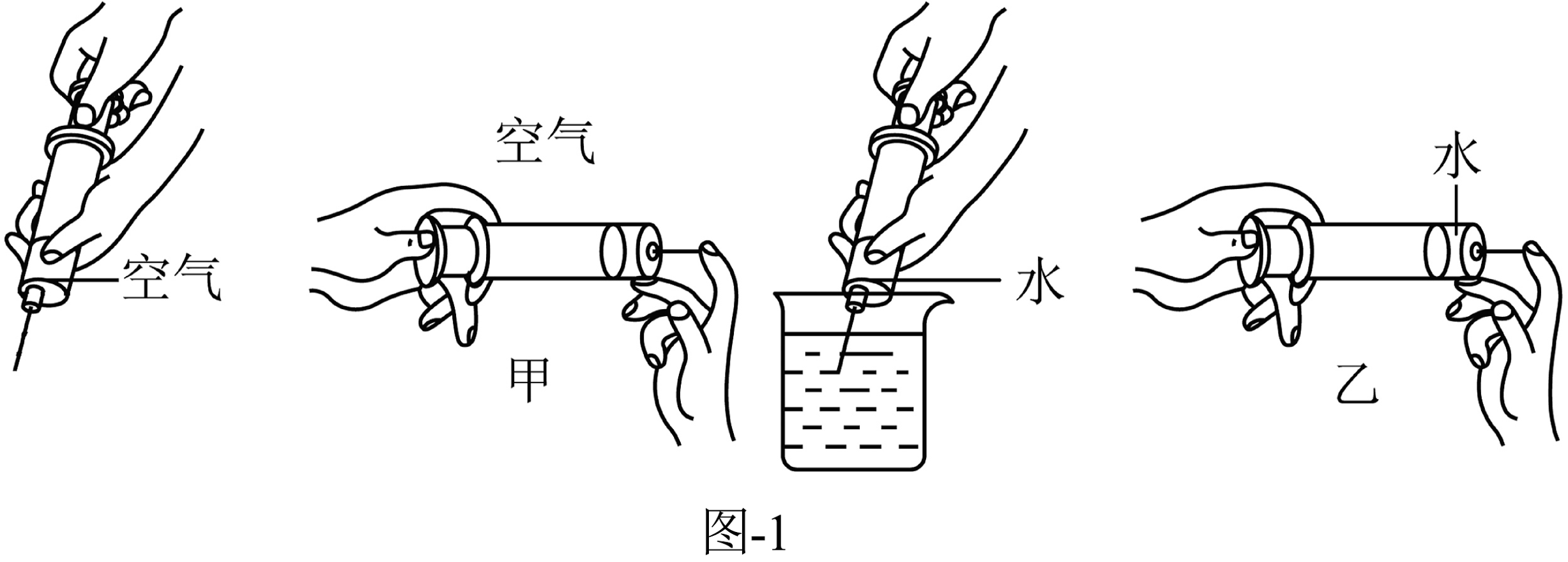
①容易被压缩的注射器是(填“甲”或“乙”)。
②通过对比两个实验,可以得出:在相同条件下,空气中的微粒间空隙比水的(填“大”或“小”)。
(2)、如图-2所示是氢分子和氧分子运动的示意图。
①根据图B和图C中所示的信息,你能得出的结论是 ,
②从图中可见,影响分子运动速率的因素除温度外,还与有关。
③图-3“水蒸气液化”,图-4“氢气在氯气中燃烧”的微观变化示意图。“○”表示氢原子,“●”表示氧原子,“
 ”表示氯原子。回答下列问题:
”表示氯原子。回答下列问题: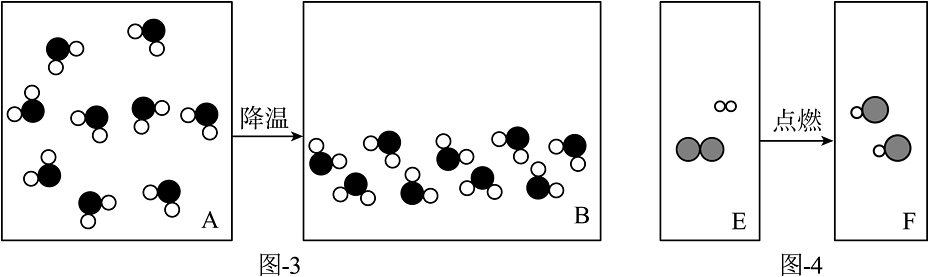
a.图-3所示的过程是变化,从微观角度解释图-3变化的本质是。
b.由图-4可得到:F的用化学式为 , 用语言描述该变化的过程。
-
5、实验室常用下列装置制取、收集氧气,并验证氧气的一些化学性质。请你按要求回答下列问题:
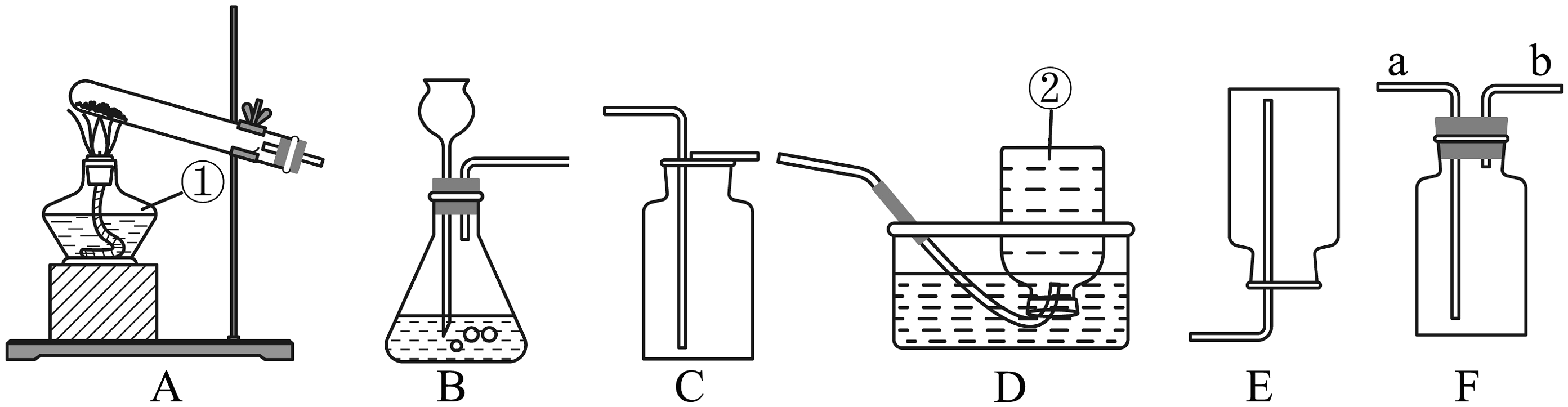
 (1)、指出图中标有数字的仪器名称:①;②;(2)、实验室用过氧化氢溶液和二氧化锰制取氧气时应选用装置(填字母标号,下同)为发生装置,写出该反应的符号表达式:;若要收集一瓶氧气做细铁丝在氧气中燃烧的实验,最好选用装置来收集氧气。(3)、实验室用高锰酸钾制取氧气,其反应的文字表达式为;若发生装置选择A,还需改进的地方是;在上述收集气体的装置中,不能用于收集氧气的是(填字母)。(4)、F是一种可用于集气、洗气等的多功能装置。若将F装置内装满水,再连接量筒,就可以用于测定收集到的氧气体积,则氧气应从(填“a”或“b”)进入F中。(5)、将收集的氧气倒入装置G的烧杯中,观察到带火星的木条自下而上依次复燃,说明氧气具有的性质是(填一条即可)。
(1)、指出图中标有数字的仪器名称:①;②;(2)、实验室用过氧化氢溶液和二氧化锰制取氧气时应选用装置(填字母标号,下同)为发生装置,写出该反应的符号表达式:;若要收集一瓶氧气做细铁丝在氧气中燃烧的实验,最好选用装置来收集氧气。(3)、实验室用高锰酸钾制取氧气,其反应的文字表达式为;若发生装置选择A,还需改进的地方是;在上述收集气体的装置中,不能用于收集氧气的是(填字母)。(4)、F是一种可用于集气、洗气等的多功能装置。若将F装置内装满水,再连接量筒,就可以用于测定收集到的氧气体积,则氧气应从(填“a”或“b”)进入F中。(5)、将收集的氧气倒入装置G的烧杯中,观察到带火星的木条自下而上依次复燃,说明氧气具有的性质是(填一条即可)。 -
6、化学用语是我们学习化学的重要工具。请用化学用语填空:(1)、保持水的化学性质的最小微粒。(2)、氯化钠是由离子构成的,写出其阳离子的离子符号。(3)、北京冬奥会上提供经过二氧化氯消毒处理的直饮水。二氧化氯的化学式为。(4)、中国嫦娥四号月球探测器首次证实构成月幔的主要物质之一是。已知中硅元素的化合价为+4,则其中铁元素的化合价为价。(5)、我国神舟号载人飞船座舱通过专用风机将座舲空气引入净化罐,利用氢氧化锶吸收二氧化碳,生成碳酸锂和水,净化后的空气再重新流回舱内。锂(Li)在化合物中的化合价为+1,利用氢氧化锂吸收二氧化碳反应的化学符号表达式为。
-
7、利用下图1装置研究过氧化氢的反应,所得结果如下图2所示,下列说法不正确的是
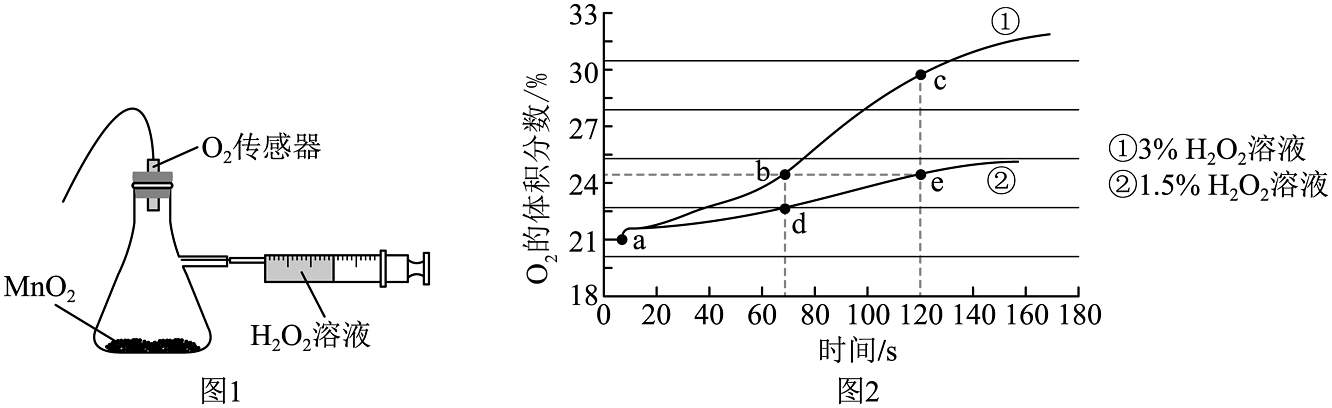 A、图2中的a点对应的操作是推动注射器活塞 B、对比c点利e点可以验证反应速率与过氧化氢溶液的浓度有关 C、对比b点和e点不能验证反应速率与过氧化氢溶液的浓度有关 D、该实验不能证明二氧化锰对过氧化氢的分解起催化作用
A、图2中的a点对应的操作是推动注射器活塞 B、对比c点利e点可以验证反应速率与过氧化氢溶液的浓度有关 C、对比b点和e点不能验证反应速率与过氧化氢溶液的浓度有关 D、该实验不能证明二氧化锰对过氧化氢的分解起催化作用 -
8、氮气与氢气反应生成氨气的过程叫作合成氨,该反应对氮肥生产具有重要意义。下图是氮气和氢气在催化剂表面合成氨气过程的微观示意图(“○”表示氢原子,“
 ”表示氮原子),正确的顺序是
”表示氮原子),正确的顺序是 A、④②③①⑤ B、⑤①③②④ C、②④③⑤① D、③⑤①④②
A、④②③①⑤ B、⑤①③②④ C、②④③⑤① D、③⑤①④② -
9、下列实验操作中不能达到实验目的的是
选项
目的
主要实验操作
A
鉴别氧气和氮气
伸入燃着的小木条,观察现象
B
除去固体中的NaCl
加水溶解,过滤,洗涤,干燥
C
区分蒸馏水和过氧化氢溶液
加入二氧化锰粉末,观察现象
D
自来水的杀菌消毒
加入活性炭,充分振荡,静置
A、A B、B C、C D、D -
10、中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我国在该领域的研究处于世界前列。氘和氚是核聚变的原料(氘原子核内有1个质子和1个中子,氚原子核内有1个质子和2个中子),聚变发生后,氘、氚原子核转变为氦原子核。根据以上叙述,下列说法正确的是A、氘原子和氚原子统称为氢元素 B、氘原子和氚原子的相对原子质量相同 C、氘原子和氚原子是不同元素的原子 D、氘、氚原子核转变为氦原子核的变化是化学变化
-
11、下列关于物质用途与性质不具有对应关系的事A、金属铁可以用于制作炊具——铁具有导电性 B、食品包装中充氮气防腐——氮气的化学性质不活泼 C、稀有气体可用于制作霓虹灯——通电时能发出不同颜色的光 D、氦气可用于填充探空气球——氦气的密度比空气的密度小
-
12、中国科学家成功以二氧化碳和水为原料人工合成葡萄糖。下列说法不正确的是A、葡萄糖的相对分子质量为180 B、葡萄糖中C、H、O元素的质量比为 C、300克葡萄糖中含有氧元素的质量为75克 D、1个葡萄糖分子中含有6个C原子、12个H原子和6个O原子
-
13、下图为几种粒子的结构示意图,有关说法正确的是
 A、以上四种粒子属于四种元素 B、②④形成的化合物化学式是MgF C、①③是原子,②④都是阳离子 D、③④对应的元素位于同一周期
A、以上四种粒子属于四种元素 B、②④形成的化合物化学式是MgF C、①③是原子,②④都是阳离子 D、③④对应的元素位于同一周期 -
14、朱砂又名辰砂,是天然的硫化汞(HgS),具有鲜红色泽,很早就被人们作为颜料使用。我国殷墟出土的甲骨文上涂有朱砂。下图所示是硫和汞在元素周期表中的信息。下列说法正确的是
16 S
硫
32.07
80 Hg
汞
200.59
A、汞和硫都是非金属元素 B、硫化汞(HgS)属于氧化物 C、硫原子和汞原子的本质区别是质子数不同 D、质量相等的汞和硫,汞比硫所含的原子数目多 -
15、规范操作是实验成功的保证。下列实验操作正确的是A、
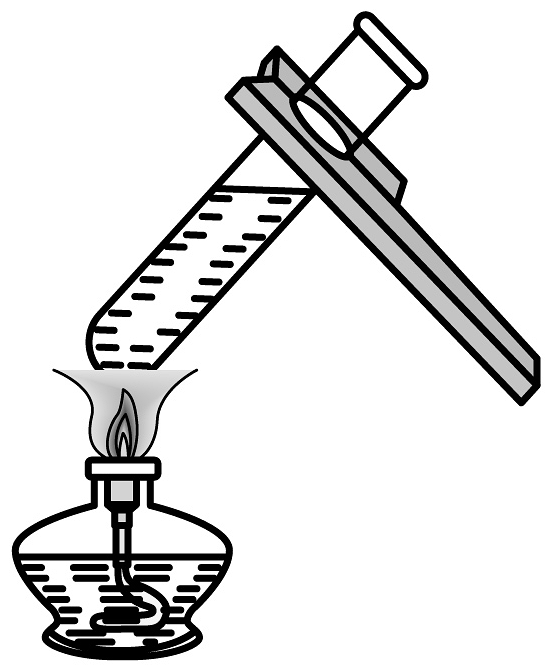 加热液体
B、
加热液体
B、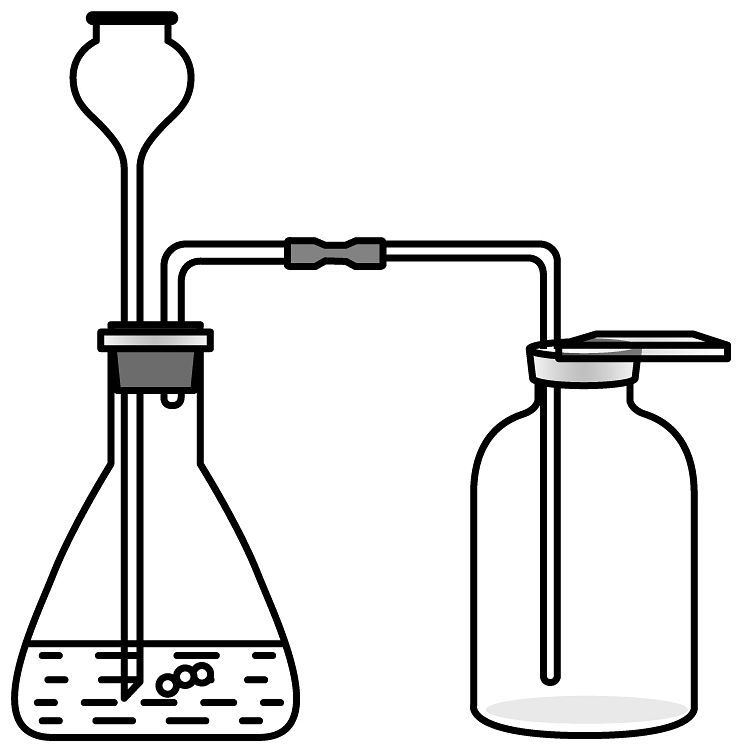 制取氧气
C、
制取氧气
C、 过滤浊液
D、
过滤浊液
D、 验满氧气
验满氧气
-
16、人类的生命活动离不开氧气。下列过程中氧气发生化学变化的是A、氧气在水中溶解 B、工业上分离液态空气制取氧气 C、硫在氧气中燃烧发出明亮的蓝紫色火焰 D、在高压、低温下,把氧气变成液体或固体
-
17、
大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是。
某研究小组发现,将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【作出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
(2)
实验步骤
实验现象
结论及解释
Ⅰ.A和B都加入5mL5%的过氧化氢溶液

A中无明显现象,B中产生大量能使带火星木条复燃的气体
B中产生的气体是①。
Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣
B中又产生大量使带火星木条复燃的气体;滤渣质量为ag
②淀粉的和在反应前后均没有发生变化,能作过氧化氢分解的催化剂
(3)写出淀粉催化过氧化氢分解的文字表达式:。
【实验拓展】
该小组设计了如图所示装置对比淀粉与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据见表:

实验编号
3%过氧化氢溶液的体积
其他物质质量
待测数据
Ⅰ
20mL
淀粉0.5g
a
Ⅱ
20mL
二氧化锰0.5g
b
(4)上述实验中“待测数据”是指;若a>b,则可得出的结论是。
(5)在过滤中玻璃棒的作用是;过滤后滤液仍然浑浊的原因可能是① , ②;过滤(填“能”“不能”)降低水的硬度。

-
18、
化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下图回答问题。

(1)写出指定仪器的名称:①________;②________。
(2)实验室用高锰酸钾制取氧气时,可选用的发生装置是________(填字母代号)。用排水法收集氧气完毕后,停止加热时的操作顺序是________,然后________,以防止水倒吸入热的试管中,造成试管破裂,高锰酸钾受热的化学反应文字表达式是________。
(3)氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水,溶于水形成的溶液是氨水。实验室用加热氯化铵和消石灰的固体混合物制取氨气。则实验室制取氨气选用的收集装置是________。
(4)小明用C装置收集氧气,一段时间后将带火星的木条伸入瓶口、瓶中,都未见木条复燃,其原因可能是________。
小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并用传感器测定收集到的氧气浓度,数据见表。
收集方法
向上排空气法
排水法
氧气浓度/%
79.6
79.7
79.9
90.0
89.8
89.3
氧气平均浓度/%
79.7
89.7
(5)小柯用向上排空气法收集氧气时,以能使放置在集气瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到________为氧气集满的标准;
(6)以上两种方法中,________法收集到的氧气更纯净;
(7)用向上排空气法收集到的氧气浓度只有80%左右的原因有___________。
A. 氧气的密度略大于空气的密度 B. 加热高锰酸钾固体产生氧气的浓度只有80%左右 C. 当观察到带火星木条复燃时,集气瓶内还有空气 D. 当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散 (8)用F装置收集氧气时氧气应从________(填“a”或“b”)通入,如果用F进行排水法收集氧气,集气瓶应先放满水,然后水由________(填“a”或“b”)排出。
-
19、已知相对原子质量(N:14 O:16 H:1),硝酸铵的化学式是:NH4NO3。回答下列问题:(1)、硝酸铵由种元素组成;(2)、每个硝酸铵分子共有个原子;(3)、硝酸铵中氮氢氧的原子数比是;(4)、硝酸铵中氮氢氧的质量比是;(5)、硝酸铵的相对分子质量是;(6)、硝酸铵中氮的质量分数是。
-
20、用元素符号或化学式或名称填空(1)、7个氮原子;3个钠离子;1个氢分子;4个二氧化碳分子。(2)、写名称:SO2;MgCl2;Na2CO3。(3)、写化学式:氧化钙;氢氧化铜;硝酸镁;碳酸亚铁;硫酸铵;氯化铝。