-
1、用化学符号填空:(1)、地壳中含量最多的元素:;(2)、氩气:;(3)、2个氮原子:;(4)、高锰酸钾制取氧气表达式:;(5)、氧化镁中镁元素的化合价:;(6)、2个碳酸根离子:;
-
2、交警对“酒驾”司机进行呼气检测的原理是:橙色的酸性溶液遇白酒中的乙醇迅速生成蓝绿色铬离子(),下列相关说法不正确的是A、检测过程中有化学变化发生 B、属于氧化物 C、中铬元素的化合价为+6 D、硫酸铬的化学式为Cr2(SO4)3
-
3、目前我国城市空气质量日报中的污染物不包括A、可吸入颗粒物 B、一氧化碳 C、二氧化氮 D、氨气
-
4、下列说法正确的是A、过氧化氢由氢、氧元素组成 B、过氧化氢由氢气和氧气混合而成 C、过氧化氢由两个氢原子和两个氧原子构成 D、一个过氧化氢分子由两个氢元素和两个氧元素组成
-
5、下列符号,既表示一种元素,又表示一个原子,还能表示一种物质的是A、N B、O2 C、Fe D、C70
-
6、欣赏中华诗词,陶冶高雅情操。下列诗词中,涉及化学变化的是( )A、北国风光,千里冰封,万里雪飘 B、野火烧不尽,春风吹又生 C、梅须逊雪三分白,雪却输梅一段香 D、乱石穿空,惊涛拍岸,卷起千堆雪
-
7、某补钙保健品中含钙元素的主要成分是碳酸钙(CaCO3)。每片中含碳酸钙约1.5g,(1)、求碳酸钙的相对分子质量;(2)、求碳酸钙中钙元素的质量分数;(3)、如成年人每天需补钙1.2g,则每天需要服用几片?
-
8、利用图甲所示的教材装置测量空气中氧气的体积分数,选用红磷作为药品是最佳选择吗?某兴趣小组设计并开展了如下实验:
①准备如图乙的玻璃容器,顶部用密封盖密封,并检查该装置的气密性。
②将氧气传感器(能实时显示容器内氧气的体积分数)固定在容器内壁,并装入足量的红磷。
③用激光笔点燃红磷,红磷剧烈燃烧,观察并记录氧气传感器所显示的氧气体积分数的变化情况。
④用白磷替换红磷重复步骤①~③。
⑤换用食品脱氧剂(可以直接与氧气反应,无需点燃的物质)重复上述步骤①~③。
根据实验数据,分别绘制三种物质氧化时容器内氧气体积分数随时间的变化情况,如图丙所示。
 (1)、红磷燃烧的的文字表达式 , 现象。(2)、步骤①中检查气密性时,将装置乙玻璃容器浸没水中,如果观察到 , 则说明气密性好。(3)、装置甲中150毫升集气瓶中装入1/5的水,量筒内装有50毫升水,根据图丙的实验数据,用红磷做实验,理论上实验结束后量筒内剩余的水为毫升。(4)、根据该兴趣小组的实验结果,用图甲装置测量空气中氧气的体积分数,你会选用药品是 , 理由。
(1)、红磷燃烧的的文字表达式 , 现象。(2)、步骤①中检查气密性时,将装置乙玻璃容器浸没水中,如果观察到 , 则说明气密性好。(3)、装置甲中150毫升集气瓶中装入1/5的水,量筒内装有50毫升水,根据图丙的实验数据,用红磷做实验,理论上实验结束后量筒内剩余的水为毫升。(4)、根据该兴趣小组的实验结果,用图甲装置测量空气中氧气的体积分数,你会选用药品是 , 理由。 -
9、下图是初中化学常用实验装置(部分夹持装置已省略)。
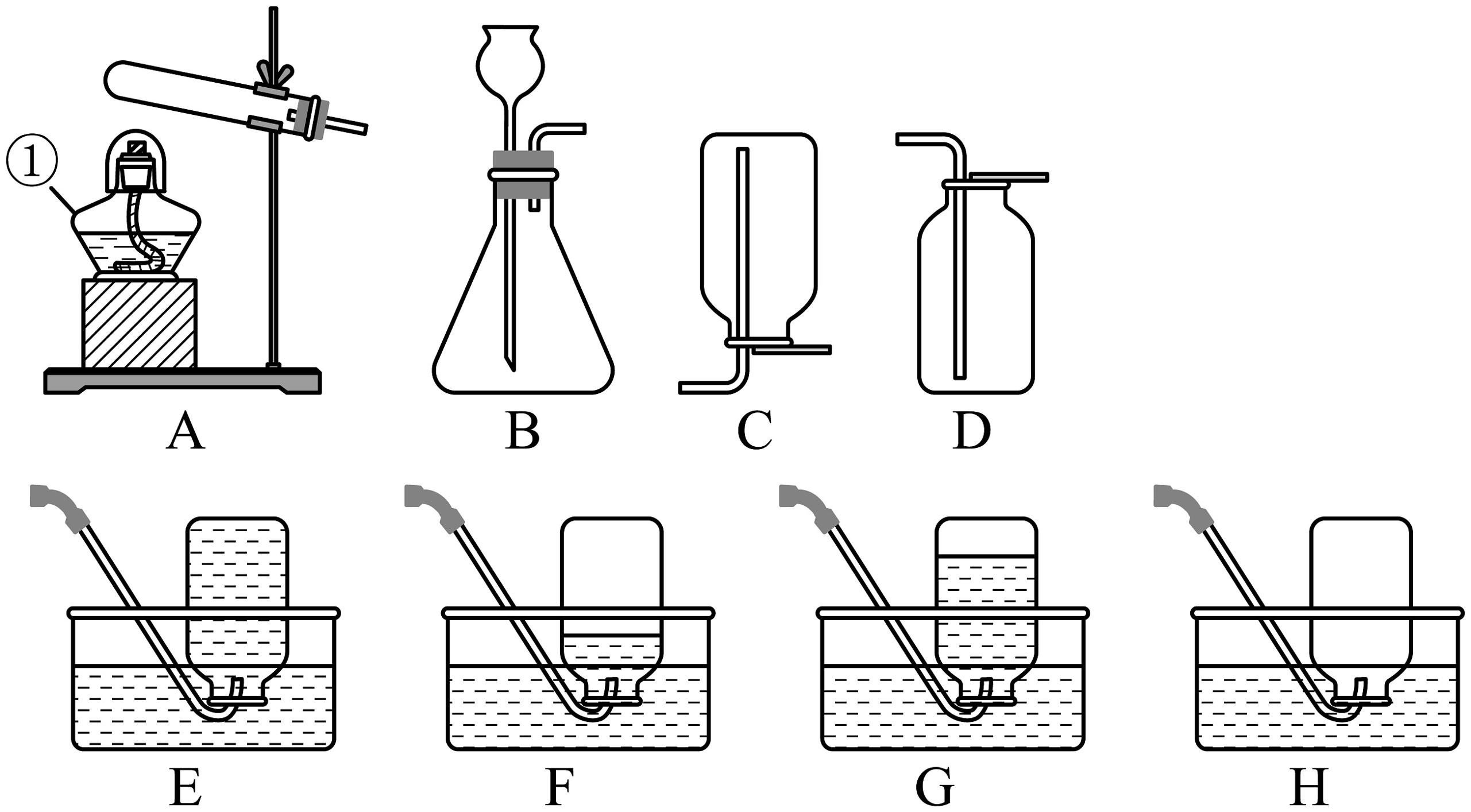 (1)、仪器①的名称是。(2)、实验室用高锰酸钾制取氧气,其反应的文字表达式为 , 反应类型属于(填基本反应类型);收集气体时,若选择装置D收集氧气,验满的方法。(3)、甲同学要做铁丝在氧气中燃烧的实验,用装置E收集氧气,这样做的优点是 , 则此燃烧实验停止收集氧气的最佳时机是(填“F”“G”或“H”);请写出铁丝燃烧的文字表达式。(4)、甲烷是一种无色无味气体,密度比空气小,难溶于水。实验室可用加热醋酸钠与氢氧化钠混合固体制得,应选取上图发生装置(填字母,下同),收集装置。
(1)、仪器①的名称是。(2)、实验室用高锰酸钾制取氧气,其反应的文字表达式为 , 反应类型属于(填基本反应类型);收集气体时,若选择装置D收集氧气,验满的方法。(3)、甲同学要做铁丝在氧气中燃烧的实验,用装置E收集氧气,这样做的优点是 , 则此燃烧实验停止收集氧气的最佳时机是(填“F”“G”或“H”);请写出铁丝燃烧的文字表达式。(4)、甲烷是一种无色无味气体,密度比空气小,难溶于水。实验室可用加热醋酸钠与氢氧化钠混合固体制得,应选取上图发生装置(填字母,下同),收集装置。 -
10、下图是在一个密闭系统中发生化学反应前后存在的分子的微观示意图:
 (1)、参加化学反应的
(1)、参加化学反应的 (一氧化氮)和
(一氧化氮)和 (一氧化碳)两种物质的分子个数比为。反应后的图示中表示的是(填“纯净物”或“混合物”)。 (2)、该反应的文字表达式为。(3)、从微观角度解释化学反应的实质是。
(一氧化碳)两种物质的分子个数比为。反应后的图示中表示的是(填“纯净物”或“混合物”)。 (2)、该反应的文字表达式为。(3)、从微观角度解释化学反应的实质是。 -
11、阅读下列科普短文,回答相关问题。
我国在火箭技术上飞速进步,离不开化学研究。火箭燃料肼(N2H4)又称联氨,有类似于氨的刺鼻气味,点燃时与助燃物质液态N2O4(四氧化二氮)发生反应,生成N2和H2O。肼燃烧放出大量的热,且燃烧产物对环境无污染,是一种高能火箭燃料。肼的熔点14℃,沸点113.5℃;有强烈的吸水性,能吸收空气中的二氧化碳;易溶于水;与液氧接触能自燃;长期暴露在空气中或短时间受热时易发生分解。
(1)、肼在常温(20℃)下为(填“固态”“液态”或“气态”)。(2)、从宏观角度上看,肼是由(填元素名称)组成,肼的化学性质是由(填微粒名称)保持的,肼在化学变化中的最小粒子是(填化学符号)。(3)、写出上述信息中的一个化学反应的文字表达式。(4)、肼需要密封保存的原因是。(5)、下列对火箭燃料燃烧时的助燃物质N2O4的认识正确的是______(填字母)。A、N2O4和NO2的化学性质相同 B、N2O4可以作为燃料 C、N2O4具有助燃性 D、N2O4的性质是氧气、氮气化学性质的综合 -
12、下表为元素周期表部分元素的相关信息,利用下表回答相关问题:
 (1)、硅原子核外电子数是 , 写一个与Ne原子电子层结构相同的阴离子(填离子符号)。(2)、表中具有相对稳定结构的元素是(填元素符号,任填一个)。(3)、氯元素位于元素周期表中第周期族,与氯元素原子化学性质相似的是(填元素符号)。(4)、从元素周期表观察发现,在同一周期,所有元素原子都有电子层,并且从左至右原子的最外层电子数依次。(5)、已知碳-12原子的质量是1.993×10-26kg,磷的相对原子质量是31,请列式计算一个磷原子的质量(列式即可,无需计算)。
(1)、硅原子核外电子数是 , 写一个与Ne原子电子层结构相同的阴离子(填离子符号)。(2)、表中具有相对稳定结构的元素是(填元素符号,任填一个)。(3)、氯元素位于元素周期表中第周期族,与氯元素原子化学性质相似的是(填元素符号)。(4)、从元素周期表观察发现,在同一周期,所有元素原子都有电子层,并且从左至右原子的最外层电子数依次。(5)、已知碳-12原子的质量是1.993×10-26kg,磷的相对原子质量是31,请列式计算一个磷原子的质量(列式即可,无需计算)。 -
13、用下列物质的序号回答有关问题:
①水蒸气 ②五氧化二磷 ③空气 ④高锰酸钾 ⑤氢气 ⑥铁粉
其中属于混合物的是 , 属于纯净物的是 , 属于单质的是 , 属于化合物的是 , 属于氧化物的是。
-
14、如图是电解水的实验装置。
 (1)、a试管得到的气体为 , a、b两试管得到的气体体积比约为。该反应的文字表达式。(2)、电解水时要在水中加少量氢氧化钠或硫酸钠,目的是为了。(3)、该实验得出的实验结论:。
(1)、a试管得到的气体为 , a、b两试管得到的气体体积比约为。该反应的文字表达式。(2)、电解水时要在水中加少量氢氧化钠或硫酸钠,目的是为了。(3)、该实验得出的实验结论:。 -
15、现在很多地方的中小学校都安装了直饮水机,其主要工作流程如图。
 (1)、流程①的作用是。(2)、流程②超滤膜表面密布许多细小的微孔,只允许水及小分子物质通过,而直径大于膜表面微孔径的物质则被截留在膜的进水侧,该过程相当于净水中的过滤操作。实验室进行该操作时,用到的玻璃仪器有玻璃棒、烧杯、 , 其中玻璃棒的作用是。(3)、实验室在进行过滤操作后,所得液体仍有浑浊,其原因可能是(答一点即可),处理措施是。流程③目的。
(1)、流程①的作用是。(2)、流程②超滤膜表面密布许多细小的微孔,只允许水及小分子物质通过,而直径大于膜表面微孔径的物质则被截留在膜的进水侧,该过程相当于净水中的过滤操作。实验室进行该操作时,用到的玻璃仪器有玻璃棒、烧杯、 , 其中玻璃棒的作用是。(3)、实验室在进行过滤操作后,所得液体仍有浑浊,其原因可能是(答一点即可),处理措施是。流程③目的。 -
16、某小组通过如图所示装置探究过氧化氢浓度对反应快慢的影响(恒压漏斗的作用是平衡装置内的气压,使漏斗内的液体顺利滴下)。实验测得的不同浓度过氧化氢溶液催化分时气压与时间的关系见图2,则下列说法错误的是
 A、由图2可知,过氧化氢浓度越高,分解速率越快 B、反应过程中温度升高,说明过氧化氢分解时不断放热 C、图2中气压先升高,后缓缓降低,可能是图1中的装置漏气 D、由以上分析,实验室制氧气,双氧水浓度略大,有利于加快收集氧气
A、由图2可知,过氧化氢浓度越高,分解速率越快 B、反应过程中温度升高,说明过氧化氢分解时不断放热 C、图2中气压先升高,后缓缓降低,可能是图1中的装置漏气 D、由以上分析,实验室制氧气,双氧水浓度略大,有利于加快收集氧气 -
17、推理是学习化学的一种常用方法,下列推理正确的是A、阴离子带负电荷,则带负电荷的粒子一定是阴离子 B、蜡烛在发生化学变化时发光发热,则发光发热一定是化学变化 C、元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素 D、原子核由质子和中子构成,则原子核中一定含有中子
-
18、央视“3·15”特别节目曝光,某品牌肉制品中含瘦肉精。某种瘦肉精的化学式C12H19ON2Cl3 , 下列有关说法正确的是A、该瘦肉精分子中含有氮分子 B、瘦肉精中氢元素与氧元素的质量比为19:16 C、该瘦肉精由碳、氢、氯、氧四种元素组成 D、瘦肉精由12个碳原子、19个氢原子、1个氧原子、2个氮原子和3个氯原子构成
-
19、区别下列各组物质所选试剂或方法错误的是A、水和食醋——闻气味 B、空气和氧气——带火星的木条 C、水和过氧化氢溶液——少量二氧化锰 D、矿泉水和蒸馏水——过滤后观察是否有杂质残留在滤纸上
-
20、“天宫课堂”中的水球光学实验使用了“人造空气”由78%氨气、21%氧气和少量二氧化碳组成。下列说法中正确的是A、该“人造空气”的主要成分都不是空气污染物 B、将燃着的木条放入“人造空气”中,会立即熄灭 C、若“人造空气”只含有氧气,则更有益于人的呼吸 D、该“人造空气”的成分与空气的成分完全相同