-
1、“双碳”即碳达峰与碳中和。落实“双碳”行动,共建美丽家园。下列做法符合该理念的是A、为了避免疾病传播,使用一次性木筷子 B、为方便翻阅,纸使用单面打印 C、为满足社会使用,大力发展火力发电 D、为出行方面,尽量使用共享自行车
-
2、下列应用只涉及物质的物理性质的是A、煤用作燃料 B、二氧化碳用于灭火 C、氧气用于医疗急救 D、干冰用于人工降雨
-
3、下列过程发生化学变化的是A、活性炭除甲醛 B、用石墨制取人造金刚石 C、将铅笔芯粉末放入生锈的锁孔,便于开锁 D、压缩二氧化碳气体制取干冰
-
4、暴雨过后的河水浑浊不堪,有同学收集到一瓶浑浊的河水,经过以下过程进行净水,实验过程如图一所示。
 (1)、图一中,加明矾的作用是。(2)、图二可用于操作①,玻璃棒的作用是。图三净水柱可代替操作①和操作②进行河水净化,其中除去河水中的色素和异味是利用了活性炭的性。为了净化效果更好,进水口应该选择图中的(选填“a”或“b”)口。(3)、以下关于净化之后水的用途说法正确的是______。A、用高压水枪灭火,是因为水降低了可燃物的着火点 B、用排水法来收集氢气,为了保证氢气纯度高,集气瓶中的水必须装满 C、净化之后的水是纯净水,可以直接饮用(4)、用图四进行电解水实验探究水的组成,写出该实验的符号表达式。
(1)、图一中,加明矾的作用是。(2)、图二可用于操作①,玻璃棒的作用是。图三净水柱可代替操作①和操作②进行河水净化,其中除去河水中的色素和异味是利用了活性炭的性。为了净化效果更好,进水口应该选择图中的(选填“a”或“b”)口。(3)、以下关于净化之后水的用途说法正确的是______。A、用高压水枪灭火,是因为水降低了可燃物的着火点 B、用排水法来收集氢气,为了保证氢气纯度高,集气瓶中的水必须装满 C、净化之后的水是纯净水,可以直接饮用(4)、用图四进行电解水实验探究水的组成,写出该实验的符号表达式。 -
5、化学兴趣小组的同学为了比较氧化铜和二氧化锰对双氧水的催化效果。用如下图所示的装置先后进行了两次实验。
 (1)、实验1:取、4%双氧水与粉末状二氧化锰反应。
(1)、实验1:取、4%双氧水与粉末状二氧化锰反应。实验2:取、4%双氧水与反应。
(2)、在检查装置的气密性后,两次实验时分别将双氧水快速全部注入盛有催化剂的小试管中,借助注射器收集氧气。测得产生相同体积的氧气用二氧化锰作催化剂的时间比用氧化铜作催化剂的时间(选填“长”或“短”),得出结论:二氧化锰对过氧化氢的催化效果比氧化铜好。(3)、写出二氧化锰作为催化剂加速过氧化氢反应的符号表达式 , 基本反应类型是反应。(4)、实验过程中发现U形管内红墨水右侧液面上升,原因是该反应(选填“放热”或“吸热”)。(5)、反思:有同学认为,在上面的实验中还不能说明二氧化锰和氧化铜是过氧化氢分解的催化剂,应补充实验证明二氧化锰、氧化铜在反应前后的质量和保持不变才行。 -
6、
具备基本的实验技能是学习化学的基础和保证。请完成下面的问题:
I、利用下图装置制取气体。

(1)指出带有标号的仪器名称:① 。
(2)A、C装置可用于实验室制备并收集氧气,装置A中反应的符号表达式是:。
(3)已知:在常温下,硫化亚铁固体和稀硫酸反应可以制得硫化氢气体。该气体易溶于水,相同条件下,密度比空气大。由上述信息推知实验室制备并收集硫化氢可选用的装置组合是(填序号)。
II、2023年初,制氧机需求旺盛,市场上出现多种类型的制氧机。
(4)分子筛制氧机:以空气为原料,空气经过分子筛时氮气分子被阻隔,而氧气分子能通过,从而获得高浓度的 , 分离过程中的变化属于(选填“物理”或“化学”)变化。
(5)化学药剂制氧机:某款家用制氧机利用过碳酸钠和二氧化锰同时加入水中,在反应仓中制取氧气,产生的氧气在反应仓高处聚集,经导管从低处进入加湿过滤仓。该制氧机的工作原理示意图如图一。

①加湿过滤仓不仅可以过滤杂质,还可利用氧气溶于水的性质,使氧气变得湿润。
②人的呼吸离不开氧气,给病人输氧时的装置如图二,该装置上类似图三的设计可以监测氧气的流速并加湿氧气,则连接病人口鼻处的是图三中的(选填“a”或“b”)端。
-
7、
化学是以实验为基础的学科,而课本实验是一切变形试验的基础。

I、林林同学为了探究物质燃烧的条件,设计了如图一所示的实验。
(1)通过对比观察①和②,两处的实验现象,能得出可燃物燃烧需要________,发生反应的符号表达式为________,热水的作用是提供热量和________。
II、生活中粉尘使用不当可能引起爆炸,如图二是面粉爆炸实验。
(2)该实验能否用木炭粉尘替代面粉________(选填“能”或“否”)。
(3)面粉加工厂防爆的安全措施是________(写一条即可)。
III、某小组设计了如图三实验装置测定空气中氧气含量。
(4)实验结束,待装置冷却至室温后,将玻璃管右端竖直伸入水槽中,在水中取下橡胶塞。以下说法正确的是______。
A. 气球可防止橡胶塞冲出 B. 实验中移动磁铁有利于装置内氧气充分反应 C. 装置不变时,可用硫磺替代白磷完成该实验 D. 白磷的多少不会影响该实验的结果 -
8、
“宏观辨识与微观探析”是化学学科的核心素养之一。在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
I、人体中必需的微量元素铁、锌、碘、氟、硒等,虽然含量少,但对健康至关重要。图一提供几种微量元素的相关信息,请认真分析并回答下列问题:

(1)上述微量元素中属于非金属元素的有种。
(2)锌原子的中子数为。
(3)碘原子在化学反应中容易得到电子形成离子,写出碘离子的符号。
II、根据图二完成下列各题:

(4)四种粒子中属于同种元素的是(填字母)。
(5)微粒B与微粒C形成的化合物的化学式为。
(6)与微粒A具有相似化学性质的是微粒(填字母)。
(7)微粒D所对应的元素在元素周期表中第周期。
-
9、
I、按照要求写出化学符号。
(1)用于探空气球的氦气;
(2)电解水时加入的氢氧化钠中的阴离子;
(3)汽水中含有的碳酸;
(4)标出中氮元素的化合价;
(5)分析碳酸氢钙的化学式 , 写出碳酸氢钠的化学式。
II、下图是某化学反应的微观示意图,白球表示氢原子,黑球表示氯原子。

(6)保持甲物质化学性质的最小微粒是(用化学用语填空,下同)。
(7)该反应中不发生改变的微粒是。
-
10、以下图像对应说法正确的是
 A、甲表示足量红磷在密封的容器中燃烧,容器内气体压强与时间的关系 B、乙表示用两份等质量等浓度的过氧化氢溶液制氧气 C、丙表示电解水产生气体的体积之比 D、丁表示加热氯酸钾制氧气,试管内固体的质量
A、甲表示足量红磷在密封的容器中燃烧,容器内气体压强与时间的关系 B、乙表示用两份等质量等浓度的过氧化氢溶液制氧气 C、丙表示电解水产生气体的体积之比 D、丁表示加热氯酸钾制氧气,试管内固体的质量 -
11、下列实验方案、现象与结论相对应的是
选项
A
B
C
D
方案




现象
干冷烧杯内壁凝结水珠
A烧杯无明显变化
B烧杯试液变红
带火星的木条复燃
木条在②瓶中比在①瓶中燃烧时间更长,更旺
结论
蜡烛中含有碳、氢、氧元素
氨分子在不断运动
氧气已集满
呼出气体中的氧气含量比空气中的少
A、A B、B C、C D、D -
12、化学家Tim Richard将分子结构简式像小狗的某物质(如图所示)取名为“小狗烯”(化学式为)。下列说法正确的是
 A、1个“小狗烯”分子是由碳元素和氢元素组成的 B、“小狗烯”由52个原子构成 C、“小狗烯”中碳元素和氢元素的质量比为 D、“小狗烯”的相对分子质量为
A、1个“小狗烯”分子是由碳元素和氢元素组成的 B、“小狗烯”由52个原子构成 C、“小狗烯”中碳元素和氢元素的质量比为 D、“小狗烯”的相对分子质量为 -
13、下列归纳正确的是
A.化学与生活
B.物质的分类
①高钙牛奶中的“钙”指钙原子
②充入氮气延长食品保质期
①工业制得的氧气是单质
②与都是化合物,也都是氧化物
C.除杂的方法
D.化学与安全
①木炭粉中混有铁粉——用磁铁吸引
②除去氮气中的氧气——通过灼热的铜
①图书、档案着火,用液态灭火器灭火
②煤气泄漏,及时打开换气扇降低室内燃气浓度
A、A B、B C、C D、D -
14、化学用语是学习和研究化学的重要工具。下列化学用语表示正确的是
① ② ③ ④ ⑤ ⑥
A、①表示2个氢原子 B、②和⑤均可以表示一种元素、一种物质和1个原子 C、④和⑥氧元素的化合价相同 D、③中“2”表示一个铁离子带2个单位正电荷 -
15、规范的操作是安全地进行实验并获得成功的重要保证。如图基本实验操作正确的是A、塞紧橡胶塞
 B、查装置气密性
B、查装置气密性 C、点燃酒精灯后,立即收集气体
C、点燃酒精灯后,立即收集气体 D、实验结束,先熄灭酒精灯
D、实验结束,先熄灭酒精灯
-
16、某市于11月3日晚下了一场大雨,下表是该市连续两天的空气质量日报,下列说法正确的是
日期
污染物及污染指数(单位:)
质量级别
一氧化碳
二氧化硫
二氧化氮
11月3日
21
84
31
25
二级
11月4日
20
23
12
11
一级
A、工厂通过加高烟囱直接排放废气能减少空气污染 B、造成该市空气污染的首要污染物是二氧化硫,且应该增加含量的测定 C、11月4日的空气质量比11月3日差 D、雨后一氧化碳含量变化不大,说明一氧化碳在水中溶解性差 -
17、下列变化中属于物理变化的是A、天然气燃烧 B、霓虹灯通电发光 C、葡萄酿酒 D、光合作用
-
18、化学兴趣小组利用传感器和数据采集器测量模拟建筑火灾现场中氧气含量、二氧化碳浓度和温度的变化,研究火场逃生策略的合理性。
在圆筒形透明塑料实验容器中底部三个位置(如图1)分别放置甲、乙、丙3根高低不同的蜡烛,在3根烛芯一定距离都依次放置氧气传感器(al、a2、a3)、温度传感器(b1、b2、b3)和二氧化碳传感器(c1、c2、c3)(如图2)。点燃蜡烛后,盖上实验容器顶盖后,采集3根蜡烛火焰附近相关数据。
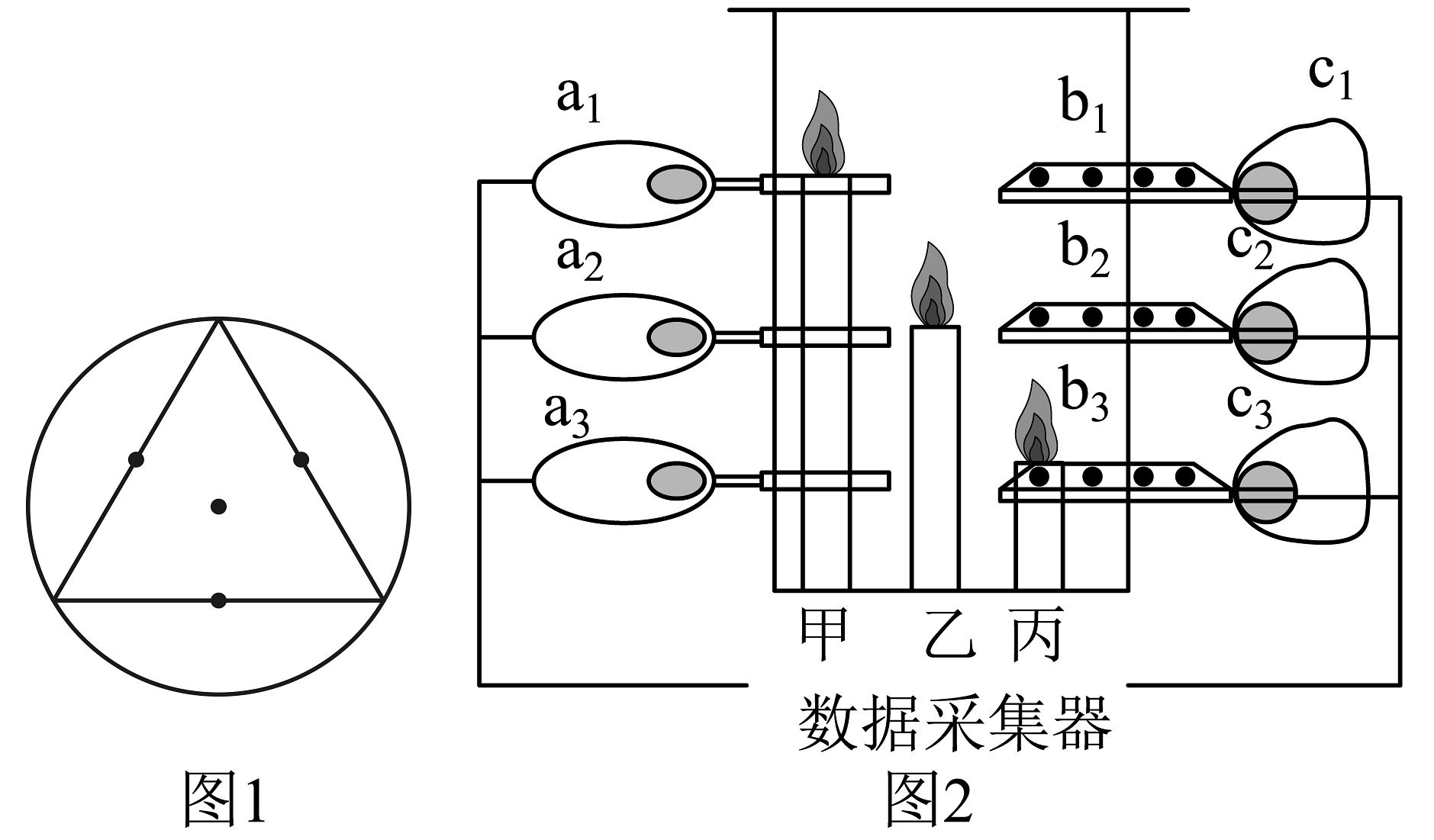 (1)、实验获取3根蜡烛从开始燃烧到熄灭的时间如表1所示,并提取每根蜡烛在这三个时间时火焰附近的含氧量如表2所示。
(1)、实验获取3根蜡烛从开始燃烧到熄灭的时间如表1所示,并提取每根蜡烛在这三个时间时火焰附近的含氧量如表2所示。表1:3根蜡烛开始燃烧到熄灭的时间
蜡烛
甲
乙
丙
时间/s
106
164
199
表2:熄灭时不同高度所测的含氧量%
熄灭时间/s
低处(a3)
中处(a2)
高处(a1)
106
19.8
19.1
18.5
164
18.9
17.7
x
199
18.6
17.1
16.5
①三支蜡烛熄灭的先后顺序是。
②表2中,x可能是(填序号)。
A.18.6 B.17.9 C.17.2 D.16.1
③蜡烛熄灭时,含氧量均不为零。请据此对燃烧条件的表述做进一步的完善:。
④纵看表2数据,处氧气含量下降最慢。
(2)、实验获取温度和二氧化碳浓度随时间变化曲线依次如图3和图4所示。
由此可知,点燃蜡烛后二氧化碳浓度由低处到高处逐渐变 , 原因是。
(3)、从以上两图分析,建筑火灾时,人员应低下身子沿墙壁或贴近地面逃生,原因是。 -
19、
学习小组开展了“设计和制作简易供氧器”的实践活动。
【活动一】
如图甲所示,反应仓中的制氧剂是过碳酸钠和二氧化锰,已知:过碳酸钠加水溶解会分解生成碳酸钠和过氧化氢。用该制氧机制氧时,在反应仓中加入适量水,再先后加入过碳酸钠和二氧化锰,反应仓内的现象为黑色粉末翻腾,溶液变得浑浊,仓壁变得温热,加湿过滤仓底部导气管口有气泡冒出。

(1)加湿过滤仓中的水除了有过滤杂质提纯氧气的作用外,还可以起到的作用是_______(填字母)。
A. 可以通过气泡观察氧气生成的速率 B. 降低氧气温度 C. 加快氧气的生成 (2)验证从加湿过滤仓导出的气体是氧气的方法是________。
【活动二】
(3)同学们在充分思考交流的基础上,利用家庭中常见材料,设计并制作了简易家用制氧机(如图乙),其中A瓶的作用相当于图甲中的________仓。

(4)氧气能大量从A瓶中逸出,是根据氧气________的性质。
(5)对比甲乙装置,说出任一装置的一个优点________。
-
20、化学是一门以实验为基础的科学。请结合如图中装置图回答问题。
 (1)、写出仪器a的名称。(2)、实验室用过氧化氢溶液制取氧气的化学方程式为。(3)、下表为用高锰酸钾制氧气的实验报告,请按要求完成实验报告。
(1)、写出仪器a的名称。(2)、实验室用过氧化氢溶液制取氧气的化学方程式为。(3)、下表为用高锰酸钾制氧气的实验报告,请按要求完成实验报告。实验操作内容
主要现象与结论、解释
I.检查装置的气密性
①将导管一端浸入水中,双手紧握试管,导管口有气泡冒出;移开手后一段时间,导管中会 , 则装置气密性良好。
Ⅱ.装入药品后,在试管口放一团棉花,组装并固定好装置
②试管口略向下倾斜的原因。
Ⅲ.加热药品
③反应的化学方程式为。
IV.用排水法收集气体
④用E装置收集氧气。若改用F装置收集氧气时,进气管应连接在(填“b”或“c”)处。
(4)、通常情况下,甲烷是一种密度比空气小,难溶于水的气体。在加热条件下,可通过醋酸钠固体与氢氧化钠固体及应制取甲烷 , 同时生成碳酸钠。若要制备并收集一瓶干燥的甲烷,选择的装置组合为和(填序号)。