-
1、下列化学用语中,对“3”的含义表述不正确的是A、—3个氮分子 B、—一个铝离子带3个单位的正电荷 C、—3个氧离子 D、—1个氨分子中含有3个氢原子
-
2、氚是氢元素的同位素之一。氢原子和氚原子结构如图所示,下列说法不正确的是
 A、氚原子与氢原子的质子数相同 B、氚原子与氢原子的中子数不同 C、氚原子与氢原子的核外电子数相同 D、氚原子与氢原子的质量相同
A、氚原子与氢原子的质子数相同 B、氚原子与氢原子的中子数不同 C、氚原子与氢原子的核外电子数相同 D、氚原子与氢原子的质量相同 -
3、透过现象看本质。下列有关宏观现象的微观解释不合理的是A、小亮说:我靠闻气味区分氮气和氨气,是因为分子总是在不断运动着,且分子不同性质不同 B、小红说:我向气球里打气,气球变大,是因为分子之间的间隔变大了 C、小明说:我一口气能喝6000万亿亿个水分子,说明水分子很小 D、小颖说:氧气助燃,液氧也助燃,是因为两者是由同种分子构成,化学性质相同
-
4、下列物质中不含有氧分子的是A、表层海水(有鱼存在) B、液氧 C、空气 D、
-
5、硅元素在半导体产业、建筑材料、化工行业等多个领域占据重要地位,如图是硅元素在元素周期表中的信息,下列相关叙述不正确的是
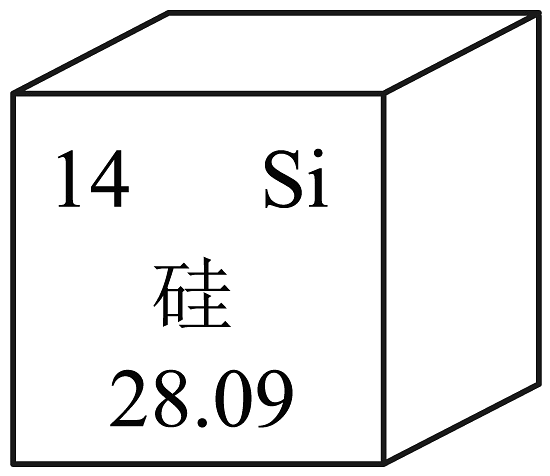 A、硅元素原子核内有14个质子 B、硅元素的元素符号为 C、硅元素属于非金属元素 D、硅元素的相对原子质量是
A、硅元素原子核内有14个质子 B、硅元素的元素符号为 C、硅元素属于非金属元素 D、硅元素的相对原子质量是 -
6、物质燃烧时,可以观察到各种不同的现象,下列关于物质燃烧的现象描述正确的是A、纯净的氢气燃烧时,声音很小,有淡蓝色火焰,冒出白烟 B、铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 C、木炭在氧气中燃烧发出白光,放热 D、蜡烛燃烧有火焰出现,分三层,焰心最亮
-
7、空气是人类和动植物生存所必需的宝贵资源,下列有关空气的说法不正确的是A、有温室效应,是影响空气质量的主要污染物之一 B、氮气的化学性质不活泼,在空气中含量最高 C、氧气可以供给动植物呼吸,用于炼钢、气焊等,是一种宝贵的资源 D、稀有气体通电时发出不同颜色的光,可用于制霓虹灯等
-
8、学习化学后,我们可知下列做法或说法不合理的是A、做完实验,走出实验室前应彻底清洗双手,关闭水电 B、使用明矾净水可以杀灭大部分的细菌和病毒 C、生活中应减少使用一次性筷子,保护森林 D、假期出门多骑单车少开私家车可以节能减排
-
9、物质总在不断变化着,下列变化中,前者属于物理变化,后者属于化学变化的是A、试管破裂、樟脑升华 B、植物光合作用、细胞呼吸作用 C、水的沸腾、粮食酿酒 D、钢铁生锈、电灯发光
-
10、如图所示为实验室中常见的气体制备和收集装置。请回答问题:
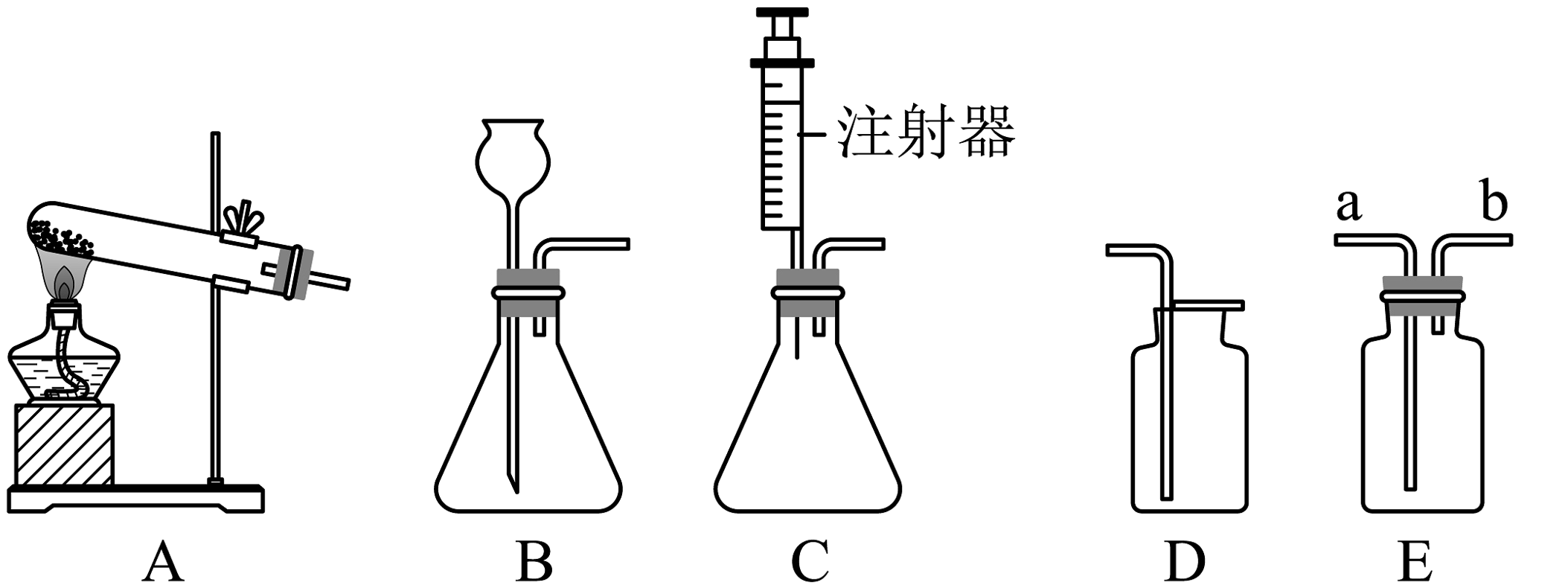 (1)、实验室用加热高锰酸钾制取氧气,应选用发生装置(填字母序号),反应的化学方程式为。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为;若选用C做发生装置,你认为该装置的优点是。(3)、若用D装置收集氧气,证明收集满了的方法是 , 欲使用装置E用排水法收集氧气,该如何操作?。(4)、“蛟龙号”是我国研制出的大深度载人潜水器。为保证载人潜水器长时间潜水,需要在潜水器里配备供氧装置,利用过氧化物供氧是一种常见的供氧技术。
(1)、实验室用加热高锰酸钾制取氧气,应选用发生装置(填字母序号),反应的化学方程式为。(2)、实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为;若选用C做发生装置,你认为该装置的优点是。(3)、若用D装置收集氧气,证明收集满了的方法是 , 欲使用装置E用排水法收集氧气,该如何操作?。(4)、“蛟龙号”是我国研制出的大深度载人潜水器。为保证载人潜水器长时间潜水,需要在潜水器里配备供氧装置,利用过氧化物供氧是一种常见的供氧技术。①过氧化钠作供氧剂的化学方程式为 , 则反应物X的化学式为。
②若用上述方法制取氧气,至少需要的质量为多少。
-
11、请从分子角度分析并解释下列问题。(1)、湿衣服在夏天比冬天蒸发快;(2)、氮气可压缩储存于钢瓶中;(3)、混合物和纯净物的不同之处。
-
12、如图是用干净烧杯承接滤液的过滤装置。
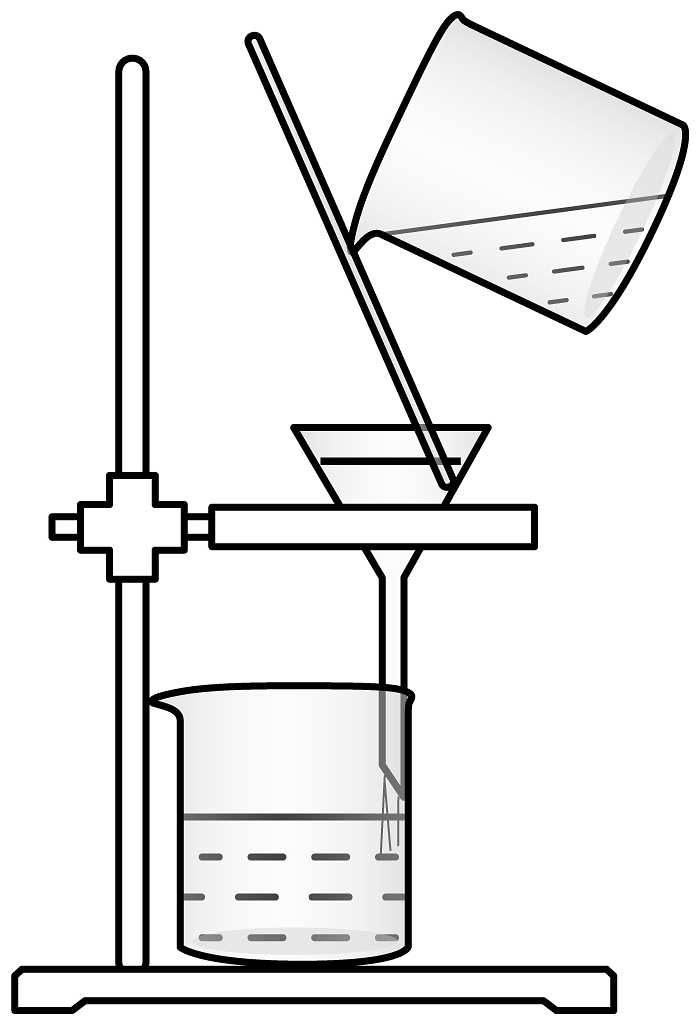 (1)、请写出此操作中玻璃棒的作用。(2)、过滤后发现滤液仍然浑浊,请分析原因。(写出一条即可)
(1)、请写出此操作中玻璃棒的作用。(2)、过滤后发现滤液仍然浑浊,请分析原因。(写出一条即可) -
13、常见铁的氧化物有三种: , 三种物质中氧元素质量分数最大的是;现有一包和的固体混合物,已测得铁元素质量分数为31%,则混合物中硫元素的质量分数为。
-
14、A、B、D是初中化学常见的物质,它们均含有同一种元素,其中A和B的组成元素相同,它们之间的部分转化关系如图所示(“→”表示一种物质可以转化为另一种物质)。
 (1)、写出A的化学式:。(2)、B→D反应的基本反应类型是什么?。(3)、自然界中CO2转变为D的过程被称为什么?。
(1)、写出A的化学式:。(2)、B→D反应的基本反应类型是什么?。(3)、自然界中CO2转变为D的过程被称为什么?。 -
15、“岩盐之都”河南叶县盛产食盐。食盐的主要成分是NaCl,除去食盐水中泥沙等不溶性杂质的方法是(填实验操作名称);已知电解食盐水可得到氢氧化钠、氯气和一种可燃性气体,则该反应的化学方程式为。
-
16、自来水厂用活性炭来除去水中的色素、异味等杂质是因为活性炭具有性;硬水中含有较多的镁离子和钙离子(填离子符号),实验室通过方法得到净化程度较高的水。
-
17、请用合适的化学用语填空:
4个亚铁离子;相对分子质量最小的氧化物;由地壳中含量最高的金属元素组成的氧化物的化学式为。
-
18、原煤(含硫元素)在氧气中不完全燃烧会生成 CO、CO2 和 SO2。SO2 在空气中溶于雨水会形成酸雨。若测得 CO、CO2 和 SO2 的混合气体中碳元素的质量分数为24%,则其中 SO2 的质量分数可能是( )A、10% B、30% C、50% D、70%
-
19、在反应中,已知A和B的相对分子质量之比为 , 当与一定量B恰好完全反应后,生成 , 则生成C的质量为A、 B、 C、 D、
-
20、如图为碘元素在元素周期表的部分信息及其原子结构示意图。下列说法错误的是
 A、碘属于非金属元素 B、碘原子的质子数为53 C、碘元素位于元素周期表中的第四周期 D、碘原子在化学反应中易获得电子
A、碘属于非金属元素 B、碘原子的质子数为53 C、碘元素位于元素周期表中的第四周期 D、碘原子在化学反应中易获得电子