-
1、阅读下列科普短文,回答有关问题。
锡是“五金”(金、银、铜、铁、锡)之一,具有质地柔软、熔点低和无毒等优良特性。自然界中的锡主要以氧化物(如锡石,主要成分为SnO2)和硫化物(如硫锡石,主要成分为SnS)的形式存在。宋代宋应星所著的《天工开物》中记载锡的冶炼:“凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化……点铅勾锡……”

常温下,锡露置于空气中能保持金属光泽,但易被酸腐蚀。锡与氯气反应生成的四氯化锡(SnCl4)可用于制作FTO导电玻璃,用来制作液晶显示屏。以锡为原料加工而成的金属工艺品以色如银,亮如镜,声如馨,色泽历久常新的特点而深受人们的喜爱。锡还广泛用于电子信息、化工冶金及航天工业等。
(1)、自然界中的锡主要以形式存在(填“单质”或“化合物”)。(2)、二氧化锡(SnO2)和硫化亚锡(SnS)中锡的化合价是否相同(填“是”或“否”)。(3)、SnO2中锡元素与氧元素的质量比为 , 炼锡时“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是。(4)、下列说法正确的是______(填序号)。A、锡常温下不易被空气氧化 B、锡制品能够盛放含有柠檬酸的饮料 C、硫锡石炼锡过程中可能会产生酸性气体,污染环境(5)、FTO导电玻璃生产过程中,以SnCl4和水反应生成HCl和一种氧化物,其化学方程式为。 -
2、明代著作《天工开物》对“海水盐”有此记载:“凡海水自具咸质”“凡煎盐锅古渭之‘牢盆’……用铁者以铁打成叶片……其下列灶燃薪,多者十二三眼,少者七八眼,共煎此盘……火燃釜底,滚沸延及成盐”。
 (1)、“咸质”的主要成分为(填化学式)。(2)、“以铁打成叶片”,铁能被打成铁片是因为铁具有良好的。(3)、“燃薪”后灶底可得草木灰(含),属于(填“酸”或“碱”或“盐”),农业上可作。(4)、“共煎此盘”时,需要不断往灶底通风,原因是。(5)、“滚沸延及成盐”是指盐水沸腾直至固体逐渐析出,此过程相当于实验室中的操作,属于(填“物理”或“化学”)变化。
(1)、“咸质”的主要成分为(填化学式)。(2)、“以铁打成叶片”,铁能被打成铁片是因为铁具有良好的。(3)、“燃薪”后灶底可得草木灰(含),属于(填“酸”或“碱”或“盐”),农业上可作。(4)、“共煎此盘”时,需要不断往灶底通风,原因是。(5)、“滚沸延及成盐”是指盐水沸腾直至固体逐渐析出,此过程相当于实验室中的操作,属于(填“物理”或“化学”)变化。 -
3、除去下列物质中的杂质(括号内为杂质),所选用试剂及操作方法均正确的是
选项
物质
选用的试剂及操作方法
A
氨气(水蒸气)
通入浓硫酸
B
Cu(NO3)2溶液(AgNO3)
加入过量铁粉,过滤
C
NaNO3溶液(Na2CO3)
加入适量的氯化钙溶液,过滤
D
KOH溶液(K2CO3)
加入适量的氢氧化钙溶液,过滤
A、A B、B C、C D、D -
4、如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是
 A、t2℃时,甲、乙、丙三种物质的溶解度大小关系甲>乙>丙 B、甲中混有少量乙时,应采用降温结晶的方法提纯甲 C、t1℃时,8g丙物质放入50g水中形成不饱和溶液 D、将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃时,溶质质量分数大小关系为乙>甲>丙
A、t2℃时,甲、乙、丙三种物质的溶解度大小关系甲>乙>丙 B、甲中混有少量乙时,应采用降温结晶的方法提纯甲 C、t1℃时,8g丙物质放入50g水中形成不饱和溶液 D、将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃时,溶质质量分数大小关系为乙>甲>丙 -
5、“一勤天下无难事。”下列劳动项目与所述的化学知识没有关联的是
选项
劳动项目
化学知识
A
使用煤炉烧水时,用扇子往炉中扇风
降低周围温度至着火点之下
B
给鱼池增氧
氧气可供给呼吸
C
用活性炭等净化河水
活性炭具有吸附性
D
用天然气做饭
燃烧放热
A、A B、B C、C D、D -
6、下列说法正确的是A、室内起火时打开门窗通风 B、锁芯加入少量铅笔芯粉末,使锁的开启更灵活 C、青少年缺钙会引起贫血 D、室内放一盆水可防止CO中毒
-
7、空间站内的气体组成和地表空气基本一致,其中体积分数为21%的气体是A、氮气 B、氧气 C、二氧化碳 D、稀有气体
-
8、水是宝贵的自然资源。下列有关水的说法正确的是A、冰水共存物属于混合物 B、探究水的组成,可以用电解水的实验来验证 C、自来水的生产过程包括蒸馏 D、为防止水污染、应禁止使用化肥和农药
-
9、科学种田,助力乡村振兴,农作物的生长需要适宜的酸碱性土壤。小张同学在实验室测量土壤样品酸碱度时,下列操作正确的是A、取水
 B、量水
B、量水 C、溶解
C、溶解 D、测
D、测
-
10、《本草纲目》记载:“火药乃焰硝、硫黄、杉木炭所合……”焰硝经处理可得到含少量的溶液,将其蒸发浓缩、冷却结晶、过滤,最终得到较纯净的固体。和的溶解度曲线如下图所示。下列说法正确的是
 A、的溶解度大于的溶解度 B、“蒸发浓缩”是为了获得较高温度下的饱和溶液 C、的溶解度随温度降低大幅减小,所以“冷却结晶”时析出晶体 D、“过滤”所得滤液中的溶质只含有
A、的溶解度大于的溶解度 B、“蒸发浓缩”是为了获得较高温度下的饱和溶液 C、的溶解度随温度降低大幅减小,所以“冷却结晶”时析出晶体 D、“过滤”所得滤液中的溶质只含有 -
11、甘油()具有润滑作用。关于甘油的说法正确的是A、属于氧化物 B、氧元素的质量分数最大 C、由14个原子构成 D、碳、氢元素质量比为3:8
-
12、水是生命之源,也是重要的化学资源。兴趣小组用思维导图梳理了对水的认识,下列说法正确的是
 A、存在:自然界中淡水的储量比咸水高 B、净化:过滤能去除水中的难溶性杂质 C、结构:水由氢原子和氧原子直接构成 D、变化:电解水生成H2和O2的质量比为2:1
A、存在:自然界中淡水的储量比咸水高 B、净化:过滤能去除水中的难溶性杂质 C、结构:水由氢原子和氧原子直接构成 D、变化:电解水生成H2和O2的质量比为2:1 -
13、科学家通过“祝融号”火星车探测器测得火星表面大气成分(体积分数)如图所示,下列说法正确的是
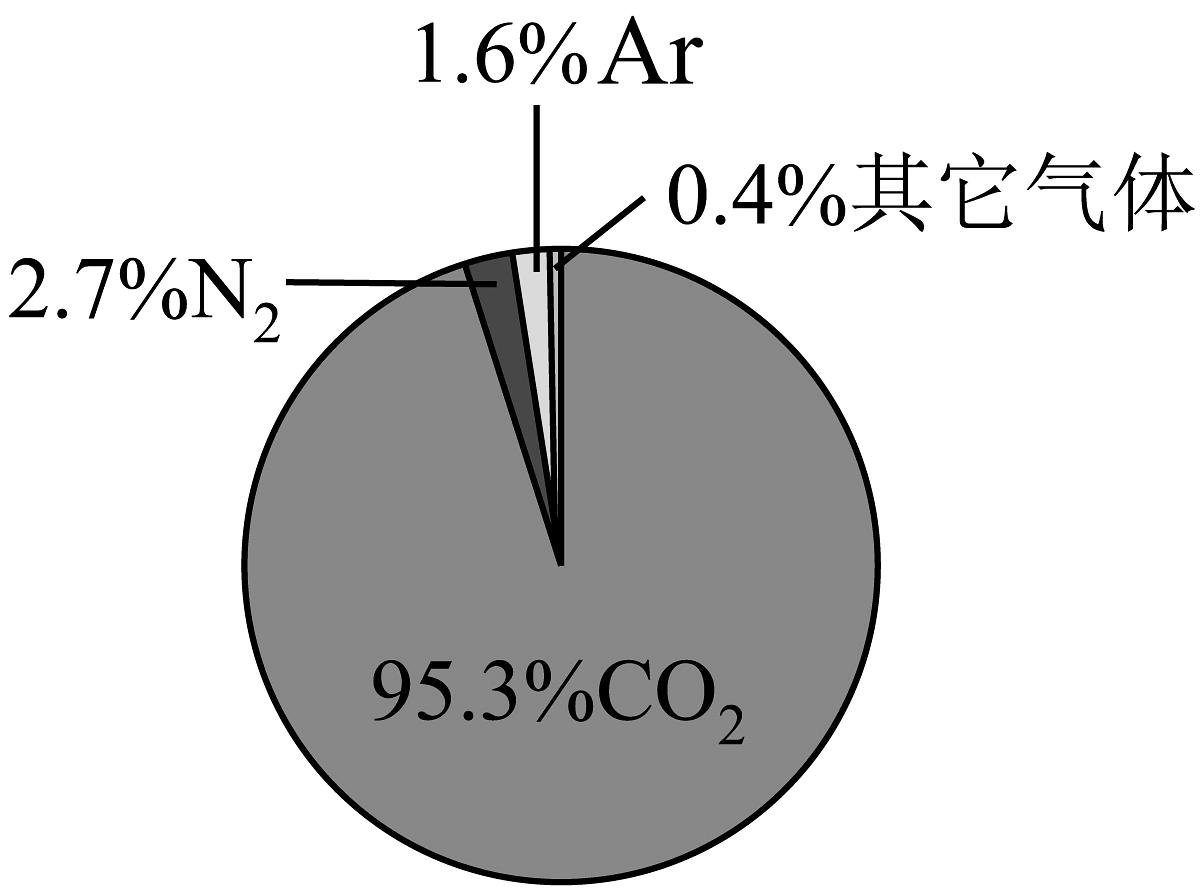 A、火星大气中不含稀有气体 B、火星大气能使带有火星的木条复燃 C、火星大气中N2的含量最高 D、火星大气中CO2的含量高于地球大气中
A、火星大气中不含稀有气体 B、火星大气能使带有火星的木条复燃 C、火星大气中N2的含量最高 D、火星大气中CO2的含量高于地球大气中 -
14、2024年5月1日,我国首部节水行政法规《节约用水条例》实施。如图为国家节水标志的是A、
 B、
B、 C、
C、 D、
D、
-
15、老师和同学们在开展“基于特定需求设计和制作简易供氧器”的跨学科实践活动中,设计了下图实验装置,在实验的过程中共消耗了200g过氧化氢溶液,制得8g氧气。请完成下列分析及计算:
 (1)、乙装置中水的作用是(答一点)。(2)、原过氧化氢溶液的溶质质量分数是。(请写出计算过程)
(1)、乙装置中水的作用是(答一点)。(2)、原过氧化氢溶液的溶质质量分数是。(请写出计算过程) -
16、
粮食安全是“国之大者”,保护好耕地,才能端牢“中国饭碗”。某化学社会实践小组的同学为深入了解当地土壤保护情况,他们在老师的指导下展开土壤肥力、退化、成分、保护等方面的项目式学习研究。
任务一:调查土壤肥力的情况
小组同学实地考察了当地多个村庄耕地,发现土壤的颜色均为黄色。
【信息搜索】
有机质为植物生长提供了养分,土壤中的有机质越多颜色越黑,其肥力就越高。土壤有机质来源主要包括栽培作物残茬,人类每年向土壤中施用的堆肥、沤肥和厩肥等。
【交流讨论】
(1)当地土壤肥力(填“较高”或“不高”)。任务二:分析导致土壤退化的原因
同学们通过数字化平台,向农科院专家进行了咨询,得知导致土壤退化有人为因素,也有自然因素,如风蚀、水蚀等自然灾害会导致土壤退化。
【分析思考】
(2)你认为导致土壤退化的人为因素有(答一点)。任务三:探究土壤中矿物质的成分
【提出问题】土壤中是否含有氯化钠、碳酸钠?
【实验准备】取少量土壤样品按的质量比与蒸馏水在烧杯中混合,充分搅拌后,静置。
【进行实验】
(3)小组同学为探究当地土壤成分设计如下方案,并完成了实验。实验步骤
现象
结论
①取少量上层清液于试管中,滴加足量稀盐酸
样品中含有
②向步骤①所得溶液中再滴加几滴硝酸银溶液
产生白色沉淀
样品中含有NaCl
【反思评价】
(4)步骤①发生反应的化学方程式为。(5)小明对步骤②的结论提出质疑,理由是。任务四:交流当地土壤的保护
【成果共享】
(6)土壤保护需要农、林、牧、工统一规划,合理利用和管理土壤资源,多用有机肥,适当提高需要量较大的营养元素N、P、的含量,使土壤肥力、土壤生产力以及环境景观都得到改善和提高。 -
17、室外的铁制栏杆在多雨季节易生锈,小谢同学对铁生锈的条件进行了探索,实验装置如图所示。5天后,发现只有装置C中的铁丝生锈了。
 (1)、装置A中生石灰(CaO)的作用是。(2)、装置B、C中的实验现象说明与接触是铁生锈的条件之一。(3)、为研究铁粉生锈快慢的影响因素,小组同学设计了如下图1实验装置分3组试剂进行实验,测得温度随时间变化的曲线如图2所示。已知铁粉生锈能放出大量的热。
(1)、装置A中生石灰(CaO)的作用是。(2)、装置B、C中的实验现象说明与接触是铁生锈的条件之一。(3)、为研究铁粉生锈快慢的影响因素,小组同学设计了如下图1实验装置分3组试剂进行实验,测得温度随时间变化的曲线如图2所示。已知铁粉生锈能放出大量的热。实验
试剂

实验1
4g铁粉、2mL水、2g氯化钠
实验2
4g铁粉、2mL水、2g活性炭
实验3
4g铁粉、2mL水、2g活性炭、2g氯化钠
分析得出:(填物质名称)共同作用下能短时间内加快铁粉的生锈。
(4)、铁锈的主要成分是氧化铁,在实验室可以用稀盐酸来除去铁钉表面的铁锈,请写出用稀盐酸除铁锈的化学方程式:。 -
18、
“扬帆起航、逐梦九天”,中国航天事业在浩瀚的太空中不断刷新“中国高度”。
【“天和”升空】“长征五号B遥二运载火箭”成功发射“天和”核心舱,中国空间站时代到来。
(1)火箭的推进剂使用液氢和液氧的组合。从微观角度分析:氢气和液氢都具有可燃性的原因是。
【“天问”探火】我国“天问一号火星探测器”着陆于火星,对火星地貌、土壤、大气等进行探测。
(2)火星土壤中含量最多的元素与地球地壳中含量最多的元素相同,该元素是(填名称)。
(3)火星大气的主要成分是 , 约占96%,而仅占0.13%。为了人类未来可以移居火星,化学家通过下图所示的过程将转化为。用途广泛,请举一例:。

【“神舟”出征】继“神舟十二号载人飞船”首次将航天员送入“天和”核心舱起,我国开启了长期驻留太空的时代。
-
19、臭豆腐是中国传统特色小吃。各地的臭豆腐中,湖南长沙臭豆腐因其“黑如墨、香如醇、嫩如酥、软如绒”的特点而深受广大消费者喜爱。臭豆腐坯的品质直接关系着臭豆腐的鲜嫩程度、入味程度和油炸效果。生产工艺流程为:黄豆豆腐坯上色(用硫酸亚铁等)臭卤浸泡臭豆腐坯。国家标准GB2760—2014中规定,在臭豆腐的制作过程中,硫酸亚铁的最大使用浓度为。实验小组研究了一定条件下硫酸亚铁浓度对臭豆腐上色效果的影响,结果如下图所示。(L值表示颜色明度,为黑色,为白色。)臭豆腐富含蛋白质、维生素等。维生素可以延缓大脑老化,降低老年痴呆的发病率。需要注意的是,臭豆腐中含有的胺类物质可与亚硝酸盐反应,生成致癌物亚硝胺。因此,在吃臭豆腐时,最好多吃富含维生素C的新鲜蔬菜和水果,以阻断亚硝胺的生成。

依据文章内容回答下列问题。
(1)、硫酸亚铁的化学式为。(2)、依据短文可知,硫酸亚铁较适宜的上色浓度为 , 理由是。(3)、臭豆腐与新鲜蔬菜和水果搭配食用更健康的原因是。 -
20、我国新能源汽车近年来发展迅速,产销量连续9年位居世界第一,燃油汽车和新能源汽车是当今社会交通工具的两大主流类型。纯电动汽车因其能源利用率高、结构简单、噪声小等优点成为近年来使用最广的新能源汽车。(1)、用新能源汽车替代燃油车,得到有效保护的不可再生能源是_______(填序号)。A、氢能 B、核能 C、石油 D、风能(2)、电池在驱动电车运行时,能量由化学能转化为 , 再转化为机械能。(3)、生产电池时,在电池材料中添加适量的石墨烯作导电剂,可以有效提高电池的性能,但过多的石墨烯会阻碍电池中锂离子的迁移,导致电池内阻增加,性能下降。为此,科研团队就石墨烯含量对粉末电阻的影响展开研究,结果如图所示。据图分析:

①电池性能最佳时石墨烯含量是。
②曲线BC段电池内阻增加的原因是。