-
1、某化学小组进行化学实验专题的探究学习,请回答下列问题。
 (1)、仪器X的名称是 , 若选用A装置利用制备 , 改进方法是在导管口。(2)、若在装置B中装满水,收集时,应从装置B的(选填“m”或“n”)口处通入。(3)、实验室用锌粒和稀硫酸制取 , 选用的发生装置是(填序号)。
(1)、仪器X的名称是 , 若选用A装置利用制备 , 改进方法是在导管口。(2)、若在装置B中装满水,收集时,应从装置B的(选填“m”或“n”)口处通入。(3)、实验室用锌粒和稀硫酸制取 , 选用的发生装置是(填序号)。 -
2、铜是人类最早利用的金属之一。利用废旧电池铜帽(含Cu、Zn两种金属)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如图所示(反应条件已略去)。
已知:。
 (1)、溶液A中一定含有的溶质是(填化学式)。(2)、过程Ⅱ的实验操作名称是。(3)、过程Ⅲ中发生反应的化学方程式是。
(1)、溶液A中一定含有的溶质是(填化学式)。(2)、过程Ⅱ的实验操作名称是。(3)、过程Ⅲ中发生反应的化学方程式是。 -
3、科普阅读
北京冬奥会期间,近千辆氢燃料电池大巴车参与服务。氢燃料电池系统包括电堆、氢气供应系统、氧气供应系统等。氢气和氧气通过在电堆中发生化学反应,实现能量转化。氢燃料电池效率高,发电效率达到80%以上。随着氢燃料电池汽车的广泛使用,氢能产业链也得到长足发展。
氢的储运是氢能产业链中的瓶颈问题。目前,储氢技术有了新的发展,其中金属氢化物储氢是把氢以氢化物的形式储存在金属或合金中。如图为一些储氢材料的质量储氢密度(储氢后氢元素在储氢材料中的质量分数)。
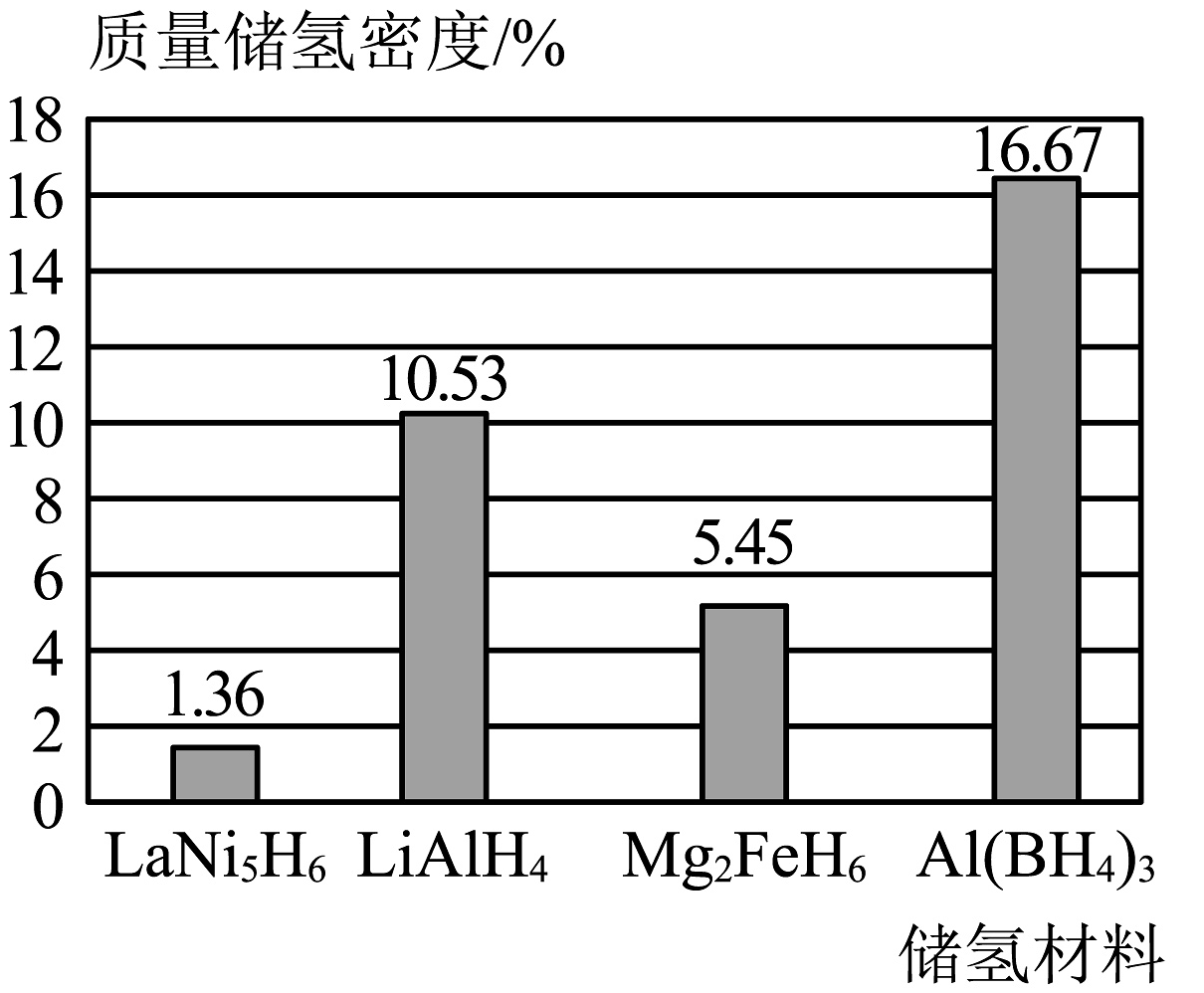 (1)、氢燃料电池的能量转化形式是。(2)、结合图示,储氢材料中最理想的是。(3)、氢燃料电池具有广阔应用前景的依据是(写一条即可)。
(1)、氢燃料电池的能量转化形式是。(2)、结合图示,储氢材料中最理想的是。(3)、氢燃料电池具有广阔应用前景的依据是(写一条即可)。 -
4、下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。回答下列问题:
 (1)、℃时,甲、乙两种物质的溶解度相等;(2)、将时甲、乙、丙三种物质的饱和溶液分别降温到 , 所得溶液的溶质质量分数由大到小的顺序为;(3)、当乙物质中混有少量甲物质时,可以用(填“蒸发结晶”或“降温结晶”)的方法提纯乙。
(1)、℃时,甲、乙两种物质的溶解度相等;(2)、将时甲、乙、丙三种物质的饱和溶液分别降温到 , 所得溶液的溶质质量分数由大到小的顺序为;(3)、当乙物质中混有少量甲物质时,可以用(填“蒸发结晶”或“降温结晶”)的方法提纯乙。 -
5、“古丈毛尖”是湖南绿茶代表,产自武陵山脉生态茶区。(1)、绿茶营养价值很高,富含的锗、硒、钼等对人体具有重要保健作用,这里的“锗、硒、钼”等是指______(填字母)。A、单质 B、原子 C、元素(2)、用含杂质少的软水泡茶,能充分体现茶的色、香、味。在生活中经常使用的方法使硬水转化为软水。(3)、“清汤绿叶,味鲜醇、香扑鼻”。“香扑鼻”从分子角度解释其原因是。
-
6、镓是一种奇妙的金属,放在手心会马上熔化,犹如荷叶上的水珠流来流去。金属镓(Ga)可用于制半导体,Ga、A、B、C、D、E的微粒结构示意图如图所示。回答下列问题:
 (1)、镓原子结构示意图中x的数值为。(2)、A—E中,与镓元素化学性质相似的是(填元素符号)。(3)、2024年长沙橘子洲灯光秀采用新型LED节能技术,LED灯的核心材料是氮化镓(GaN)。氮化镓中氮元素为价,则镓元素的化合价为。
(1)、镓原子结构示意图中x的数值为。(2)、A—E中,与镓元素化学性质相似的是(填元素符号)。(3)、2024年长沙橘子洲灯光秀采用新型LED节能技术,LED灯的核心材料是氮化镓(GaN)。氮化镓中氮元素为价,则镓元素的化合价为。 -
7、将铝粉加入到一定质量的溶液中,充分反应后得到蓝色滤液和滤渣。下列说法正确的是A、滤渣中可能含有Al,滤液中一定含有 B、向滤渣中滴加稀盐酸,无气泡产生 C、滤渣中只含Cu,滤液中可能含有 D、所得滤渣的质量一定小于加入的铝粉质量
-
8、下列四个图像中能正确反映对应变化关系的是
 A、用等质量等浓度的过氧化氢溶液制取 B、与稀盐酸的反应 C、加热一定质量的高锰酸钾固体 D、木炭还原氧化铜的反应
A、用等质量等浓度的过氧化氢溶液制取 B、与稀盐酸的反应 C、加热一定质量的高锰酸钾固体 D、木炭还原氧化铜的反应 -
9、著名的发明家诺贝尔经过长期的研究与试验,终于发明了安全炸药——三硝酸甘油酯,三硝酸甘油酯的化学式为C3H5N3O9 , 这种炸药发生爆炸的化学方程式为:4C3H5N3O9═12CO2↑+10H2O↑+6X↑+O2↑,则X的化学式为( )A、NO B、NH3 C、N2 D、N2O4
-
10、在探究铁生锈条件的实验中,如图所示。依据所学知识可知下列说法不正确的是
 A、试管A、C对比即可得出铁生锈的条件 B、试管B中使用“煮沸并迅速冷却的蒸馏水”,目的是除去蒸馏水中溶解的氧气 C、试管B中铁钉不易生锈 D、试管D中铁钉生锈的速率比C快
A、试管A、C对比即可得出铁生锈的条件 B、试管B中使用“煮沸并迅速冷却的蒸馏水”,目的是除去蒸馏水中溶解的氧气 C、试管B中铁钉不易生锈 D、试管D中铁钉生锈的速率比C快 -
11、维生素C(化学式:)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法正确的是A、维生素C是氧化物 B、维生素C的相对分子质量为174 C、维生素C中氧元素的质量分数最大 D、维生素C由6个碳元素、8个氢元素、6个氧元素组成
-
12、下列对应的化学方程式书写完全正确的是A、水的电解: B、一氧化碳作燃料: C、镁条燃烧: D、金属铝与硫酸铜溶液反应:
-
13、晋代葛洪所著《抱朴子》一书中记载有“丹砂烧之成水银”,丹砂指的是HgS。如图为该反应的微观示意图(甲、乙、丙、丁分别代表图中对应的四种物质)。下列有关该反应的说法正确的是
 A、该反应是复分解反应 B、参加反应的甲、乙的质量比为 C、该反应前后原子数目发生变化 D、该反应前后氧元素的化合价发生了改变
A、该反应是复分解反应 B、参加反应的甲、乙的质量比为 C、该反应前后原子数目发生变化 D、该反应前后氧元素的化合价发生了改变 -
14、2025年“两会”国务院总理李强的政府工作报告提出:“单位国内生产总值能耗降低3%左右,生态环境质量持续改善”。下列做法能持续改善生态环境质量的是A、大量施用农药,减少作物病虫害 B、直接排放工厂废气,降低生产成本 C、推广使用脱硫煤,减少酸雨的产生 D、焚烧垃圾,保持环境干净整洁
-
15、水是宝贵的自然资源。下列有关水的说法中正确的是A、用水可以区分生石灰和小苏打 B、水由氢气和氧气组成 C、酒精溶液中水不是溶剂 D、电解水实验生成的氢气与氧气的质量比为
-
16、化学反应常常会伴随各种现象。下列有关反应实验现象的描述正确的是A、甲烷在空气中燃烧会产生淡蓝色火焰,生成水和二氧化碳,放出热量 B、溶液与溶液反应,生成白色沉淀 C、锌粒中加入稀盐酸,产生大量气泡,溶液变为浅绿色 D、铁丝在空气中剧烈燃烧,火星四射,生成黑色固体,放出热量
-
17、
项目学习小组对某食品包装中的脱氧剂进行探究。
资料:①该脱氧剂的主要成分包括铁粉、氯化钠、碳酸钠、碳粉和硅藻土。
②氢氧化钠溶液可吸收且不与氢气反应。
③常温常压下,氢气的密度是。碳粉和硅藻土不参与反应。
任务一:探究脱氧原理
同学们设计图1装置进行实验。经过一段时间,待充分反应后,打开止水夹。

(1)观察到的现象是。
(2)造成该现象的原因是。
任务二:探究氯化钠的作用及脱氧过程的温度变化
模拟脱氧剂成分,选择部分试剂设计图2装置进行实验。检查装置气密性,将5g铁粉和2g碳粉加入三颈烧瓶,时刻加入2mL饱和NaCl溶液后,再将一支装有5mL稀盐酸的注射器插到三颈烧瓶上,采集数据(如图3、图4)。

(3)据图3,对比AB段和BC段,说明。时刻,压强又突然变大,其原因.是。
(4)据图4分析,说明脱氧剂在脱氧过程中会(填“放出“或“吸收”)热量。时刻后反应并未停止温度却开始降低,原因是。
任务三:测定脱氧剂中铁粉的含量
为测定脱氧剂中铁粉含量,同学们继续设计并进行实验(如图5)。通过分液漏斗加入稀盐酸至甲中不再产生气泡。注射器起始读数为 , 待反应恢复至室温后,注射器读数为。

(5)甲中铁粉反应的化学方程式为。丙中洗气瓶内盛装的试剂是。若无乙装置,测定结果会(填“偏大”或“偏小”)。
(6)计算脱氧剂中铁粉所占的质量分数为(用字母表示)。
(7)若未“待反应恢复至室温”便读数,对测定结果有何影响,判断并说明理由。
-
18、氢气是理想的绿色能源。如图是我国科学家研发的制氢和贮氢新工艺。
 (1)、中铁元素的化合价为。(2)、“循环制氢”中能循环利用的物质有(填化学式),需不断补充的物质是(填化学式)。该方法与传统电解法制氢相比,其优点是。(3)、“贮氢”时需通入氩气,其目的是。与反应可以“释氢”,其原理为: , 方框内物质的化学式为。(4)、“反应1~反应3”中,属于分解反应的是。写出“反应1”“反应3”的化学方程式:、。
(1)、中铁元素的化合价为。(2)、“循环制氢”中能循环利用的物质有(填化学式),需不断补充的物质是(填化学式)。该方法与传统电解法制氢相比,其优点是。(3)、“贮氢”时需通入氩气,其目的是。与反应可以“释氢”,其原理为: , 方框内物质的化学式为。(4)、“反应1~反应3”中,属于分解反应的是。写出“反应1”“反应3”的化学方程式:、。 -
19、
利用下图实验仪器完成相应的实验活动。

实验一:去除粗盐中难溶性杂质
(1)“溶解”时需用玻璃棒搅拌,其作用是。
(2)“过滤”需选用的仪器有(填字母序号,下同)。若滤纸完好,但所得滤液仍浑浊,此时应。
(3)“蒸发”需选用的仪器有。实验过程中,当时,停止加热。
实验二:探究镍、锌、铜的金属活动性顺序
【猜想】结合已知的金属活动性顺序,同学们作出如下猜想。
(4)猜想一: 猜想二: 猜想三:
【实验】
(5)设计如下实验进行探究。
实验内容
现象
结论
①
镍片上有气泡产生
猜想错误
②将用砂纸打磨过的锌片浸入盛有溶液的烧杯中
猜想二正确
(6)写出实验①中反应的化学方程式:。
-
20、如图是二氧化碳的制取与性质实验。
 (1)、检查图①装置气密性的方法是。(2)、图①实验中检验二氧化碳是否集满的方法是。若用该装置在实验室制取氧气,则制氧的化学方程式为。(3)、图②实验观察到的现象是。依据该现象,可以得出关于二氧化碳性质的结论是、。(4)、根据化学方程式计算,制取2.2g二氧化碳,至少需要碳酸钙的质量是多少?
(1)、检查图①装置气密性的方法是。(2)、图①实验中检验二氧化碳是否集满的方法是。若用该装置在实验室制取氧气,则制氧的化学方程式为。(3)、图②实验观察到的现象是。依据该现象,可以得出关于二氧化碳性质的结论是、。(4)、根据化学方程式计算,制取2.2g二氧化碳,至少需要碳酸钙的质量是多少?