-
1、用27.5g含杂质的高锰酸钾样品制取氧气(杂质不反应),充分加热至固体质量不再改变时,称量固体质量为25.1g。请计算:(1)、生成氧气的质量是g。(2)、计算样品中高锰酸钾的质量分数。(结果精确到0.1%)
-
2、
镁是一种重要的金属,主要用于航空航天和化工等领域。
任务1:了解镁的制备
(1)1792年,科学家通过加热苦土(氧化镁)和木炭的混合物制得镁,同时生成二氧化碳,反应的化学方程式为。
(2)海水淡化后所得的浓盐水中含有较多的氯化钠、氯化镁、硫酸钙等物质,写出浓盐水中的一种阳离子的符号。

任务2:认识镁的应用
(3)镁棒打火石常用于户外生火,用小刀从镁棒上轻轻刮下镁屑,刮削镁棒产生的火花能点燃镁屑及周围的干草,小刀能从镁棒上轻轻刮下镁屑,说明镁具有的物理性质为 , 点燃镁屑发生反应的化学方程式为。
任务3:探究镁的变化
【提出问题】长期存放的镁条表面有一层灰黑色固体,该物质是什么?
【猜想假设】
(4)有同学认为是氧化镁,很快被其他同学否定了,理由是。
【查阅资料】
Ⅰ.已知灰黑色固体为碱式碳酸镁,化学式为 , 高温完全分解生成、、。
Ⅱ.浓硫酸能吸收水蒸气,碱石灰能吸收水蒸气和气体。
【实验过程】称取39.4g该灰黑色固体样品按图进行实验,持续加热至反应完全,测得B、C装置分别增重1.8g、17.6g。

(5)加热前、后均需通入氮气,停止加热后通氮气的作用为(填字母)。
a.防止倒吸
b.使生成的和气体分别被后续B、C装置完全吸收
(6)根据B、C装置增重的质量计算:
①氢元素的质量为0.2g,碳元素的质量为g。
②对数据进行分析后确定,中y=2,z=4,则x=。
-
3、结合图示实验装置,回答下列问题。
 (1)、指出图中b仪器的名称;(2)、用高锰酸钾固体制取较为纯净的氧气,选用的发生装置是(填字母)。(3)、实验室制取二氧化碳时,选用B装置,反应的化学方程式为 , 如用E装置收集二氧化碳,气体应从端通入(填“c”或“d”)。(4)、乙炔()气体由碳化钙(块状固体)与水反应生成,且反应非常剧烈,乙炔难溶于水,密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置组合是。
(1)、指出图中b仪器的名称;(2)、用高锰酸钾固体制取较为纯净的氧气,选用的发生装置是(填字母)。(3)、实验室制取二氧化碳时,选用B装置,反应的化学方程式为 , 如用E装置收集二氧化碳,气体应从端通入(填“c”或“d”)。(4)、乙炔()气体由碳化钙(块状固体)与水反应生成,且反应非常剧烈,乙炔难溶于水,密度比空气略小。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置组合是。 -
4、下图是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
 (1)、反应I在80—900℃的条件下进行,生成TiCl4 , TiCl4中Ti的化合价为;(2)、反应II使用的原料镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应。反应II在高温下可获得海绵钛,请写出化学方程式 , 该反应在下列哪种环境中进行(填字母)。
(1)、反应I在80—900℃的条件下进行,生成TiCl4 , TiCl4中Ti的化合价为;(2)、反应II使用的原料镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应。反应II在高温下可获得海绵钛,请写出化学方程式 , 该反应在下列哪种环境中进行(填字母)。A.稀有气体中 B.空气中 C.N2中 D.CO2气体中
(3)、该工艺流程中,可以循环使用的物质有(填化学式)。 -
5、我国“十四五”规划已经明确“2030年前实现碳达峰”的目标,“碳达峰”是指二氧化碳的排放达到峰值,不再增长,如图为自然界中的循环图,图中箭头指向表示产生(排放)或消耗的途径,回答下列问题:
 (1)、途径④通过光合作用吸收的量白天(填“大于”或“小于”)夜晚。(2)、用学科观点分析碳循环和氧循环,其中正确的是___________(填字母序号)。A、变化观:每个人都在参与碳、氧循环 B、守恒观:碳、氧循环过程中各元素守恒,其化合价不变 C、平衡观:碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 D、微粒观:绿色植物的作用是使自然界中的氧原子总数增加(3)、自然界中的碳循环主要是通过二氧化碳来实现的,图中消耗二氧化碳的途径有(填数字序号)。
(1)、途径④通过光合作用吸收的量白天(填“大于”或“小于”)夜晚。(2)、用学科观点分析碳循环和氧循环,其中正确的是___________(填字母序号)。A、变化观:每个人都在参与碳、氧循环 B、守恒观:碳、氧循环过程中各元素守恒,其化合价不变 C、平衡观:碳、氧循环有利于维持大气中氧气和二氧化碳含量的相对稳定 D、微粒观:绿色植物的作用是使自然界中的氧原子总数增加(3)、自然界中的碳循环主要是通过二氧化碳来实现的,图中消耗二氧化碳的途径有(填数字序号)。 -
6、下图中A~E是初中化学常见的物质,已知A和E都是有可燃性的气体,且A是天然气的主要成分,C是能使澄清石灰水变浑浊的气体,D是实验室常见的一种无色无味的液体。请分析回答:
 (1)、写出物质的化学式:C;D;E。(2)、反应②的化学方程式为。
(1)、写出物质的化学式:C;D;E。(2)、反应②的化学方程式为。 -
7、下图中的①、②分别是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
 (1)、1869年,___________(填字母)发现了元素周期律并编制出元素周期表。A、张青莲 B、门捷列夫 C、拉瓦锡(2)、氟元素的相对原子质量为;(3)、A、B、C、D所示粒子共种元素(填数字);(4)、A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号)(5)、氟原子在化学反应中易(填“得到”或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为。
(1)、1869年,___________(填字母)发现了元素周期律并编制出元素周期表。A、张青莲 B、门捷列夫 C、拉瓦锡(2)、氟元素的相对原子质量为;(3)、A、B、C、D所示粒子共种元素(填数字);(4)、A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似(填序号)(5)、氟原子在化学反应中易(填“得到”或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为。 -
8、按要求用化学用语表示:(1)、3个碳原子;(2)、8个氢气分子;(3)、3个硝酸根离子;(4)、标出锰酸钾中锰元素的化合价。
-
9、生活中处处有化学。现有以下常见的物质:请按要求填空(填字母编号):
A.干冰 B.活性炭 C.氮气 D.石墨
(1)、可用作食品保护气的是。(2)、常用于冰箱除臭的是。(3)、可作制冷剂,也可用于人工降雨的是。(4)、用作电池电极的是。 -
10、重庆被誉为“山水之城,魅力之都”。下列关于水的说法错误的是A、自然界的水循环主要通过物理变化实现 B、活性炭在净水过程中体现了吸附性 C、园林以喷灌和滴灌形式浇灌可节约用水 D、电解水产生的H2和O2的质量比为2:1
-
11、连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为(。下列有关没食子酸的说法,正确的是A、属于氧化物 B、碳、氢、氧元素的质量比为 C、含有3个原子 D、碳、氢、氧元素的原子个数比为
-
12、下列对有关实验现象的叙述或实验操作正确的是A、铁丝在空气燃烧产生黄色火焰 B、硫粉在空气中燃烧产生微弱的淡蓝色火焰 C、将CO还原的尾气直接排入空气 D、加热高锰酸钾制取氧气,并用排水法收集满氧气后,先撤酒精灯,后移出导管
-
13、下列有关空气的说法正确的是A、空气中氧气的质量分数为21% B、空气中各成分的含量相对稳定,是混合物 C、法国化学家拉瓦锡研究了空气的成分,得出氧气约占空气总体积的的结论 D、测定空气中氧气含量实验结束后,容器中剩余的气体为纯净物
-
14、长征五号B运载火箭以偏二甲肼(C2H8N2)和X作推进剂,反应的化学方程式为: , 则X的化学式是A、N2O4 B、NO C、N2O3 D、N2O5
-
15、下列实验方案设计能达到实验目的的是
选项
实验目的
实验设计
A
除去二氧化碳中的少量一氧化碳
在氧气流中加强热
B
除去中的
溶解、过滤、洗涤、干燥
C
鉴别、、三种气体
分别点燃气体,在火焰上方罩一个干冷烧杯
D
除去氧气中的少量氮气
将气体缓缓通过灼热的铜网
A、A B、B C、C D、D -
16、下列物质的用途中,主要利用其化学性质的是A、铜和铝用于生产电缆 B、钢铁作为建筑材料 C、稀有气体用于霓虹灯 D、酒精用作燃料
-
17、习近平总书记指出:“中华优秀传统文化是中华文明的智慧结晶和精华所在,是中华民族的根和魂。”古诗词是中华传统文化的精髓,以下诗句中不涉及化学变化的是A、春蚕到死丝方尽,蜡炬成灰泪始干 B、露从今夜白,月是故乡明 C、爆竹声中一岁除,春风送暖入屠苏 D、千锤万凿出深山,烈火焚烧若等闲
-
18、
中国传统医学对世界医学发展有着深远影响。东晋葛洪《食肉方》(去除黑痣的药方)记载:“取白炭灰、荻灰等分,煎令如膏……可去黑子。”其主要意思是:取等质量“白炭灰”(生石灰)和“荻灰”(即草木灰,其有效成分K2CO3的性质与Na2CO3相似),用水煎煮、去渣浓缩,可用于去除黑痣。某学习小组对药方进行了以下研究,请回答下列问题。
任务一:处理药方。
(1)该小组取少量药方中的材料,加水煎煮时,其中发生的化合反应的方程式为________。(2)取少量滤液,向其中滴加少量酚酞溶液,溶液显________色。(3)该小组同学经过查阅资料,得知最早记载生石灰的《周礼》,其中的生石灰是用牡蛎壳(主要成分是CaCO3)高温烧制而成。该小组同学采用《周礼》中记载的化学原理制备生石灰:先称量11g牡蛎壳,高温烧制后,充分反应至不再产生气体,冷却后称得剩余固体的质量为6.6g。求牡蛎壳中碳酸钙的质量分数。(结果精确到0.1%)任务二:探究药方功效。
2015年诺贝尔生理学或医学奖获奖者屠呦呦,也正是看到《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”才得到灵感,开始研究用乙醚(C2H5OC2H5)从青蒿中提取抗疟疾药物。1972年5月,进行人体试验,试验相关数据如下表所示。根据世卫组织的统计数据,自2000年起,撒哈拉以南非洲地区约2.4亿人受益于青蒿素联合疗法,约150万人因该疗法避免了疟疾导致的死亡。
疟疾类型
使用剂量(每次3g)
总病例数
平均退热时间
疗效
痊愈
有效
无效
间日虐
1日2次,连服3天
3
36时20分
1
2
1日3次,连服3天
4
11时23分
2
2
1日4次,连服3天
4
19时6分
3
1
恶性虐
1日2次,连服3天
2
39时50分
1
1
1日3次,连服3天
2
24时
1
1
1日4次,连服3天
5
35时9分
1
4
(4)请你从见效时间和疗效效果等角度,对间日性疟疾病人给出服药建议:________。 -
19、
CO2是温室气体之一,若得以综合利用,对于温室气体的整治具有重大意义。

Ⅰ.利用CO2和H2O可以制取甲酸(CH2O2)或者甲醇(CH4O),转化关系如上图。
(1)反应①中,若反应条件没有催化剂,二者直接反应的化学方程式为________。
(2)分析图中反应②③,你对催化剂新的认识是________。
(3)反应④的化学方程式为________。
(4)制取甲醇的过程中,可循环利用的物质有________。
Ⅱ.利用CO2通入氨化的饱和食盐水中是著名的“侯氏制碱法”,其原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl。
(5)写出NH4Cl在农业上的用途:________。
Ⅲ.低碳生活。
(6)下列说法错误的是________。(填字母)
A. CO2是温室气体,对人类生活有害无利 B. 化石燃料的过度开采与使用是大气中二氧化碳含量增多的因素之一 C. 植树造林是利用植物的光合作用吸收CO2 , 光合作用属于化学变化 D. 人工合成淀粉为碳的捕集、利用和封存提供了全新的循环方案 (7)作为一名中学生,你能为减少二氧化碳的排放做到:________。(填一种具体做法)
-
20、
在深圳市规划和自然资源局(市海洋渔业局)的指导下,大鹏LNG在陆地上建设“海洋牧场”,利用冷排水开展渔业水产品的养殖研究。化学实践小组的同学们对冷排水的成分等产生了浓厚的兴趣,他们在老师的指导下展开了项目式学习活动。

任务一:探究冷排水的成分。
【教师指导】老师告诉同学们:①鱼池底部泥中的有机物分解易使水质酸性增强;②该鱼池养殖鱼虾,需定期投入为鱼虾补充钙质;③硬水中含有较多和。
【猜想假设】同学们猜想:该鱼塘水呈酸性,且含有。
【实验探究】
(1)
实验步骤
实验现象
实验结论
①取少量冷排水于试管中,向其中滴加几滴________
溶液变成红色
鱼塘水呈酸性,且含有
②另取少量冷排水于试管中,向其中滴加足量溶液
有气体产生,滴加一段时间后产生________
【反思评价】
(2)有同学对实验结论提出了质疑,理由是________,同学们改进方案后重新进行实验,得出了正确的结论。
跨学科实践活动:设计鱼类运输供氧箱
任务二:选供氧剂。
查阅资料:过氧化钙()、过氧化钠()都能与水或二氧化碳反应生成。等质量的两种固体与足量水作用生成碱和氧气,生成的质量与时间的关系如图1所示。
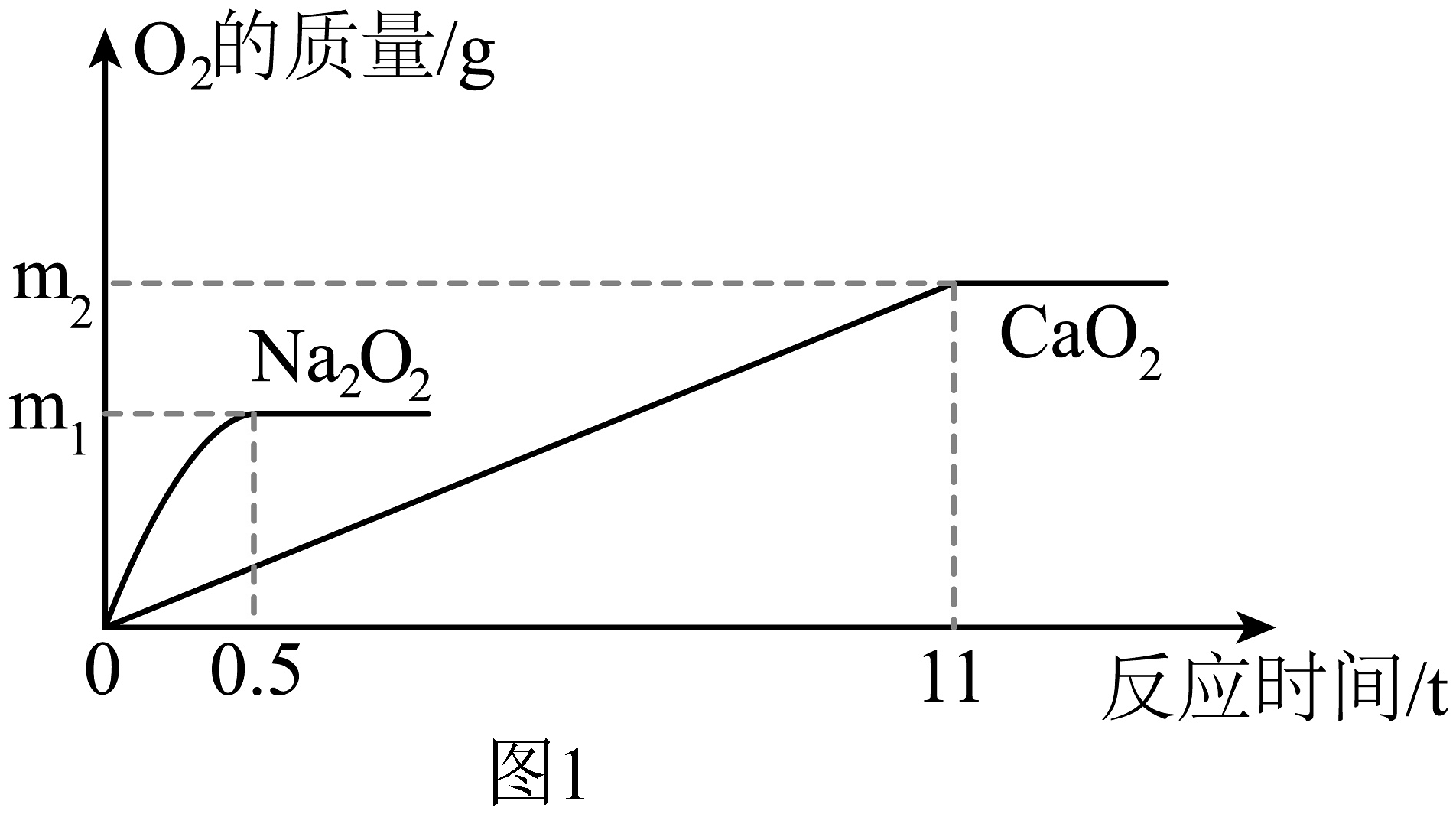
(3)小组讨论后认为选择CaO2更好,理由是________。(写出一条即可)
(4)由资料可知,为防止过氧化钙在空气中变质,应________保存。
任务三:设计装置。
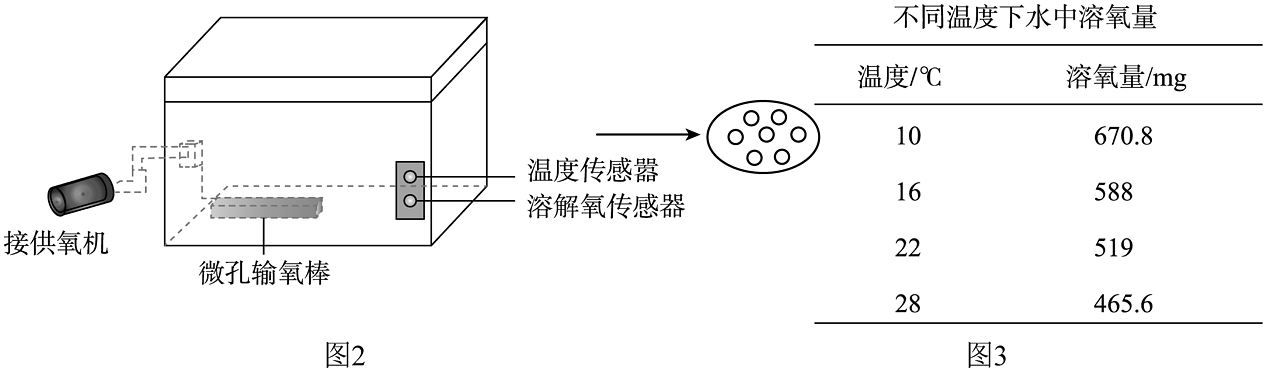
(5)为保证不同鱼类在运输中的存活率,需要监测水中溶氧量和温度。同学们在老师的指导下,设计了如图2的鱼类运输供氧箱,利用该装置持续供氧5分钟,数据记录如图3所示,可得出水中溶氧量随温度变化的规律为________。
(6)选择制作简易供氧器的反应原理时,需要考虑__________。(多选题)
A. 原料是否价廉易得 B. 反应速率是否适中 C. 实验条件是否易于控制 D. 是否安全、环保