相关试卷
-
1、北关中学某同学利用下图微型实验装置进行燃烧条件的探究,下列说法不正确的是
 A、挤压右滴管并轻微加热燃烧管,白磷燃烧而红磷不燃烧,说明燃烧需要温度达到可燃物的着火点 B、挤压左滴管,一段时间后白磷熄灭,说明二氧化碳不支持燃烧、也不可燃烧 C、该探究实验采用了控制变量的探究方法 D、由于该实验没有产生有害气体,所以不需要进行尾气处理
A、挤压右滴管并轻微加热燃烧管,白磷燃烧而红磷不燃烧,说明燃烧需要温度达到可燃物的着火点 B、挤压左滴管,一段时间后白磷熄灭,说明二氧化碳不支持燃烧、也不可燃烧 C、该探究实验采用了控制变量的探究方法 D、由于该实验没有产生有害气体,所以不需要进行尾气处理 -
2、热爱劳动从我做起。下列家务劳动中所涉及的化学知识错误的是
选项
家务劳动
化学知识
A
将洗净的铁锅擦干放置
潮湿的铁锅在空气中易生锈
B
用活性炭除去冰箱异味
活性炭具有吸附性
C
用厨余垃圾自制花肥
物质发生缓慢氧化
D
用食醋除去水壶内的水垢
食醋的pH>7
A、A B、B C、C D、D -
3、火力发电厂为防止煤烟气中二氧化硫污染环境,使用石灰石进行烟气脱硫,发生反应的化学方程式为 , 则X是A、CO2 B、CaO C、CO D、SO3
-
4、打铁花是一种民间传统焰火,属于国家级非物质文化遗产,表演者用木棒将千余度高温的铁水击打到空中,形成十几米高的铁花,场面相当壮观。请完成下列小题。(1)、打铁花表演中,铁水被击打成微小铁屑后剧烈燃烧,其根本原因是A、铁屑温度更高 B、氧气浓度增加 C、铁屑质量更小 D、铁与氧气接触面积增大(2)、打铁花选用生铁而非纯铁,主要利用了生铁的A、熔点更低 B、硬度更大 C、密度更小 D、延展性更好
-
5、常德安乡黄山头的特产之一是绿茶,以下关于绿茶制作中涉及化学变化的是A、高温,破坏酶的活性 B、自然晾晒,去除露水 C、通过外力作用将叶片揉碎 D、蒸发水分并整理外形
-
6、高锰酸钾既可用于实验室制取氧气,也可在生活中用于消毒杀菌。(1)、配制一定溶质质量分数的高锰酸钾溶液的过程如图所示,正确的步骤顺序是(填标号)。
 (2)、实验室需制取0.96g氧气,若完全由高锰酸钾产生,计算消耗高锰酸钾的质量(结果精确到0.1g)。
(2)、实验室需制取0.96g氧气,若完全由高锰酸钾产生,计算消耗高锰酸钾的质量(结果精确到0.1g)。 -
7、
化学兴趣小组的同学在做镁燃烧实验时发现,镁条表面的灰黑色固体会使其难以点燃。他们查阅资料得知,这种灰黑色固体是碱式碳酸镁,其化学式可表示为Mg(OH)b(CO3)c , 该物质受热后可分解为三种氧化物。该小组同学继续对镁条展开探究。已知碱石灰可以吸收水和二氧化碳。
【探究一】金属镁与稀盐酸反应
甲组同学取一小段镁条,用砂纸打磨后进行如图所示的实验。

(1)仪器X的名称是(填“试管”或“集气瓶”)。
(2)图1中发生反应的化学方程式是。
【探究二】测定灰黑色固体的组成
乙组同学称取mg该灰黑色固体进行如图所示的实验,持续加热至样品完全分解。

实验前后,各装置及药品质量如表(假设每步反应、吸收都完全):
装置D
装置E
装置F
实验前质量/g
m1
m2
m3
实验后质量/g
m4
m5
m6
(3)装置B中所盛药品是(填标号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)依据实验数据可算出b∶c=。
(5)若缺少装置A,则测得b∶c的值(填“偏大”“偏小”或“无影响”)。
-
8、纳米Fe3O4在生物医药、污水处理等领域具有良好的应用前景。用铁泥(主要成分为Fe2O3 , 还含有少量FeO和Fe)制备纳米Fe3O4的工艺流程如图所示。
提示:“转化”时发生的反应为Fe+Fe2(SO4)3=3FeSO4。

回答下列问题:
(1)、铁泥属于(填“纯净物”或“混合物”)。(2)、浸取液中含有的离子是(填离子符号)。(3)、酸浸时稀硫酸与氧化铁反应的化学方程式为。(4)、“氧化”时发生反应的化学方程式为“2Fe(OH)2+H2O2=2FeOOH↓+2X”,则X的化学式。(5)、假设此过程中总体转化率为80%,若要制取232t纳米Fe3O4 , 则消耗铁泥和铁粉的总质量不可能是______。A、210t B、270t C、232t D、300t -
9、我国化工专家侯德榜发明的“联合制碱法”享誉全球。该方法以食盐为主要原料制取纯碱,其中氯化钠和碳酸钠的溶解度如表所示。
温度/℃
0
10
20
30
40
50
60
70
溶解度/g
氯化钠
35.7
35.8
36.0
36.3
36.6
37.0
37.3
37.8
碳酸钠
7.1
12.5
21.5
39.7
49.0
48.7
46.5
45.8
用如表绘制出的溶解度曲线如图所示,回答下列问题:
 (1)、t1℃对应的温度是℃。(2)、将接近饱和的氯化钠溶液转化为饱和溶液,可采用的一种方法是。(3)、40℃时,将40.0g碳酸钠加入50.0g水中,充分溶解后所得溶液中溶质与溶液的质量比为。(4)、下列有关说法正确的是______(填标号)。A、t2℃的温度范围是30~40℃ B、t3℃时,配制两种物质的饱和溶液,所需碳酸钠大于氯化钠 C、将t3℃时两种物质的饱和溶液降温至t2℃,所得溶液中溶质的质量分数相同 D、欲从含少量氯化钠杂质的碳酸钠浓溶液中分离出碳酸钠,可以采用降温结晶的方法
(1)、t1℃对应的温度是℃。(2)、将接近饱和的氯化钠溶液转化为饱和溶液,可采用的一种方法是。(3)、40℃时,将40.0g碳酸钠加入50.0g水中,充分溶解后所得溶液中溶质与溶液的质量比为。(4)、下列有关说法正确的是______(填标号)。A、t2℃的温度范围是30~40℃ B、t3℃时,配制两种物质的饱和溶液,所需碳酸钠大于氯化钠 C、将t3℃时两种物质的饱和溶液降温至t2℃,所得溶液中溶质的质量分数相同 D、欲从含少量氯化钠杂质的碳酸钠浓溶液中分离出碳酸钠,可以采用降温结晶的方法 -
10、氢气被认为是理想的清洁、高能燃料,如图为有关氢气的实验。
 (1)、实验I中制取氢气的方法说明氢气的密度比空气(填“大”或“小”)。(2)、实验II中若氢气较纯,应听到______(填标号)。A、尖锐的爆鸣声 B、声音很小 C、没有声音(3)、实验III中氢气燃烧时的化学方程式为。
(1)、实验I中制取氢气的方法说明氢气的密度比空气(填“大”或“小”)。(2)、实验II中若氢气较纯,应听到______(填标号)。A、尖锐的爆鸣声 B、声音很小 C、没有声音(3)、实验III中氢气燃烧时的化学方程式为。 -
11、将Zn和金属R(化合价为+2)的混合粉末m1g加入一定量Cu(NO3)2溶液中,反应时溶液质量的变化情况如图所示。完全反应后过滤,滤渣洗涤、干燥后称得质量为m2g。关于本实验以下说法正确的是:

①由图可知m1=m2;
②由图可知Zn、Cu、R的金属活动性由强到弱的顺序为R>Zn>Cu;
③图中a点和c点在同一高度,说明R的相对原子质量小于Cu;
④bc段发生反应的化学方程式为R+Cu(NO3)2=R(NO3)2+Cu;
⑤d点的溶液中一定含有Zn(NO3)2、R(NO3)2 , 一定不含有Cu(NO3)2;
⑥过滤所得滤渣中一定含有Cu,可能含有R。
A、②③⑤⑥ B、①③④⑤ C、①③④⑥ D、②④⑤⑥ -
12、已知A、B、C、D、E分别是初中化学所学常见物质,它们之间相互转化的关系如图所示,“→”表示物质相互之间的转化,“—”表示物质之间能发生反应,A、B、C、E分别属于不同类别的化合物,其中一种物质可改良酸性土壤。下列说法不正确的是
 A、D可用于灭火 B、A→E可能为分解反应 C、A与C、E与C之间的反应产物可能相同 D、C与A可能为中和反应
A、D可用于灭火 B、A→E可能为分解反应 C、A与C、E与C之间的反应产物可能相同 D、C与A可能为中和反应 -
13、动植物呼吸都会产生二氧化碳。下列有关二氧化碳的实验中正确的是

 A、图甲中的两个实验均能说明二氧化碳的密度比空气大 B、图乙中的实验可验证二氧化碳能与水发生反应 C、图丙实验U型管中的红墨水最终将左低右高 D、图丁实验既可探究二氧化碳能溶于水,又能说明二氧化碳能使石蕊溶液变红
A、图甲中的两个实验均能说明二氧化碳的密度比空气大 B、图乙中的实验可验证二氧化碳能与水发生反应 C、图丙实验U型管中的红墨水最终将左低右高 D、图丁实验既可探究二氧化碳能溶于水,又能说明二氧化碳能使石蕊溶液变红 -
14、在日常生活中,氮气具有广泛的用途。豆科植物可利用根瘤菌将空气中的氮气转化为氨气,从而被植物吸收。相关反应的微观示意图如图所示。下列说法正确的是
 A、该反应的基本反应类型为置换反应 B、参加反应的甲、乙的质量比为7∶3 C、反应生成的丁和戊的分子个数比为3∶4 D、反应物和生成物中共有3种氧化物
A、该反应的基本反应类型为置换反应 B、参加反应的甲、乙的质量比为7∶3 C、反应生成的丁和戊的分子个数比为3∶4 D、反应物和生成物中共有3种氧化物 -
15、劳动创造美好生活。下列与劳动项目相关的解释错误的是
选项
劳动项目
化学知识
A
用明矾处理较浑浊的天然水
明矾主要起杀菌消毒的作用
B
用活性炭除去冰箱异味
活性炭具有吸附性
C
自热米饭用生石灰做发热包
生石灰与水反应放出大量热
D
油锅着火用锅盖盖灭
利用隔绝氧气的原理灭火
A、A B、B C、C D、D -
16、某品牌饮用水的配料表如图所示。下列说法正确的是
配料表:
水
氯化钾(3~35mg/L)
硫酸镁(0.5~10mg/L)
A、氯化钾的化学式是CIK B、水中氢元素的化合价为+1价 C、硫酸镁中含有两种金属元素 D、镁离子的结构示意图为
-
17、规范的实验操作是实验成功和安全的重要保证。下列实验操作正确的是A、
 倾倒液体
B、
倾倒液体
B、 取用固体
C、
取用固体
C、 点燃酒精灯
D、
点燃酒精灯
D、 液体加热
液体加热
-
18、武汉美食享誉全国。以下制作过程中发生化学变化的是A、糯米酿酒 B、包鸡冠饺 C、刀切豆皮 D、拌热干面
-
19、构成物质的微粒有分子、原子、离子等。下列物质由离子构成的是A、
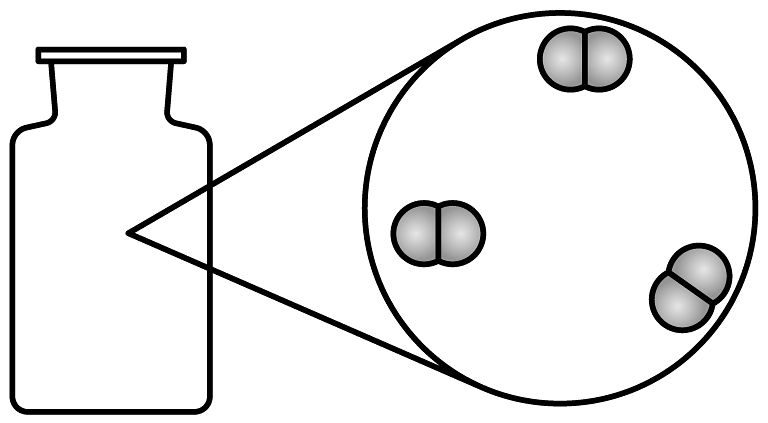 氮气
B、
氮气
B、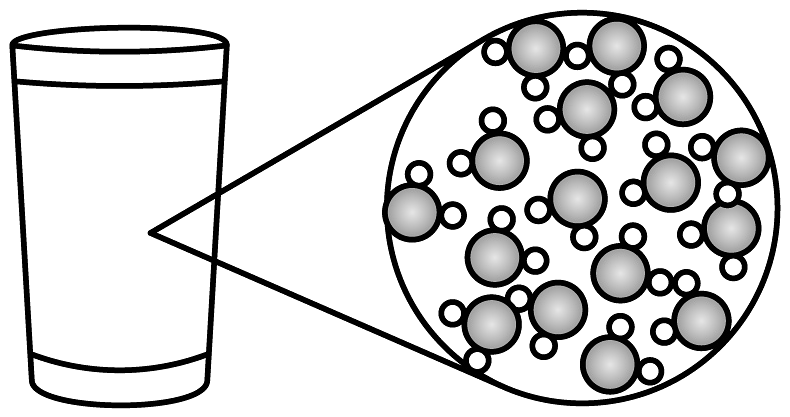 水
C、
水
C、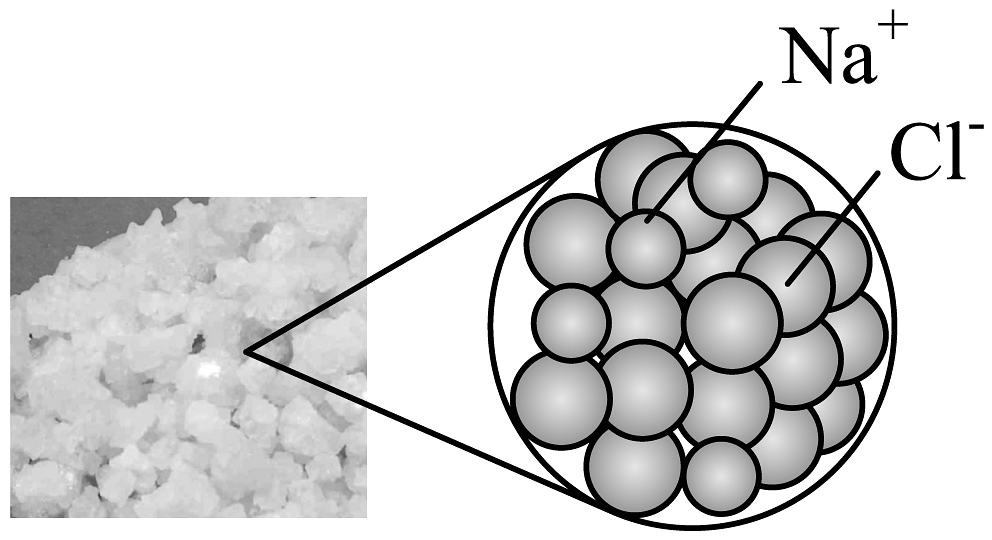 氯化钠
D、
氯化钠
D、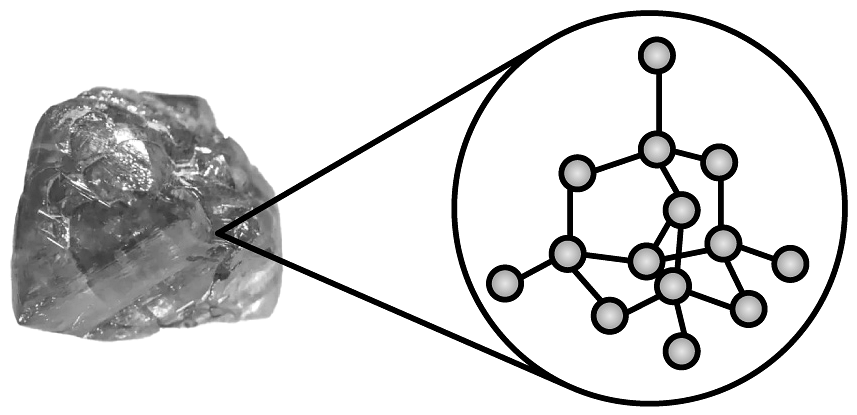 金刚石
金刚石
-
20、
自热食品中的发热包浸泡在水中即可发热。下图为某食品发热包的标签,化学兴趣小组为解密发热包展开项目式学习活动。
【品名】食品发热包 【主要成分】氧化钙、铝粉、碳酸钠 【净含量】
【使用方法】撕开塑料袋后加常温水发热 【贮存条件】存放于阴凉干燥处
【注意事项】使用时有气体产生,要远离明火,严禁在密闭场所中使用
资料1:;
资料2:发热包发热温度能保持在以上分钟;
任务一,认识发热包的主要成分
(1)氧化钙:氧化钙与水反应放出热量,写出该反应的化学方程式:。
(2)碳酸钠:在碳酸钠溶液中加入无色酚酞,可以观察到的现象是。

任务二:探究发热包可以持续发热的原理
小组同学分别取不同样品,各加水,用数字化实验获得如下曲线图(图1):
【分析得出结论】
(3)发热包可以持续发热的原理是。
任务三:自制发热包
兴趣小组将碳酸钠粉末、氯化钙粉末(稍过量)、铝粉混合均匀配成50克的自制发热包,倒入无纺布袋中后封口。小组同学将自制发热包放入烧杯,加常温水,并用温度传感器和传感器进行测量,结果如图2所示,观察有大量气泡产生。
(4)内,先降低后升高的原因是。
(5)根据检测结果,该自制发热包不能达到专用发热包的效果。小组同学提出可能是物质的质量比不恰当导致的。请通过计算说明铝粉、生石灰、碳酸钠的质量比理论上应是。
【拓展延伸】
(6)使用发热包时,撕开外包装塑料袋,检查装有发热粉的无纺布袋无破损后,放入凉水中。使用后妥善处理发热包。试推测无纺布应具备的性质(答一条即可)。
任务三:发热包使用过程中的注意事项及使用后的处理方法。
(7)使用过程中不能加入开水,请结合燃烧的条件分析可能的原因:。
(8)使用后的废液含有氢氧化钠、碳酸钠等物质,不能直接扔掉。请写出合适的处理法。