相关试卷
-
1、化学兴趣小组同学对空气中氧含量测定实验装置进行改进,回答下列有关问题:(1)、如图为书本测定空气中氧气含量的实验装置,该实验发生的化学反应的文字表达式为。
 (2)、小林同学对图四实验进行了改进,设计如图甲所示实验装置,试管容积为45mL(规格是18180mm)。实验前,打开弹簧夹,将注射器的活塞前沿从30mL刻度处推至25mL刻度处,然后松手,若活塞仍能返回至30mL刻度处,则说明。
(2)、小林同学对图四实验进行了改进,设计如图甲所示实验装置,试管容积为45mL(规格是18180mm)。实验前,打开弹簧夹,将注射器的活塞前沿从30mL刻度处推至25mL刻度处,然后松手,若活塞仍能返回至30mL刻度处,则说明。 (3)、实验开始,将少量红磷装入试管中,将30mL的注射器活塞置于15mL刻度处,松开弹簧夹,点燃酒精灯,红磷燃烧,撤去酒精灯,待试管冷却后再读取注射器活塞的数据。实验过程中,可以观察到注射器活塞移动情况是 , 注射器活塞最终停在约为mL刻度处。(4)、小刘同学又改用图乙装置使用暖宝宝贴来测定空气中氧气的含量,已知暖宝宝贴(主要成分是铁粉、木炭、食盐)的热量来源于铁粉的缓慢氧化(即铁与氧气、水发生反应生锈),实验开始前的装置如图乙所示,实验后从量筒中倒吸入集气瓶(容积为250mL)中的水的体积为47mL(铁粉生锈消耗的水忽略不计)。通过该实验测得空气样品中氧气的体积分数为(精确到0.1%)。
(3)、实验开始,将少量红磷装入试管中,将30mL的注射器活塞置于15mL刻度处,松开弹簧夹,点燃酒精灯,红磷燃烧,撤去酒精灯,待试管冷却后再读取注射器活塞的数据。实验过程中,可以观察到注射器活塞移动情况是 , 注射器活塞最终停在约为mL刻度处。(4)、小刘同学又改用图乙装置使用暖宝宝贴来测定空气中氧气的含量,已知暖宝宝贴(主要成分是铁粉、木炭、食盐)的热量来源于铁粉的缓慢氧化(即铁与氧气、水发生反应生锈),实验开始前的装置如图乙所示,实验后从量筒中倒吸入集气瓶(容积为250mL)中的水的体积为47mL(铁粉生锈消耗的水忽略不计)。通过该实验测得空气样品中氧气的体积分数为(精确到0.1%)。 -
2、A-H是初中常见的八种物质,有如下图所示关系,“→”表示一种物质能生成另一种物质,其中A是一种暗紫色固体,D能使带火星的木条复燃,F是一种最常见的液体,反应③剧烈燃烧、火星四射,并且H是一种黑色的固体,在反应②前后B的质量和化学性质均不改变。试推断:
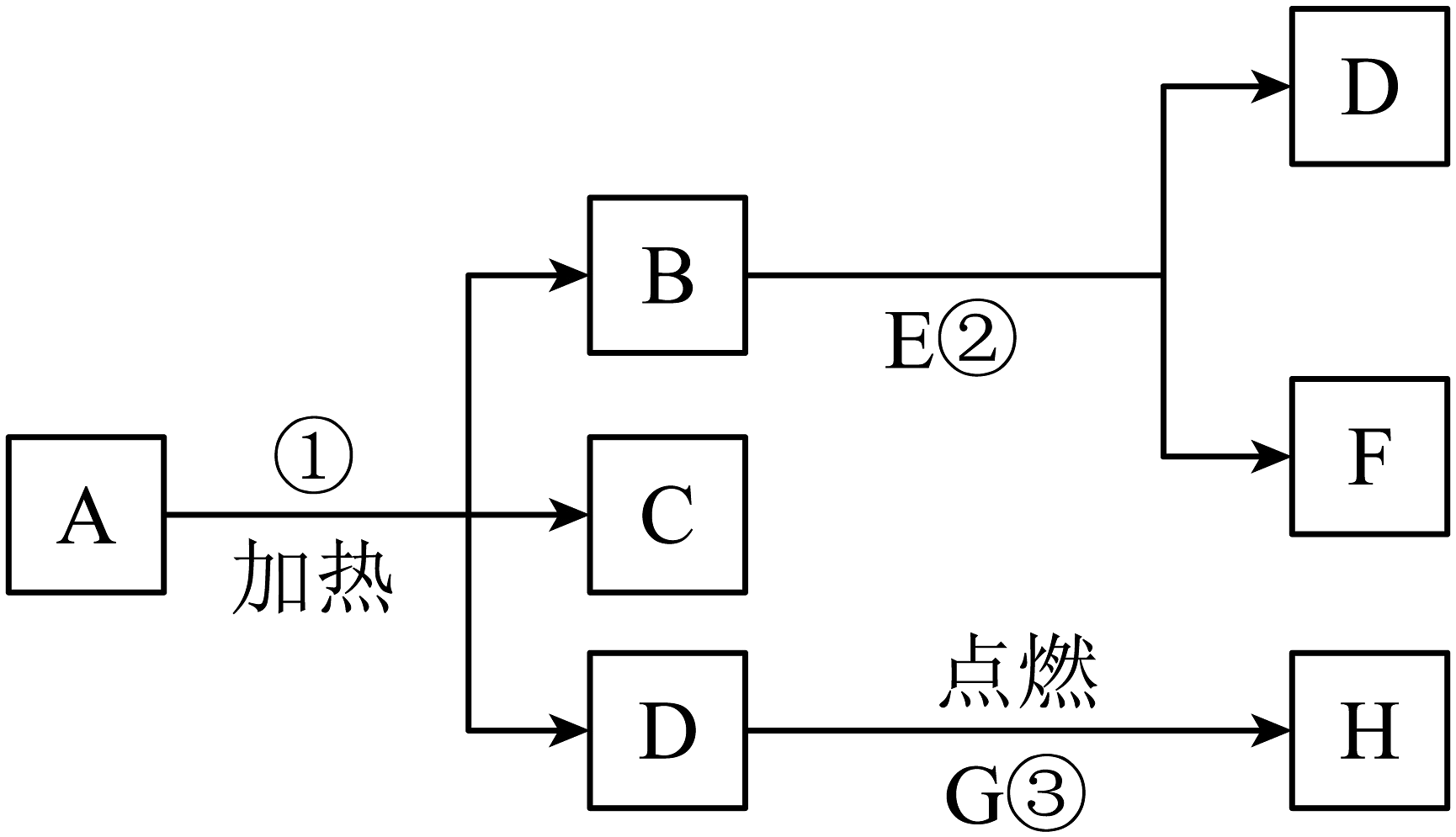 (1)、写出物质名称E:、H:。(2)、反应②中B物质的作用是。(3)、写出反应①的文字表达式。
(1)、写出物质名称E:、H:。(2)、反应②中B物质的作用是。(3)、写出反应①的文字表达式。 -
3、下图为实验室中常见的气体制备和收集装置,请回答下列问题:
 (1)、请写出仪器X的名称。(2)、用F装置进行排空气法收集氧气,将带火星的木条放在(选填“a”或“b”)处,若观察到带火星的木条复燃,则表示氧气已集满。(3)、实验室用一定质量的氯酸钾与适量的二氧化锰混合加热制取氧气,选择将装置G和H连接用排水集气法测定生成氧气的总体积,则导管的连接顺序为 , 实验过程中的说法正确的是。
(1)、请写出仪器X的名称。(2)、用F装置进行排空气法收集氧气,将带火星的木条放在(选填“a”或“b”)处,若观察到带火星的木条复燃,则表示氧气已集满。(3)、实验室用一定质量的氯酸钾与适量的二氧化锰混合加热制取氧气,选择将装置G和H连接用排水集气法测定生成氧气的总体积,则导管的连接顺序为 , 实验过程中的说法正确的是。A.要先用产生的氧气排出试管内的空气,再连接装置H
B.若试管未冷却至室温就读数,会造成测量结果偏大
C.若读数时俯视量筒读数,则测量结果偏大
(4)、检查C装置气密性的操作是:用止水夹夹住胶皮管,向长颈漏斗内加水,一段时间后,若 , 则装置气密性良好。(5)、某同学查资料得知,过氧化钠(Na2O2)是一种淡黄色固体粉末,常温下可与水反应生成氢氧化钠和氧气,如果在实验室用过氧化钠和水反应来制取并收集一瓶较纯净的氧气,同时希望控制反应的速率,应该选择的装置为(填写装置字母编号) -
4、请回答下列问题:(1)、下列物质:①氧气、②人体呼出的气体、③液氮、④空气中0.94%的稀有气体、⑤二氧化碳、⑥洁净的空气、⑦冰水混合物,其中属于纯净物的是。(2)、某同学用托盘天平称量5.5g(1g以下用游码)药品,称量时砝码和药品的位置放反了,则所称药品的质量是g。(3)、小刚量取8mL水时,仰视量筒内凹液面的最低处,导致量取的水的体积8mL(“大于”、“小于”或“等于”)。
-
5、如图所示的热现象,说法错误的是

①甲中炙热的铁水具有内能,冰冷的冰块没有内能
②图乙中冬天搓手取暖是将机械能转化为内能
③图丙中用湿毛巾冷敷降温是通过热传递的方式减小人体的内能
④丁图中能量转化与汽油机做功冲程能量转化都是机械能转化为内能
⑤甲图中冰块内能增大的方法,与图丁中硝化棉内能增大的方法相同
A、②③⑤ B、①④⑤ C、①④ D、②③ -
6、如图所示,关于分子热运动理论,以下反映微粒间有作用力的是A、
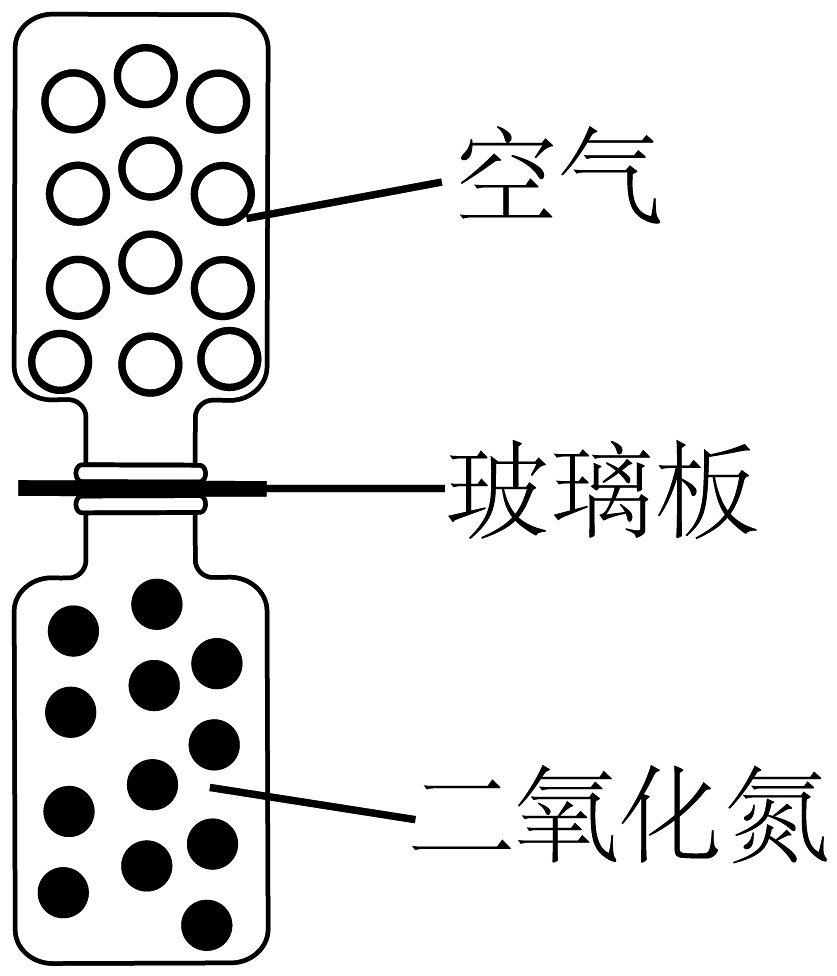 气体扩散
B、
气体扩散
B、 金块中的金原子
C、
金块中的金原子
C、 两个铅柱不分开
D、
两个铅柱不分开
D、 四溢的花香
四溢的花香
-
7、某同学在做“对人体吸入空气和呼出气体的探究”实验时,进行了如下图的实验探究。下列说法错误的是
 A、图二实验中,吸气时应打开a,关闭b;呼气时应该打开b,关闭a B、图三实验中,吸气或呼气时都不需要关闭c、d C、图三乙装置中球形干燥管的作用是防止吸气时乙中液体进入口中 D、以上三个实验均可以证明呼出气体中二氧化碳的含量比空气中二氧化碳的含量高
A、图二实验中,吸气时应打开a,关闭b;呼气时应该打开b,关闭a B、图三实验中,吸气或呼气时都不需要关闭c、d C、图三乙装置中球形干燥管的作用是防止吸气时乙中液体进入口中 D、以上三个实验均可以证明呼出气体中二氧化碳的含量比空气中二氧化碳的含量高 -
8、下列图像能正确反映对应变化关系的是
 A、加热一定质量的高锰酸钾固体 B、将足量的硫粉与一定质量的氧气在密闭装置内引燃 C、向一定量的二氧化锰中加入过氧化氢溶液 D、用等质量的氯酸钾在有、无催化剂并加热的条件下制氧气
A、加热一定质量的高锰酸钾固体 B、将足量的硫粉与一定质量的氧气在密闭装置内引燃 C、向一定量的二氧化锰中加入过氧化氢溶液 D、用等质量的氯酸钾在有、无催化剂并加热的条件下制氧气 -
9、下列选项中,仅利用选项中提供的实验仪器(规格和数量不限,药品试剂省略)能够完成相应实验的是
选项
实验仪器
相应实验
A
铁架台(带铁夹)、大试管、玻璃片、单孔橡皮塞(带导管)、水槽、酒精灯
用高锰酸钾固体制取氧气
B
研钵(带研杵)、药匙
胆矾的研碎
C
集气瓶、橡胶塞、烧杯、弹簧夹
用红磷测定空气里氧气的含量
D
铁架台(带铁夹)、大试管、玻璃片
水的沸腾
A、A B、B C、C D、D -
10、化学概念间有包含、并列、交叉等不同关系。下列选项符合如图所示关系的是
A
B
C
D

X
纯净物
化学变化
氧化反应
化合反应
Y
混合物
物理变化
化合反应
分解反应
A、A B、B C、C D、D -
11、下列有关物质燃烧的现象描述正确的是( )A、蜡烛在空气中燃烧:产生黄色火焰,生成二氧化碳和水蒸气 B、铁在氧气中燃烧:剧烈燃烧,火星四射,生成黑色固体 C、硫在氧气中燃烧:产生淡蓝色火焰,放出热量,生成有刺激性气味的气体 D、木炭在空气中燃烧:发出白光,生成气体能使澄清的石灰水变浑浊
-
12、空气是生命赖以生存的物质基础,也是人类生产活动的重要资源,下列有关空气说法错误的是A、空气中分离出的氮气化学性质不活泼,食品包装中充氮气可以防腐 B、空气中含有少量的稀有气体,它们可以制成多种用途的电光源 C、空气质量日报中空气质量指数越大、空气质量级别越高,代表空气污染越严重 D、空气主要是由氮气和氧气组成的,其中氧气的质量约占空气体积的五分之一
-
13、“84”消毒液在应对突发公共卫生事件中起到了重要作用,其主要成分为NaClO(次氯酸钠)。已知NaClO中钠为+1价,氧为-2价。试计算:(1)、NaClO中氯元素的化合价;(2)、NaClO的相对分子质量;(3)、NaClO中钠元素和氧元素的质量比;(4)、NaClO中氯元素的质量分数。
-
14、空气是人类赖以生存的必需物质之一,我们可以用以下装置粗略地测定空气中氧气的含量。
 (1)、红磷燃烧的化学方程式为 。(2)、待红磷熄灭并完全冷却后,打开止水夹,我们观察到的现象为瓶内水平面上升约五分之一,通过这一现象可说明空气中氧气约占空气体积的 。(3)、某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断不正确的是 (填序号)。
(1)、红磷燃烧的化学方程式为 。(2)、待红磷熄灭并完全冷却后,打开止水夹,我们观察到的现象为瓶内水平面上升约五分之一,通过这一现象可说明空气中氧气约占空气体积的 。(3)、某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断不正确的是 (填序号)。 A、a点时容器内氮气的体积分数小于85% B、容器内水的作用主要是降温和防止污染 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、通过此实验可测得空气中氧气的质量分数
A、a点时容器内氮气的体积分数小于85% B、容器内水的作用主要是降温和防止污染 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、通过此实验可测得空气中氧气的质量分数 -
15、水是人类宝贵的自然资源。小玲收集到一瓶浑浊的河水,她想模拟自来水厂的净水过程,制成自来水。其实验过程如图所示,请回答以下问题。
 (1)、操作①的名称是 , 该操作需要用到的玻璃仪器除了漏斗和烧杯,还有 , 若经过操作①后,所得液体C中仍有浑浊,原因可能是。(填序号)
(1)、操作①的名称是 , 该操作需要用到的玻璃仪器除了漏斗和烧杯,还有 , 若经过操作①后,所得液体C中仍有浑浊,原因可能是。(填序号)A.漏斗内的滤纸有破损
B.漏斗下端未靠在烧杯内壁
C.漏斗内液面高于滤纸的边缘
(2)、操作②过程中常用活性炭来除去一些异味和色素,这是利用活性炭的作用。(3)、爱护水资源从我做起、从点滴做起,下列做法可行的有 (填字母序号)。A、洗脸、刷牙时随时关闭水龙头 B、用洗菜、洗衣的水冲厕所 C、将生活废水直接排入河流 D、禁止使用化肥和农药 -
16、请根据如图提供的实验装置,回答有关问题。
 (1)、写出图中标有、的仪器名称: ; 。(2)、实验室利用高锰酸钾制取氧气,化学方程式为。实验开始前应先检查装置的 。安装仪器时,试管口应略向倾斜。为防止加热时粉末状物质进入导管,试管口应放一团。若用排水法收集氧气,停止加热时,应(填序号)。
(1)、写出图中标有、的仪器名称: ; 。(2)、实验室利用高锰酸钾制取氧气,化学方程式为。实验开始前应先检查装置的 。安装仪器时,试管口应略向倾斜。为防止加热时粉末状物质进入导管,试管口应放一团。若用排水法收集氧气,停止加热时,应(填序号)。A、先熄灭酒精灯,再把导管移出水面 B、先把导管移出水面,再熄灭酒精灯
(3)、实验室利用过氧化氢溶液制取并收集氧气的化学方程式为 ,选用的装置为 (填字母)。(4)、用酒精灯给试管加热时,应用酒精灯的 (填“内焰”、“外焰”或“焰心”)。(5)、已知某气体密度大于空气,难溶于水。实验室若用盛满水的F装置收集该气体,则气体应该从 (填“”或“”)通入。 -
17、学习化学离不开应用质量守恒定律分析问题。回答:(1)、化学反应前后,可能发生变化的是(填序号)。
①物质总质量 ②原子数目 ③原子质量 ④元素种类 ⑤分子种类
(2)、煤燃烧时会排放出二氧化硫、二氧化氮等污染物。在一定条件下,二氧化硫、二氧化氮能发生反应:SO2+NO2SO3+X,其中X的化学式为 。(3)、“绿色化学”的特点之一是“零排放”。一氧化碳和氢气在催化剂、高温高压条件下反应生成甲醇(CH3OH),只生成一种产物就实现“零排放”,请写出这一反应的化学方程式 。(4)、已知某燃料中碳元素的质量分数为75%,现取10g该可燃物充分点燃烧,可以生成二氧化碳的质量为 g。 -
18、无色液体A在一定条件下可分解生成B、C两种物质,其中B为无色气体,C为无色液体,将点燃的细铁丝放入B中,铁丝剧烈燃烧,火星四射,并生成一种黑色固体D,若向A物质中加入一种黑色的固体E,则A的分解速率加速,而E在反应前后本身的化学性质和质量都不改变,试回答下列问题:(1)、写出下列物质的化学符号:B;C;(2)、其中E在化学反应中起作用。(3)、铁丝在B中燃烧的化学方程式:;基本反应类型属于反应。
-
19、写出下列反应的化学方程式:(1)、硫在氧气中燃烧;(2)、氢气在氧气中燃烧;(3)、镁在空气中燃烧。
-
20、如图为电解水实验的示意图。若b试管中产生2mL气体,则a试管中产生气体约为mL。试管(填“a”或“b”)中产生的气体使燃着的木条燃烧更旺。电解水的化学反应方程式为。该实验证明水是由 组成的。
