相关试卷
-
1、下列从物质构成或者组成的角度对物质的分类错误的一项是A、由分子构成:、、 B、由原子构成:铁、铜、金 C、由离子构成:、 D、氧化物:水、锰酸钾
-
2、下列物质的用途中,主要利用其物理性质的是A、液氮用作制冷剂 B、氧气用于抢救病人 C、氮气用来作保护气 D、氢气可作燃料
-
3、空气是一种宝贵的自然资源。下列有关空气的说法正确的是A、很多物质在空气中可以燃烧,因为具有可燃性 B、空气中氮气的质量分数为78% C、空气中含量越高说明空气质量越好 D、工业上利用沸点不同分离液态空气制取氧气
-
4、“改善环境质量,推动绿色发展”是当前我市环保工作的重点。下列做法不符合这一要求的是A、建立污水处理厂,处理城市生活污水 B、提倡公交出行,减少城市雾霾 C、采用绿色化学工艺,使原料尽可能转化为产品 D、全面禁止使用农药、化肥
-
5、钙是人体必需的常量元素,每日必须摄入足够量的钙。目前市场上的补钙药剂很多,如图是某种品牌的补钙药品的部分说明书。请回答下列问题:
 (1)、碳酸钙的相对分子质量为。(2)、碳酸钙中碳元素与氧元素的质量比是。(3)、成年人体中缺钙易患。(4)、若每片钙片的质量为1g,则钙片中钙元素的质量分数为。(5)、如果按用量服用,通过服用此钙片,每天摄入钙元素的质量是g。
(1)、碳酸钙的相对分子质量为。(2)、碳酸钙中碳元素与氧元素的质量比是。(3)、成年人体中缺钙易患。(4)、若每片钙片的质量为1g,则钙片中钙元素的质量分数为。(5)、如果按用量服用,通过服用此钙片,每天摄入钙元素的质量是g。 -
6、
茶垢清洁剂可以轻松除茶垢,在茶垢清洁剂中加水,会产生大量气泡。某化学兴趣小组对茶垢清洁剂的除垢原理、使用方法等进行了系列探究。
【提出问题】茶垢清洁剂遇水产生的气体是什么?
【查阅资料】茶垢清洁剂的主要成分为过碳酸钠【 Na2CO4】; NaOH溶液可以吸收CO2。
【猜想假设】
(1)同学们对该气体的成分提出了三种猜想。
猜想1: 只有O2;
猜想2:只有;
猜想3: 既有O2又有CO2;
【实验验证】按如图1装置对猜想进行实验:

操作
现象
结论
向A中加入热水, 将生成的气体依次通过B、C, 再将带火星的木条伸入D中
观察到 B中石灰水无
现象, D中木条复燃
猜想1正确
【对比实验】兴趣小组同学改用冷水重复上述实验,观察到锥形瓶中有小气泡缓慢放出,带火星的木条没有复燃。
【交流讨论】老师提示:过碳酸钠与水反应生成碳酸钠和过氧化氢,因过氧化氢不稳定会产生具有强氧化性的活性氧,便茶垢分解、剥离、脱落。使用时加入温度稍高的水,效果更好。
(2)根据过碳酸钠的性质,保存茶垢清洁剂应注意。
(3)写出过碳酸钠与水反应生成碳酸钠和过氧化氢的文字表达式。
(4)使用冷水时木条没有复燃的原因可能是 , 导致产生的氧气浓度低。
【拓展实验】由上述实验同学们发现物质燃烧需要氧气达到一定的浓度。为了研究这个问题,同学们借助数字传感器进行实验,装置如图2. 先点燃足量红磷,氧气浓度变化如图3曲线 ab,等红磷熄灭后点燃足量白磷,氧气浓度变化如曲线 bc。

(5)写出白磷和氧气反应的文字表达式。
【实验反思】
(6)采用红磷燃烧测定空气中氧气含量的结果会偏小的原因为。
【数据处理】
(7)由图3可知红磷燃烧所需要的最低氧气浓度的取值范围是。
(8)由图3可知红磷燃烧消耗氧气的能力(填“大于”“小于”或“等于”) 白磷。
-
7、
实验是进行科学探究的重要方式,实验室制取氧气有多种方法。氧气用途广泛,生活、生产都需要氧气。
活动一:生产、生活中制氧
(1)工业上采用分离液态空气制取氧气,属于________(填“物理变化”或“化学变化”) 。
(2)为满足生产、生活对氧气的需求,市场上出现多种类型制氧机。分子筛制氧机以空气为原料,空气经过分子筛时氮气被吸附,氧气通过,获得高浓度的 O2。其微观示意图如图。请在方框中画出空气通过后的微粒图示。

活动二:实验室制氧气
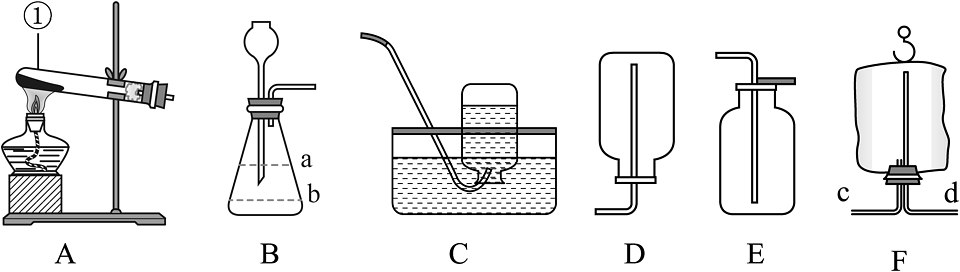
(3)写出图中标号仪器的名称:________。
(4)装置A可用于高锰酸钾制氧气,反应的文字表达式________,加热高锰酸钾制取氧气,往试管中加入高锰酸钾粉末的操作是________。
(5)用装置B制取氧气时,应先向锥形瓶中加入的固体是________,然后通过长颈漏斗向锥形瓶内添加液体至________(填“a”或“b”)处。若将装置A 中的长颈漏斗改成注射器或分液漏斗,其优点是________。
(6)收集较纯净的氧气可选择装置________(填“C” “D”或“E”),某同学利用空塑料输液袋(图F)收集制得的氧气,氧气应从________(填“c”或“d”) 端进入。
-
8、元素周期表是学习化学的重要工具,核电荷数为1~18的元素的原子结构示意图等信息如下,请回答下列问题:
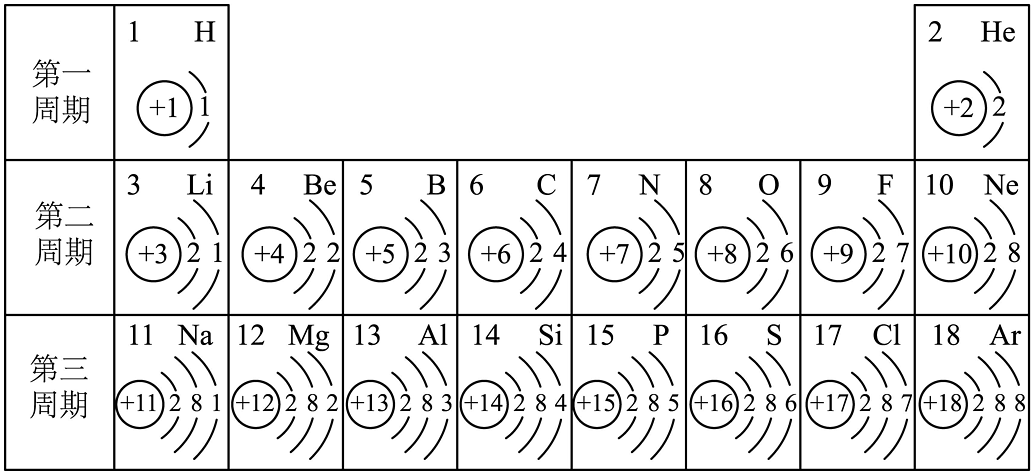 (1)、不同元素之间最本质的区别是 不同(填字母)。A、核电荷数 B、质子数 C、中子数 D、核外电子数(2)、第4号元素属于(填“金属”或“非金属”)元素。(3)、表中9号和17号元素最外层电子数相同,都易(填“得到”或“失去”) 电子。(4)、同周期元素,随着原子序数的增加,各元素原子的依次增加。(5)、原子序数为8和14的元素组成化合物的化学式为。(6)、Ne元素的化学性质 (填“活泼”或“不活泼”) , 原因是。
(1)、不同元素之间最本质的区别是 不同(填字母)。A、核电荷数 B、质子数 C、中子数 D、核外电子数(2)、第4号元素属于(填“金属”或“非金属”)元素。(3)、表中9号和17号元素最外层电子数相同,都易(填“得到”或“失去”) 电子。(4)、同周期元素,随着原子序数的增加,各元素原子的依次增加。(5)、原子序数为8和14的元素组成化合物的化学式为。(6)、Ne元素的化学性质 (填“活泼”或“不活泼”) , 原因是。 -
9、A-F六种初中常见的化学物质,有如图所示关系。其中A是一种紫红色固体,B是黑色固体,D能使带火星的木条复燃,E、F都是组成元素相同的液体。反应③中部分反应物、生成物及条件略去,请分析作答。
 (1)、物质D的化学式是。(2)、物质B的作用是。(3)、反应②的基本反应类型是反应。(4)、写出反应③的文字表达式:。(5)、下列关于反应③的说法正确的有 (选项字母序号) 。A、一定要点燃 B、一定属于氧化反应 C、一定会放热 D、一定属于化合反应
(1)、物质D的化学式是。(2)、物质B的作用是。(3)、反应②的基本反应类型是反应。(4)、写出反应③的文字表达式:。(5)、下列关于反应③的说法正确的有 (选项字母序号) 。A、一定要点燃 B、一定属于氧化反应 C、一定会放热 D、一定属于化合反应 -
10、某课外实验小组设计的电解水装置如图1 所示,已知该装置气密性良好,关闭两个弹簧夹,实验进行一段时间后,停止通电,请结合图示回答下列问题。
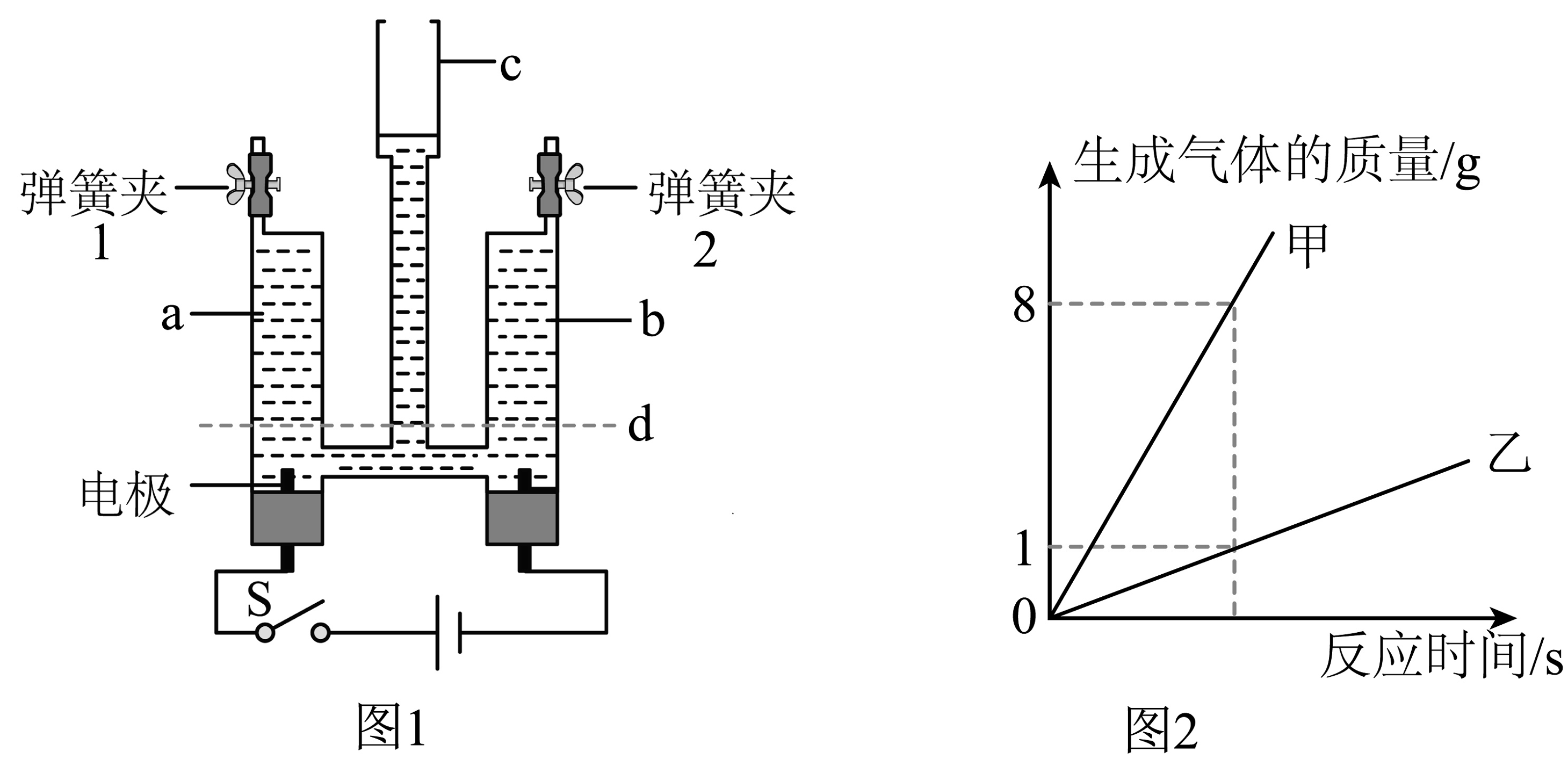 (1)、停止通电后,观察到a、b管中液面下降,但均高于d线,c管中可观察到的实验现象是 , 出现该现象的原因是。(2)、已知等温、等压下氧气的密度是氢气密度的16倍,图2为电解水时生成气体的质量与反应时间的关系图,闭合开关S后,a管中生成气体对应的曲线为(填“甲”或“乙”)。(3)、电解一段时间后,(填“a”或“b”)管内水位下降得快,其原因是。(4)、写出电解水的文字表达式:。
(1)、停止通电后,观察到a、b管中液面下降,但均高于d线,c管中可观察到的实验现象是 , 出现该现象的原因是。(2)、已知等温、等压下氧气的密度是氢气密度的16倍,图2为电解水时生成气体的质量与反应时间的关系图,闭合开关S后,a管中生成气体对应的曲线为(填“甲”或“乙”)。(3)、电解一段时间后,(填“a”或“b”)管内水位下降得快,其原因是。(4)、写出电解水的文字表达式:。 -
11、新版《生活饮用水卫生标准》 (GB5749-2022)于2023年4月1日起正式实施。新标准根据目前我国的水质现状、制水工艺现状和对人体健康的影响、增加了高氯酸盐、乙草胺、2-甲基玖醇和土臭素,删除了13项指标。(1)、标准中规定了镉、铅等的限值。这里的镉、铅指的是 (填序号)。A、原子 B、分子 C、元素 D、单质(2)、标准中规定的消毒剂有液氮、臭氧、二氧化氯和氯胺等。
①二氧化氯的化学式为、
②臭氧在消毒过程中转化为氧气,臭氧和氧气都属于(填“单质”或“化合物”):二者的组成元素相同,化学性质不同,原因是。
(3)、标准规定自来水应无异臭、异味,要达到该要求,利用活性炭的除去。长期饮用硬水对健康不利,生活中常用的方法降低水的硬度。(4)、标准规定,合格的生活饮用水以CaCO3计算总硬度限值为450 mg/L,则合格的生活饮用水中钙元素的含量不超过 mg/L。(5)、新标准中增加了乙草胺等4项指标。乙草胺是一种常用的除草剂,为避免水源被农药污染,应(填“合理”或“禁止”) 使用农药。 -
12、阅读下列短文,回答问题:
氮气
氮气是一种无色、无味的气体,密度比空气略小,难溶于水。在极低的温度下能被液化成液体,工业上储存在钢瓶中,利用液态氮和液态氧的沸点不同,工业上采用分离液态空气的方法制取氮气。在实验室中,常通过饱和的氯化铵(NH4Cl)和亚硝酸钠(NaNO2)溶液反应来制取氮气, 同时还有氯化钠和水生成。氮气常作保护气,如食品和灯泡的填充气等。液氮还可以用作深度冷冻剂,医疗上常在液氚冷冻麻醉条件下进行手术。
氮是植物生长的一种营养元素,人类能够有效利用氮气的主要途径是合成氨气、近年来、人们在竭力研究植物固氮的机理,希望能在温和条件下开发利用空气中的氮资源。
(1)、氮气的物理性质(仅写一条)(2)、氮气常用作保护气是因为。(3)、利用氮气合成的氨气中氮元素的化合价是价。(4)、写出实验室制取氮气的文字表达式为。(5)、工业上制备氮气的微观过程如图所示:
由图可知空气属于(填“纯净物”或“混合物”) 。该过程属于变化, 该变化的微观解释是。
-
13、化学用语是学习化学的重要工具,是国际通用的化学语言。请用相关化学知识填空:(1)、①地壳中含量最高的元素;
②2个硫原子;
③ 硫酸铝的化学式;
④标出氧化镁中镁元素的化合价;
(2)、①2NH3中的“2”表示;②Fe2+中的“2”表示;
(3)、化学元素与人体的健康有着密切的关系,这些元素在人体中的功能无法由别的元素来代替。①人体中含量最多的金属元素是;
②我们知道,缺碘可能会导致甲状腺疾病,人体摄入过量的碘元素容易引起病。
-
14、对下列实验指定容器中的水,其解释没有体现水的主要作用的是
A
B
C
D
实验装置

硫在氧气中燃烧

测定空气中氧气含量

铁丝在氧气中燃烧

排水法收集氧气
解释
集气瓶中的水:吸收放出的热量
量筒中的水:通过水体积的变化得出体积
集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂
集气瓶中的水:水先将集气瓶内的空气排净,后便于观察何时收集满
A、A B、B C、C D、D -
15、物质的分类是化学的基础,它有助于我们更好地理解物质的组成、结构、性质和变化规律。下列各组物质按单质、化合物、混合物的顺序排列的是A、水银、氧化镁、液态氮 B、红磷、冰水共存物、75%的酒精 C、水、生理盐水、洁净的空气 D、氢气、澄清石灰水、五氧化二磷
-
16、构建化学基本观念是学好化学的基础。下列对化学基本观念的认识中,不正确的是A、结构观:金刚石和石墨性质不同,因为它们的结构不同 B、分类观:根据组成元素的不同,可将纯净物分为单质和化合物 C、变化观:在一定条件下, H2O和 O2可以互相转化 D、微粒观:所有原子的原子核都是由质子和中子构成的
-
17、将宏观、微观以及化学符号联系在一起是化学特有的思维方式。下图是某化学反应过程的微观示意图,下列有关说法正确的是
 A、反应前后分子的个数不变 B、生成物有三种 C、反应前后汞原子和氧原子的个数不变 D、汞和氧气都由分子构成
A、反应前后分子的个数不变 B、生成物有三种 C、反应前后汞原子和氧原子的个数不变 D、汞和氧气都由分子构成 -
18、人体中化学元素含量的多少会直接影响人体健康。下列人体所缺元素与引起的健康问题关系错误的是A、缺铁会引起贫血 B、缺碘会引起龋齿 C、缺钴会引起贫血 D、缺锌会引起儿童发育不良
-
19、从《中国成语大会》到《中国诗词大会》,中国诗词文化大放异彩,很多成语、诗词中蕴含着丰富的科学道理,下列叙述错误的是A、“百炼成钢”与“沙里淘金”所涉及的变化相同 B、“一畦看韭绿,十里稻花香”是因为分子在不断地运动 C、“真金不怕火炼”说明黄金的化学性质非常稳定 D、“水滴石穿”主要是化学变化,涉及到水和空气中的二氧化碳与石头中的碳酸钙发生化学反应
-
20、A、B、C、D、E是初中化学常见的物质,A为暗紫色固体,B为黑色固体,E为无色液体,其中D能使带火星的木条复燃,将G放入D中燃烧,可观察到火星四射,生成黑色固体H。请根据图中物质间的相互转化关系,箭头表示一种物质转变为另一种物质,连线表示两物质可以反应,回答有关问题:
 (1)、D是;E是。(填化学式)(2)、反应③的化学方程式 , 为了防止集气瓶被炸裂,应在集气瓶底。(3)、写出物质D的用途:(一条即可)。
(1)、D是;E是。(填化学式)(2)、反应③的化学方程式 , 为了防止集气瓶被炸裂,应在集气瓶底。(3)、写出物质D的用途:(一条即可)。