相关试卷
-
1、填空。(1)、空气是一种宝贵的自然资源,我们要珍惜、爱护大气。
①空气属于混合物,食品包装袋中充氮气可防腐,是因为常温下氮气的化学性质。
②二氧化硫排放到空气中,降雨时易形成。
③下图是我国“祝融号”火星车测得的火星大气成分的体积百分比(体积分数)。

从图中可知,火星与地球的大气成分是不同的。下列有关说法错误的是。
A.地球和火星的大气中均含有氮气
B.地球和火星的大气中均含有二氧化碳
C.假如分别收集一瓶地球和火星上的大气,可用澄清的石灰水来鉴别
D.假如分别收集一瓶地球和火星上的大气,可用带火星的木条来鉴别
从火星大气成分可知,火星(填“适合”或“不适合”)人类居住。
④2022绿色发展国际科技创新大会的主题为“绿色低碳合作共享”。下列做法不符合这一主题的是
A.提高城市绿化面积 B.垃圾分类回收利用
C.推广使用共享单车 D.植物秸秆露天焚烧
(2)、下列物质中:①雨水;②氧气;③冰水混合物;④铁粉;⑤牛奶。属于混合物的是(填序号,以下同),属于纯净物的是。 -
2、根据空气的成分填空。(1)、酥脆饼干在空气中放置会逐渐变软,说明空气中含有。(2)、通电时,各种电光管会发出不同颜色的光,说明空气中含有。(3)、很多物质在空气中能剧烈燃烧,说明空气中含有。(4)、空气是制造氮肥的原料之一,说明空气中含有。
-
3、如图为大自然中的氧循环示意图,通过图中信息不能得出的结论是
 A、二氧化碳的含量高有利于植物光合作用 B、地球人口的增多,其呼吸和使用的燃料耗氧越来越多 C、光合作用的反应物中有二氧化碳,产物中有氧气 D、生物呼吸作用和物质的燃烧过程中都放出热量
A、二氧化碳的含量高有利于植物光合作用 B、地球人口的增多,其呼吸和使用的燃料耗氧越来越多 C、光合作用的反应物中有二氧化碳,产物中有氧气 D、生物呼吸作用和物质的燃烧过程中都放出热量 -
4、在实验室里用加热氯酸钾与二氧化锰的混合物来制取氧气,合适的实验装置是(部分夹持装置已略去)A、
 B、
B、 C、
C、 D、
D、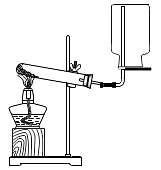
-
5、学校在举办冬季田径运动时.田径比赛发令枪打响后,产生了大量白烟,该白烟主要是A、二氧化硫 B、五氧化二磷 C、二氧化碳 D、四氧化三铁
-
6、传承了千年的手工艺品在视觉上给人以透空的感觉和艺术享受。以下铜仁的传统手工艺中涉及化学变化的是A、印江造纸
 B、碧江藤编
B、碧江藤编 C、松桃苗绣
C、松桃苗绣 D、思南花烛
D、思南花烛
-
7、我国化学电池技术全球领先,磷酸铁锂是电池的重要原料。(1)、某种锂原子的质量为 , 碳原子质量的1/12为 , 则该锂原子的相对原子质量是多少?(需写出计算过程,结果精确到0.1)(2)、在我国近代化学启蒙者徐寿与他人合译的《化学鉴原》中,许多元素的中文名称如钠、铝、钾、钙、锌等沿用至今。其中锌原子的相对原子质量是65,中子数为35,这种锌原子的质子数为。(3)、秀山新星初级中学九年级的学生可以利用周末在家做一些“家庭小实验”。想一想你们能找到日常生活中哪些物品作为化学实验仪器的代用品。
-
8、实验室常用下列装置制取氧气,请你根据所学知识回答下列问题。实验室常用如图所示装置来制取氧气:
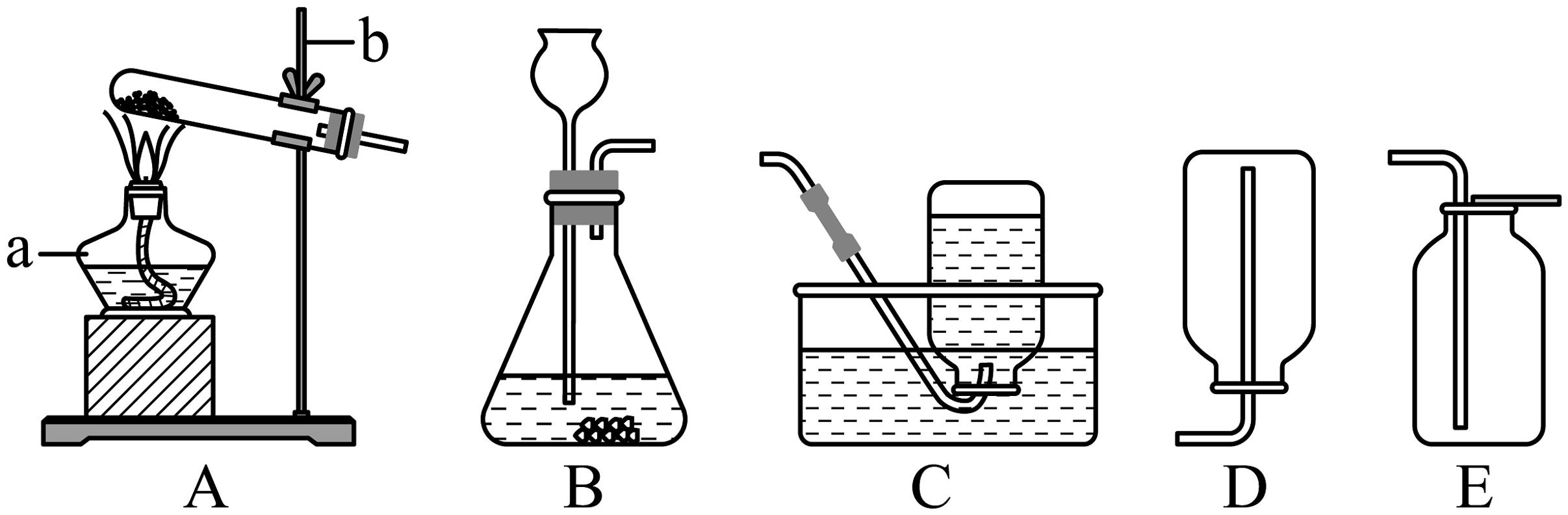 (1)、写出图中有标号仪器的名称:a;b。(2)、用过氧化氢溶液和二氧化锰制取氧气时,可选用的发生装置是(填序号),反应的符号表达式为:。(3)、用E装置收集氧气的依据是 , 检验氧气是否集满的方法是。
(1)、写出图中有标号仪器的名称:a;b。(2)、用过氧化氢溶液和二氧化锰制取氧气时,可选用的发生装置是(填序号),反应的符号表达式为:。(3)、用E装置收集氧气的依据是 , 检验氧气是否集满的方法是。 -
9、2024年5月3,嫦娥六号探测器成功发射,开启月球背面采样之旅。(1)、月球背面的水有固态和气态两种存在方式。
①气态水的分子间隔比固态水更(填“大”或“小”)。
②水由固态变为气态的过程中,分子种类(填“改变”或“未改变”),因此水的化学性质(填“改变”或“未改变”)。
(2)、科研人员曾用嫦娥五号带回的月壤证实:在一定条件下,月壤中的FeO(铁橄榄石的主要成分)分解生成(磁铁矿的主要成分)以及单质铁。①写出该反应的符号表达式。
②(填“得到”或“失去”)电子变成Fe。
-
10、用所学化学知识回答下列问题:

上图是某密闭容器中物质变化过程的微观示意图:上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是(填“Ⅰ或Ⅱ或Ⅲ”),该化学变化中一定不变的粒子是(填化学符号)。从微观角度看,化学变化的实质是。
-
11、金属镓(Ga)可用于制作半导体,镓元素在元素周期表的信息以及Ga、A、B、C、D、E的微粒结构示意图如下图所示,回答下列问题:
 (1)、镓元素位于元素周期表第周期。(2)、上图中,一共涉及种元素。(3)、E失去3个电子,形成阳离子,该离子符号为。(4)、具有相对稳定结构的是(填字母序号),Ga与E化学性质相似的原因是相同。
(1)、镓元素位于元素周期表第周期。(2)、上图中,一共涉及种元素。(3)、E失去3个电子,形成阳离子,该离子符号为。(4)、具有相对稳定结构的是(填字母序号),Ga与E化学性质相似的原因是相同。 -
12、水是生命之源,也是人类宝贵的资源,请回答下列问题:(1)、下列“水”属于纯净物的是______(填序号)。A、冰水混合物 B、蒸馏水 C、澄清石灰水 D、矿泉水(2)、在实验室为了得到净化程度最高的水,可采用的方法是。(3)、在过滤操作中需要的玻璃仪器有玻璃棒、烧杯和 , 其中玻璃棒的作用是。
-
13、用化学符号或文字填空。(1)、“高压氖灯”中的稀有气体。(2)、3个镁离子:。(3)、5Fe表示的意义是。(4)、地壳中含量最多的元素:。
-
14、下列实验现象的描述中,正确的是A、木炭在氧气中燃烧,生成有刺激性气味的气体 B、硫在氧气中燃烧,发出淡蓝色火焰 C、熄灭蜡烛会产生一缕白雾 D、铁丝在氧气中燃烧,火星四射,生成黑色固体
-
15、田昊同学对化学非常感兴趣,当他在练习使用量筒时,做了如下操作:先俯视读数量取了 18mL水,然后倒出一部分,再仰视读数为 10mL。请你判断他到底倒出了多少水A、>8mL B、<8mL C、=8mL D、无法判断
-
16、下列化学符号既能表示一种元素,又能表示一个原子,还能表示一种物质的是A、H B、He C、 D、
-
17、下列推理正确的是A、分子、原子、离子都是构成物质的微粒 B、水和过氧化氢的组成元素相同,所以它们的化学性质相同 C、催化剂在化学反应前后质量和性质都不变 D、离子带电,所以带电荷的粒子一定是离子
-
18、下列装置都可用于测定空气里氧气的含量。a、b两物质的选择正确的是
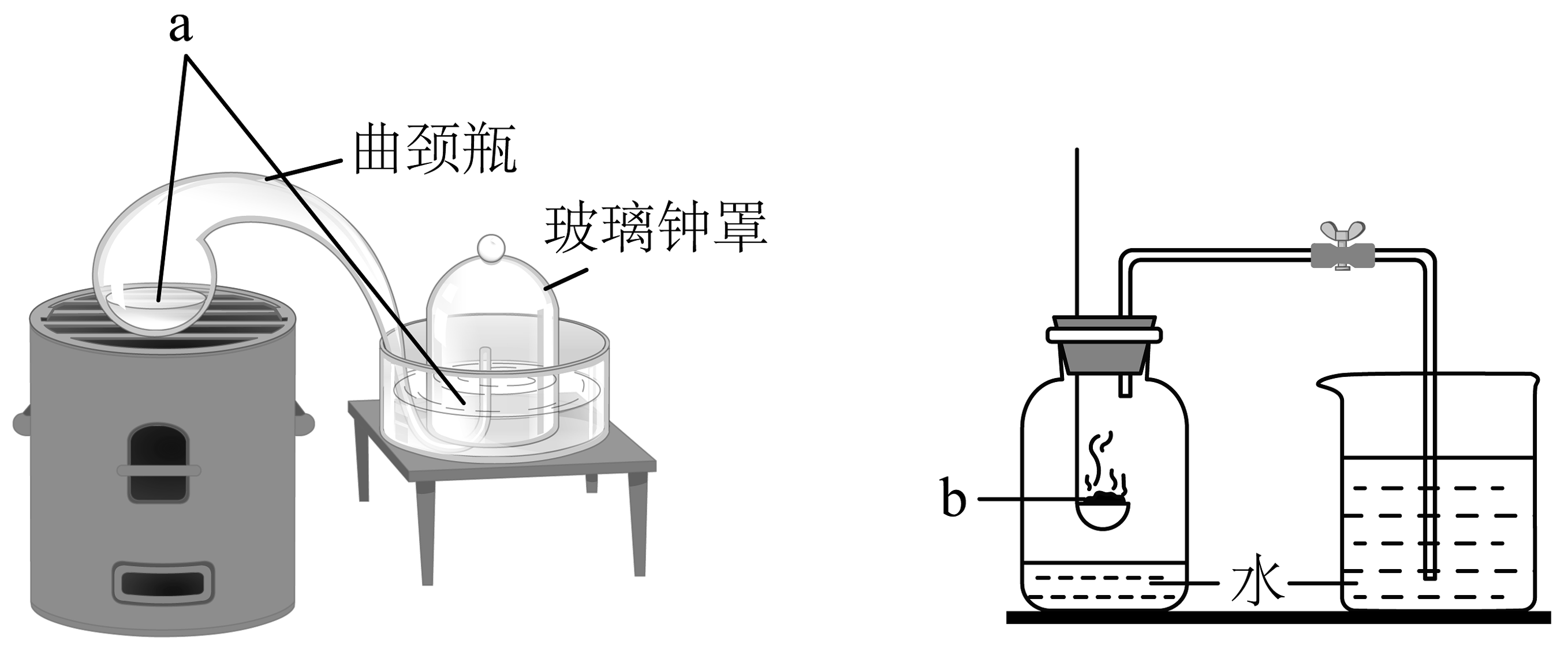 A、a是铜、b是红磷 B、a是铜、b是木炭 C、a是汞、b是红磷 D、a是汞、b是木炭
A、a是铜、b是红磷 B、a是铜、b是木炭 C、a是汞、b是红磷 D、a是汞、b是木炭 -
19、某牛奶的营养成分表如图所示。表中“钠”和“钙”指的是
营养成分表
项目 每100g
能量 309kJ
蛋白质 3.6g
脂肪 4.4g
糖类 5.0g
钠 65mg
钙 120mg
A、元素 B、分子 C、原子 D、离子 -
20、“天水麻辣烫”红遍全国,其中“甘谷辣椒”是麻辣烫的灵魂所在。辣椒中含有的辣椒碱是一种天然植物碱,其化学式为 , 试计算:(1)、的相对分子质量为;(2)、中碳、氢、氧、氮的原子个数比为;(3)、中各元素质量比为;(4)、中碳元素质量分数为;(5)、可从辣椒经过萃取得到,同时还能萃取出辣椒红素 , 试计算多少质量的与的辣椒红素的含氧量相等?