相关试卷
- 广东省清远市2016-2017学年九年级化学一模考试试卷
- 广西钦州港经济开发区2015-2016学年九年级上学期化学期末考试试卷
- 广西北海市合浦县教育局教研室2013-2014学年九年级上学期化学期末考试试卷
- 广西北海市合浦县2012-2013学年九年级上学期化学期末考试试卷
- 广东省肇庆市鼎湖中学2017-2018学年九年级上学期化学期中考试试卷
- 2016年广西钦州市中考化学试题
- 2015年广西钦州市中考化学试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西桂林市灌阳县2015-2016学年九年级上学期化学期中考试试卷
- 广西钦州地区2016-2017学年九年级化学中考模拟考试试卷
-
1、
氯化钠是生活必需品,也是重要的化工原料。
Ⅰ.古法制盐:古人用煎盐法制取食盐主要步骤有:①制卤水;②测卤水浓度;③煎卤得粗盐;④用“花水”冲洗粗盐得精品盐。
制取卤水的方法有两种:刮土淋卤:将结有盐霜的土,聚集成堆,清水浇注,卤水从堆底流出;
草木灰淋卤:将草木灰浸入海水然后晾晒至现出白光,再用海水淋之,得卤水。
(1)上述两种制取卤水的方法属于变化。
(2)卤水入锅前,以石莲子或鸡蛋投入卤中,检验卤水浓度,石莲子或者鸡蛋沉入水下的为淡卤,半飘浮的为半淡卤,浮立于水面的为成卤,其中溶质质量分数最大的是(填“淡卤”“半淡卤”或“成卤”)。
(3)以成卤入锅煎盐,有白色晶体析出。此过程制盐的原理是。
(4)经调查发现,“花水”是NaCl的饱和溶液,用“花水”冲洗粗盐而不用淡水冲洗的原因是。
Ⅱ.工业制盐:目前工业上常用真空法制备食盐,通过减压使热的海水快速蒸发而获得食盐。某同学在实验室中用溶液a(3%NaCl溶液1000g)模拟真空法制备食盐的流程(忽略物质的损耗)及氯化钠溶解度曲线如图所示:

(5)溶液a中溶质的质量为g。溶液a经减压蒸发后得到溶液b和NaCl固体xg,x的数值为。溶液b的质量溶液c的质量(填“<”“=”或“>”)。
(6)海水晒盐是借助日光和风力使水分蒸发。对比分析真空制盐,海水晒盐的优点是。
-
2、
气体制取及燃烧条件的探究。
Ⅰ.气体制取

(1)利用如图装置A实验室制取氧气的化学方程式为________,此发生装置还可用与稀盐酸和大理石制取二氧化碳的原因是________,反应的化学方程式为________。
(2)用装置B检验二氧化碳所用的试剂为________(填化学式),C收集二氧化碳并验满,此过程体现二氧化碳的性质有________。
Ⅱ.探究燃烧条件
小组同学利用如图1装置探究燃烧的条件,点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入集气瓶中,使铝盒中的白磷立即燃烧。如图2是瓶中①二氧化碳和②氧气的含量随时间变化的图像。

(3)导致铝盒中白磷燃烧的原因是________。
(4)结合实验探究及图像变化分析合理的是
A. 时蜡烛燃烧消耗氧气,含量减少,生成二氧化碳,含量增加 B. 时蜡烛熄灭,说明瓶内氧气被消耗完 C. 二氧化碳含量升高是因为白磷燃烧,继续消耗瓶内的氧气,气体总量减少 D. 之后白磷燃烧没有生成二氧化碳,气体含量不变 (5)由图像中曲线②分析可知:不同可燃物在空气中燃烧除需要氧气、温度达到其着火点之外,还需要考虑的因素是________。
-
3、我国是较早冶铁的国家。《天工开物》中记载了古法炼铁的过程,图1是古法炼铁的工艺流程。请结合图文信息,分析思考解决问题。
 (1)、利用水碓将块状铁矿石捣成粉末,这样做的目的是。(2)、高温炉中为了提高炉温,使燃料充分燃烧进行的操作是 , 写出高温炉内(赤铁矿)炼铁的反应原理:。(3)、每年因铁制品锈蚀,导致大量金属资源的浪费。为探究其锈蚀原因设计如图2实验,简述还需补充的实验操作是。
(1)、利用水碓将块状铁矿石捣成粉末,这样做的目的是。(2)、高温炉中为了提高炉温,使燃料充分燃烧进行的操作是 , 写出高温炉内(赤铁矿)炼铁的反应原理:。(3)、每年因铁制品锈蚀,导致大量金属资源的浪费。为探究其锈蚀原因设计如图2实验,简述还需补充的实验操作是。 -
4、阅读科普短文,回答下列问题:
钠是一种银白色金属,质软,密度为 , 化学性质很活泼。钠遇水立即发生剧烈反应,生成氢氧化钠和氢气。实验室,通常将钠保存在煤油中。金属钠在工业上具有非常重要的用途。利用钠的强还原性,在一定条件下可将钛、锆等稀有金属从其氯化物中置换出来。工业上通常采用电解熔融氯化钠的方式制取单质钠。阅读分析,解决问题:
(1)、在实验室,将钠保存在煤油中的原因是。(2)、写出钠和水发生反应的化学方程式。(3)、工业上制取金属钠的原理属于(填基本反应类型)。(4)、金属镁与钠位于元素周期表中同一周期,其化学性质却没有钠活泼,请从原子结构分析其原因是。(5)、铜的活泼性不如钠,但也能置换出硝酸银中的银。如图是铜丝插入硝酸银溶液中反应的微观示意图,写出发生反应的化学方程式 , 从微观粒子变化的角度分析该反应的实质是。
-
5、生活中处处有化学。(1)、空气是人类生活生产的重要资源,在晨跑时供给呼吸的气体是 , 能闻到树木花草的清香是因为。(2)、在食盐中加入适量的碘酸钾补充碘元素。碘酸钾中碘元素的化合价 , 从化学式中可以获得的信息是(写一条即可)。(3)、我国海域埋藏着大量的可燃冰(主要含有甲烷水合物),其燃烧过程中伴随的能量转化是将化学能转化为 , 你还知道的新能源有(写一种即可)。(4)、制造太阳能电池板需要铝合金片,铝合金能加工成箔片是利用了金属的性。铝制品在空气中不易被腐蚀的原因是。
-
6、向盛有10g49%稀硫酸的烧杯中加入的铁粉,充分反应后有固体残留,时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。分析错误的是
 A、 B、c点时,溶液中有两种溶质 C、d点固体,加入盐酸一定没有气泡产生 D、a点,溶液中溶质的总质量逐渐增大
A、 B、c点时,溶液中有两种溶质 C、d点固体,加入盐酸一定没有气泡产生 D、a点,溶液中溶质的总质量逐渐增大 -
7、设计实验方案,分析实验原理,解决实验问题,是化学独特的学科思想。下列实验设计能达到相应实验目的的是A、证明蜡烛中含碳元素
 B、验证质量守恒定律
B、验证质量守恒定律 C、探究不同溶剂中物质溶解性大小
C、探究不同溶剂中物质溶解性大小 D、除去CO2中的CO气体
D、除去CO2中的CO气体
-
8、下列实验现象中,能够验证质量守恒定律的是A、铜在空气中加热固体质量增加 B、硫酸铜溶液与铁反应,总质量不变 C、碳酸钠粉末与稀盐酸反应后质量减轻 D、镁条在空气中燃烧后,生成物质质量增加
-
9、2024年7月30日,中国运动员孙颖莎和王楚钦获得了巴黎奥运会乒乓球混双冠军,乒乓球的主要成分是聚酯纤维,是由对苯二甲酸和乙二醇为原料制成的,对其原料对苯二甲酸的说法不正确的是A、对苯二甲酸属于化合物 B、对苯二甲酸的相对分子质量为166g C、对苯二甲酸中碳、氢、氧元素的质量比为 D、每个对苯二甲酸分子由8个碳原子、6个氢原子和4个氧原子构成
-
10、下列劳动实践,不是直接利用所给物质性质的是
选项
劳动实践
化学知识
A
用氮气防止食品腐烂
氮气的化学性质不活泼
B
用竹炭去除汽车内的异味
竹炭具有吸附性
C
用二氧化碳生产碳酸饮料
二氧化碳是无色、无臭的气体
D
用石墨制造受电弓滑板
石墨的熔点高,具有优良的导电性能
A、A B、B C、C D、D -
11、某同学学习了粗盐提纯的实验操作过程,用到了以下基本实验操作。其中正确的是A、称取固体
 B、溶解固体
B、溶解固体 C、过滤
C、过滤 D、蒸发
D、蒸发
-
12、春节,《哪吒之魔童闹海》的爆火,让越界影城成为贵阳新的名片。下列做法能体现贵阳这座文明城市的行为是A、商铺污水任意排放 B、市区尽量开车出行 C、菜市场大量使用塑料袋 D、生活垃圾分类回收
-
13、通常条件下,能与反应生成。若在某纳米催化剂表面将与接触,可发生如图所示反应。下列说法不正确的是
 A、雨水pH略小于7是由于空气中的与反应生成了 B、在纳米催化剂表面,与参加反应的质量比为44:45 C、对比上述两个反应可知,相同反应物在不同条件下,产物可能不同 D、纳米催化剂表面所发生的反应有利于实现的资源化利用
A、雨水pH略小于7是由于空气中的与反应生成了 B、在纳米催化剂表面,与参加反应的质量比为44:45 C、对比上述两个反应可知,相同反应物在不同条件下,产物可能不同 D、纳米催化剂表面所发生的反应有利于实现的资源化利用 -
14、二氧化锰因其广泛的应用备受关注。(1)、科学家以石墨烯为基体,以二氧化锰为增强体,制得了一种新型材料,用于能源存储领域,这种新材料属于材料(填“金属”或“合成”或“复合”)(2)、某研究小组采用下图装置通过焙烧制取 , 发生反应的化学方程式为:。
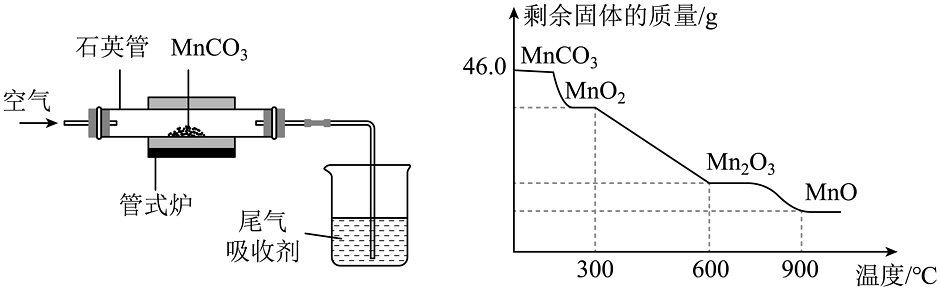
①实验过程中,石英管内剩余固体的质量和成分随温度的变化如上图所示,则焙烧制取应该控制反应的温度不高于℃。
②从加热到的过程中,剩余固体中锰元素的质量分数逐渐增大的原因是。
③若把反应温度控制在 , 充分反应后管内剩余固体的质量为g。
④实验室用二氧化锰催化过氧化氢制取氧气,现有100g溶质质量分数为6.8%的过氧化氢溶液,理论上可以制得氧气的质量为多少?(写出计算过程)
-
15、金属可用于制造货币、合金结构钢、氢化催化剂等。粗制氧化镍主要含氧化镍(NiO),以及少量氧化钴(CoO)和氧化铁,以粗制氧化镍为原料制备纯镍的流程如下:
 (1)、反应③中,黑色单质的化学式是。(2)、反应①的基本反应类型为;反应②中生石灰在生活中的用途是。(3)、从安全操作角度要求反应⑤开始前用氮气充分吹扫设备内部,其目的是 , 该反应中氧化镍转化为金属镍的化学方程式是。(4)、查阅资料,获知部分物质的沸点:
(1)、反应③中,黑色单质的化学式是。(2)、反应①的基本反应类型为;反应②中生石灰在生活中的用途是。(3)、从安全操作角度要求反应⑤开始前用氮气充分吹扫设备内部,其目的是 , 该反应中氧化镍转化为金属镍的化学方程式是。(4)、查阅资料,获知部分物质的沸点:物质
沸点/℃
43
106
52
从、和的混合物中用蒸馏的方法提应选择的温度(T)范围是。
(5)、以上生产流程中循环使用的物质是(填化学式)。(6)、若将制得的放入溶液中,没有观察到明显现象,证明的金属活动性比(选填“强”或“弱”)。 -
16、
高锰酸钾是一种重要的化工产品,它不仅是初中化学制取氧气的重要原料,在医疗上还可以用于杀菌消炎。某兴趣小组对高锰酸钾展开项目式学习。
【任务一】的物理性质
为探究高锰酸钾的溶解性,小组同学设计了如图实验。
 (1)在两支试管中分别加入一小粒高锰酸钾,如图操作,观察到A试管中固体全部溶解,溶液呈________色;B试管中固体不溶解,汽油不变色。说明物质的溶解性与________有关。(2)溶液中含有、两种离子,小明认为溶液的颜色是的颜色,请你结合所学知识回答判断依据是________。
(1)在两支试管中分别加入一小粒高锰酸钾,如图操作,观察到A试管中固体全部溶解,溶液呈________色;B试管中固体不溶解,汽油不变色。说明物质的溶解性与________有关。(2)溶液中含有、两种离子,小明认为溶液的颜色是的颜色,请你结合所学知识回答判断依据是________。【任务二】的化学性质
(3)高锰酸钾常用于实验室中制取氧气,写出该反应的化学方程式:________。【查阅资料】维生素C能与反应,使溶液褪色。
【实验探究】探究果蔬汁中维生素C含量
【进行实验】用几种果蔬汁完成实验,记录观察到溶液恰好褪色时所需果蔬汁的用量。
实验操作
果蔬汁
果蔬汁用量/滴

鲜榨的白菜汁
12
鲜榨的橙汁
8
鲜榨的西红柿汁
11
加热后冷却至室温的新鲜西红柿汁
14
放置12小时的西红柿汁
15
【实验结论】
(4)由上述实验现象可知,影响果蔬汁中维生素C含量的因素有________。(5)下列做法中能提高上述果汁中维生素C含量测量的准确度的有______(多选,填字母序号)。A. 减小高锰酸钾溶液质量分数 B. 用管口较小的滴管 C. 将等量的果蔬汁用等量的水稀释 D. 增加高锰酸钾溶液体积 (6)日常饮用橙汁时需要注意的事项是________(写一点)。(7)继续实验,发现猕猴桃汁中维生素C含量大于西红柿汁中维生素C含量,其实验方案为按照图中实验装置,逐滴滴加猕猴桃汁,________。 -
17、
Ⅰ、二氧化碳的制取
根据下列仪器装置,回答问题。

(1)写出标号仪器的名称:a.________。
(2)实验室制备和收集可从中选用________(填字母),其制取的反应原理为________(用化学方程式表示);装置是在装置基础上的改进,其优点是________。固体试剂放在多孔塑料板的________(填“上方”或“下方”)。

Ⅱ、自制简易发生器并应用于水草中,化学小组制成发生器甲与装置乙(用于除杂和观察气泡)组合为给鱼池中水草提供(如图丙)。
(3)下列分析正确的是______(多选,选填字母)。
A. 甲中的b口应与乙中的c口相连接 B. 为除去中混有的醋酸,可以是溶液 C. 可根据中冒出气泡的快慢来调节甲中的流速调节器 D. 甲装置无法用于实验室制氧气 (4)小组同学用自制的发生器连接气体细化器向水草缸中通入气体,实践效果很好。使用气体细化器的作用是________。
(5)发生器的不合理使用会影响缸中鱼类生存,请写出使用时的一条注意事项________。
-
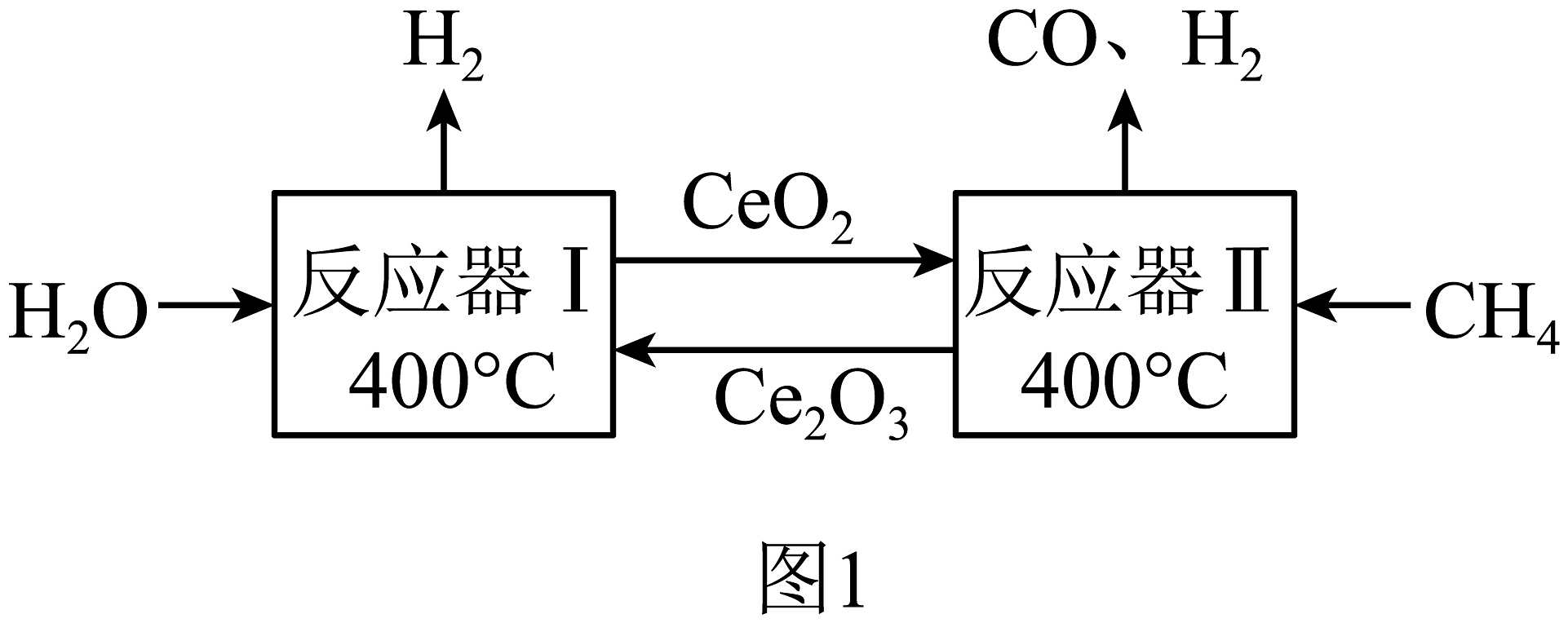
18、氢能是面向未来的清洁能源。目前,我国制氢方式有化石能源制氢[包括煤制氢和天然气制氢(如图1)]、电解水制氢和乙醇裂解制氢等。其中化石能源制氢技术比较成熟,是当前主要的制氢方式。利用可再生能源电解水制氢是理想的制氢技术,其技术主要有三种,分别是光催化、光电催化和光-电催化耦合制氢,对应的氢能转化率如下表。
可再生能源制氢技术
氢能转化率
光催化
不足5%
光电催化
不足5%
光-电催化耦合
70%以上
氢合金,中国科学家提出的“液态阳光”也是一种氢气储运是氢能产业链的重要环节。除了储储氢载体。“液态阳光”是指利用太阳能等可再生能源制取绿色氢气,结合二氧化碳加氢技术制备以甲醇为代表的液态燃料。甲醇相比氢气、甲烷等燃料,它可以直接使用现有的以汽油为主的燃料储存运输设施,降低了氢气储存和运输的成本。
“液态阳光”关键技术之一是合成甲醇时催化剂的选择。工业生产选择催化剂时,催化剂的稳定性是重要参考条件之一,中国科学家突破了这一关键技术(部分成果如图2),推动了“液态阳光”生产从实验室走向应用。事实证明,这是切实可行的碳中和路径。请依据上述材料及所学化学知识,回答下列问题。
 (1)、氢气作为清洁能源具有的优点之一是对环境无污染。当前我国最主要的制氢方式是。(2)、结合图1,试分析天然气制氢工艺存在的不足是。(3)、如表所示,光-电催化耦合技术优势之一是。(4)、煤经过加工合成的甲醇,(填“(能”或“不能”)称作“液态阳光”。(5)、“液态阳光”技术使用的可以用溶液捕获,其化学方程式为。(6)、根据图2中信息,选出合成“液态阳光”最适合的催化剂______(填标号)。A、 B、 C、(240℃) D、(7)、除“液态阳光”技术外,下列哪些措施也能促进碳中和______(填标号)。A、大力推广使用脱硫煤 B、加快煤的开采与使用,发展经济 C、大规模开采可燃冰作为新能源 D、研发新工艺将二氧化碳转化为化工产品
(1)、氢气作为清洁能源具有的优点之一是对环境无污染。当前我国最主要的制氢方式是。(2)、结合图1,试分析天然气制氢工艺存在的不足是。(3)、如表所示,光-电催化耦合技术优势之一是。(4)、煤经过加工合成的甲醇,(填“(能”或“不能”)称作“液态阳光”。(5)、“液态阳光”技术使用的可以用溶液捕获,其化学方程式为。(6)、根据图2中信息,选出合成“液态阳光”最适合的催化剂______(填标号)。A、 B、 C、(240℃) D、(7)、除“液态阳光”技术外,下列哪些措施也能促进碳中和______(填标号)。A、大力推广使用脱硫煤 B、加快煤的开采与使用,发展经济 C、大规模开采可燃冰作为新能源 D、研发新工艺将二氧化碳转化为化工产品 -
19、
当化学与浪漫相遇,你喜欢哪一款?广东肇庆中学第五届科技创新节中,化学科组推出的“晶绽创想-创意晶体制作”和“蚀韵铜华-铜板腐蚀画制作”两大特色活动作品惊艳亮相。
(1)1.科技创新节开幕式,我校化学科组的老师们用“掌中火焰”点燃了同学们对科学的热情。老师在开始表演前需将手用水浸湿,再用火机点燃手上肥皂泡中的丁烷气体使其燃烧,丁烷在手掌中燃烧不会灼伤皮肤是因为。

2.晶绽创想-创意晶体制作
选取原料:制备硫酸铜晶体使用的原料是胆矾()
(2)制备硫酸铜饱和溶液:在烧杯中加入一定量的蒸馏水并用酒精灯进行加热,逐步往其中加入胆矾,用玻璃棒搅拌至不再溶解。其中玻璃棒的作用是。
(3)制备硫酸铜晶体模型:小肇和小钟购入了一批形状各异的假花、塑料制成的玩偶以及铜丝编制的工艺品,将其浸泡在硫酸铜的饱和溶液中经过一系列操作,即可制备出精致的硫酸铜晶体模型。
①根据右侧表格中不同温度下硫酸铜在水中的溶解度,其中“一系列操作”中包含(填“降温结晶”或“蒸发结晶”)。
温度/℃
20
40
60
80
100
溶解度/g
20.7
28.5
40
55
75.4
②所购买的材料中不能是金属铁制成的,原因是(用化学方程式解释)。
硫酸铜晶体的保存:硫酸铜晶体()不能放在阳光下暴晒,否则失去晶体中的结晶水变成白色的无水硫酸铜。
3.蚀韵铜华-铜板腐蚀画制作

铜板腐蚀画的制作的原理是:利用蚀刻液与裸露金属之间发生反应,最终形成精美图案。
(4)小玥用一块铜板制作金属字画,她先用马克笔在铜板上写上“端溪书院”字,接着将铜板没入试剂a中,取出后出现银白底紫红色的“端溪书院”字。则试剂a为(填序号)。
①稀硫酸 ②硝酸银溶液 ③硫酸铜溶液
(5)保护字画。为防止金属画锈蚀。可采取的措施有(填序号)
①表面涂一层保护膜 ②放置在潮湿地方 ③常用汗手直接取用
-
20、某同学在学习溶液时进行了如图1和如图2所示实验探究,图一温度为20℃,此时硝酸钾溶解度为31.6g。下列说法正确的是
 A、图1实验①②③烧杯中的溶液,一定属于饱和溶液的是②③ B、图1实验烧杯②中硝酸钾溶质质量分数是烧杯①中的2倍 C、图1实验烧杯②溶液中溶质、溶剂质量之比为 D、图2实验,一木块悬挂在饱和硝酸钾溶液中,在恒温条件下向烧杯内溶液中加入氯化钠固体,则弹簧称读数将变小
A、图1实验①②③烧杯中的溶液,一定属于饱和溶液的是②③ B、图1实验烧杯②中硝酸钾溶质质量分数是烧杯①中的2倍 C、图1实验烧杯②溶液中溶质、溶剂质量之比为 D、图2实验,一木块悬挂在饱和硝酸钾溶液中,在恒温条件下向烧杯内溶液中加入氯化钠固体,则弹簧称读数将变小