相关试卷
-
1、“碳达峰”“碳中和”“低碳”成为网络热词,其相关内容是二氧化碳导致的温室效应。二氧化碳的转化和利用成为一个重要的研究课题。回答下列问题:(1)、乙烯是一种重要的化工原料,利用和为原料可生产乙烯。已知相关热化学方程式如下:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
①反应Ⅳ: 。
②在某种催化剂的作用下,在容积为2.0L的恒容密闭容器中充入和 , 体系中主要发生上述反应Ⅰ和反应Ⅳ两个竞争反应。反应进行时测得两种烃的物质的量随温度的变化如下图所示,该催化剂在840℃时主要选择(填“反应Ⅰ”或“反应Ⅳ”);520℃时,内用氢气表示反应Ⅳ的平均反应速率(用含t的代数式表示)。
 (2)、多聚胺[
(2)、多聚胺[ ]可捕捉环境中的 , 然后将其转化为甲醇,反应机理如下图所示:
]可捕捉环境中的 , 然后将其转化为甲醇,反应机理如下图所示:
该反应机理中,多聚胺的作用是 , 该反应机理的总反应的化学方程式是。
(3)、碳酸二甲酯(DMC)为一种非常重要的有机化工原料,华东理工大学以镁粉为催化剂,通过甲醇与反应成功制备了DMC:。①上述反应达到平衡时,其他条件不变,向恒压密闭容器中充入少量 , 甲醇的平衡转化率(填“增大”“减小”或“不变”)。
②温度为TK,按投料比向恒容密闭容器中投料,平衡前后气体的压强之比为6:5,测得平衡体系中气体的压强为 , 则TK时该反应的压强平衡常数(以分压表示,分压=总压×物质的量分数)。
-
2、中国科学家在淀粉人工光合成方面取得重大突破性进展,该实验方法首先将CO2催化还原为CH3OH。已知CO2催化加氢的主要反应有:
①CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1
②CO2(g)+H2(g)CO(g)+H2O(g) △H2=+41.2kJ•mol-1
其他条件不变,在相同时间内温度对CO2催化加氢的影响如图。下列说法不正确的是( )

已知:CH3OH的选择性=×100%
A、增大有利于提高CO2的平衡转化率 B、使用催化剂,能降低反应的活化能,增大活化分子百分数 C、其他条件不变,增大压强,有利于反应向生成CH3OH的方向进行 D、220~240℃,升高温度,对反应②速率的影响比对反应①的小 -
3、资源化利用是实现“碳中和”的重要途径,与氢气反应制的一种催化机理如图所示,总反应为>0,下列说法正确的是( )
 A、过程Ⅲ中,没有化学键断裂 B、在Ni催化作用下产生·H为吸热过程 C、反应中释放出 D、总反应中,反应物的键能之和小于生成物的键能之和
A、过程Ⅲ中,没有化学键断裂 B、在Ni催化作用下产生·H为吸热过程 C、反应中释放出 D、总反应中,反应物的键能之和小于生成物的键能之和 -
4、25 ℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与lg X的变化关系如图所示。已知:lg X=lg或lg , 下列叙述正确的是( )
 A、曲线m表示pH与lg的变化关系 B、当溶液呈中性时,c(Na+)=c()+2c() C、Ka1(H2CO3)的数量级为10-6 D、滴加过程中,保持不变
A、曲线m表示pH与lg的变化关系 B、当溶液呈中性时,c(Na+)=c()+2c() C、Ka1(H2CO3)的数量级为10-6 D、滴加过程中,保持不变 -
5、750℃时,NH3和O2发生以下两个反应:
①4NH3(g)+5O2(g)4NO(g)+6H2O(g) △H1
②4NH3(g)+3O2(g)2N2(g)+6H2O(g) △H2
下列说法正确的是( )
A、反应①的平衡常数可表示为K1= B、反应②的△S<0 C、反应①中每生成2molNO,转移电子数约为6.02×1024 D、反应②的△H2=2E(N≡N)+12E(H-O)-12E(N-H)-3E(O=O) -
6、下列装置或操作能达到目的的是( )




A.排出酸式滴定管中的气泡
B.灼烧海带
C.比较CH3COOH的Ka和H2CO3的Ka1大小
D.测定氯水的pH
A、A B、B C、C D、D -
7、已知常温下,几种物质的电离平衡常数,下列说法正确的是( )
弱酸
HCOOH(甲酸)
HClO
K(25℃)
A、向NaClO溶液中通入足量SO2能提高次氯酸的浓度 B、向HCOONa(甲酸钠)溶液中滴加过量CO2: C、向Na2CO3溶液中通入过量Cl2: D、向NaClO溶液中通入少量CO2: -
8、某化学小组同学研究温度和压强对反应速率和化学平衡的影响,测得化学反应中C的百分含量(C%)与时间(t)、温度(T)、压强(p)的关系如图所示。下列说法正确的是( )
 A、、 B、、 C、、 D、、
A、、 B、、 C、、 D、、 -
9、下列装置能达到设计目的的是( )




①
②
③
④
A、装置①用于深埋在潮湿的中性土壤中钢管的防腐 B、装置②用于深浸在海水中的钢闸门的防腐 C、装置③用于模拟铁制品表面镀铜 D、装置④用于构成锌铜原电池 -
10、已知反应: , 其他相关数据如下表:
化学键
1化学键断裂时吸收的能量/
x
498
803
464
下列说法正确的是( )
A、反应物的总能量小于生成物的总能量 B、的燃烧热是806.0 C、 D、断开氧氧键形成1氧原子需要放出能量249 -
11、化学电源在日常生活和高科技领域中都有广泛应用。下列说法错误的是( )
 A、甲:反应时盐桥中的阳离子移向溶液 B、乙:正极的电极反应式为 C、丙:锌筒作负极,发生氧化反应,锌筒会变薄 D、丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
A、甲:反应时盐桥中的阳离子移向溶液 B、乙:正极的电极反应式为 C、丙:锌筒作负极,发生氧化反应,锌筒会变薄 D、丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降 -
12、已知强酸强碱的稀溶液发生中和反应时,生成放热 , 若用与的稀溶液反应,每完全中和时放热 , 下列说法正确的是( )A、是一种强酸 B、浓硫酸与反应生成时放热为 C、表示与中和反应的热化学方程式为: D、电离的热化学方程式为:
-
13、科研人员发现利用低温固体质子导体作电解质,催化合成 , 与传统的热催化合成氨相比,催化效率较高。其合成原理如图甲所示,其他条件不变,电源电压改变与生成速率的关系如图乙所示,下列说法不正确的是( )
 A、是该合成氨装置的阳极 B、电极出口混合气可能含有、、 C、若H2的进出口流量差为22.4 L/min(标准状况),则固体质子导体中的流速为1 mol/min D、当电压高于1.2V时,随电压升高,在阴极放电生成的速率加快
A、是该合成氨装置的阳极 B、电极出口混合气可能含有、、 C、若H2的进出口流量差为22.4 L/min(标准状况),则固体质子导体中的流速为1 mol/min D、当电压高于1.2V时,随电压升高,在阴极放电生成的速率加快 -
14、已知碘化氢分解吸热,分以下两步完成:2HI(g)→H2(g)+2I•(g);2I•(g)→I2(g),下列图像最符合上述反应历程的是( )A、
 B、
B、 C、
C、 D、
D、
-
15、中华优秀传统文化涉及了很多化学知识,下列有关说法错误的是( )A、《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金。”强水为强电解质 B、《神农本草经》中“石胆……能化铁为铜、成金银”描述的是湿法炼铜 C、刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水为熵增的过程 D、“火树银花合,星桥铁锁开”中涉及化学能转化为热能和光能
-
16、CH3OH是一种绿色燃料,工业上制备CH3OH发生如下反应:
反应1:CO2(g) + 3H2(g)CH3OH(g) + H2O(g) ΔH1= - 49.5 kJ/mol
反应2:CO2(g) + H2(g)CO(g) + H2O(g) ΔH2= + 41.2 kJ/mol
(1)、n起始(CO2)∶n起始(H2) = 1∶3的混合气体发生反应1和反应2,恒压分别为1 MPa、3 MPa、5 MPa下反应达到平衡时CO2的转化率(α)(曲线a、b、c)以及3 MPa时生成CH3OH、CO选择性(S)的变化如图1所示(选择性为目标产物在总产物中的比率)。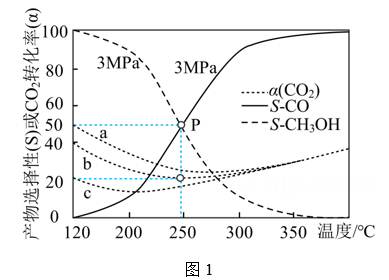
①随着温度升高,a、b、c三条曲线接近重合的原因是。
②250℃时,反应2的平衡常数K=。
(2)、恒压下,n起始(CO2)∶n起始(H2) = 1∶3的混合气体以一定流速通入分子筛膜反应器(如图2所示),反应相同时间,测得甲醇选择性随温度的变化如图3所示。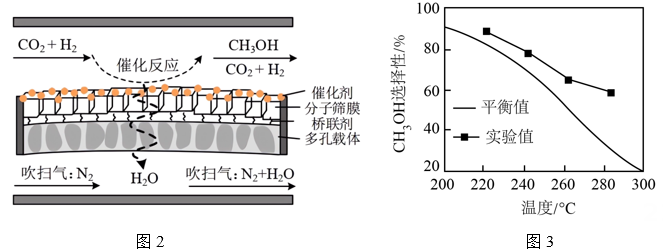
①随温度升高,平衡时CH3OH选择性降低的原因是。
②温度相同时,CH3OH选择性的实验值高于平衡值,其原因可能是。
③分子筛膜反应器可提高CO2转化率的原因是。
(3)、某甲醇燃料电池的工作原理如图4所示。负极的电极反应式为。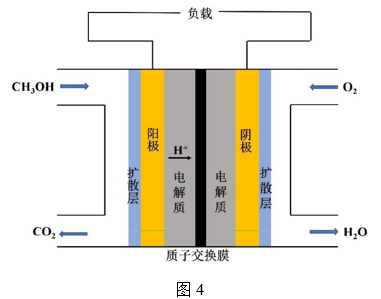
-
17、实验室以废铜屑(杂质为CuO、Al2O3、Fe2O3、FeO和SiO2)为原料制取碱式碳酸铜[aCu(OH)2·bCuCO3]的流程如下:
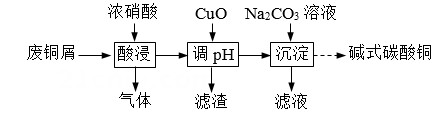
已知部分氢氧化物开始沉淀与沉淀完全的pH见下表:
物质
Fe(OH)3
Fe(OH)2
Cu(OH)2
Al(OH)3
开始沉淀pH
1.9
6.5
4.2
3.4
沉淀完全pH
3.2
9.7
6.7
4.0
(1)、按图1所示的装置加料后进行“酸浸”操作。①提高Cu元素浸出速率的方法还有。

②与使用图2所示漏斗相比,使用漏斗Y的优点是。
(2)、“调pH”的合理范围是。(3)、“沉淀”时需要对混合物加热至70℃但又不宜过高,理由是。(4)、可采用滴定法、热重分析法分别对碱式碳酸铜的组成进行分析。①滴定法涉及的部分反应:
2Cu2+ + 4I- =2CuI↓+ I2、I2 + 2Na2S2O3 = 2NaI + Na2S4O6。
请补充完整测定碱式碳酸铜中Cu元素含量的实验方案:准确称取一定质量的碱式碳酸铜样品,在搅拌下分批加入稀硫酸直至固体完全溶解,配成100mL溶液。;根据数据计算Cu元素含量(须使用的试剂:KI溶液、0.1000 mol/L Na2S2O3溶液、淀粉溶液)。
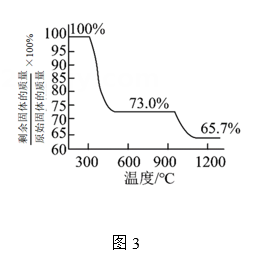
②测得碱式碳酸铜的热重分析结果如图3所示,已知当剩余固体质量与原始固体质量的比值为65.7%时固体呈砖红色,则计算可知(保留3位有效数字)。 -
18、莫西赛利(化合物E)是一种治疗脑血管疾病的药物,其合成路线如下:
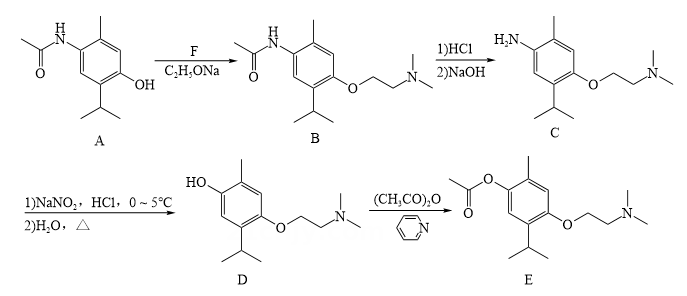 (1)、
(1)、 中N原子的杂化类型为。 (2)、D→E的反应类型为。(3)、F的分子式为C4H10ClN。A→B步骤中C2H5ONa的作用为。(4)、写出同时符合下列条件的化合物A的同分异构体的结构简式。
中N原子的杂化类型为。 (2)、D→E的反应类型为。(3)、F的分子式为C4H10ClN。A→B步骤中C2H5ONa的作用为。(4)、写出同时符合下列条件的化合物A的同分异构体的结构简式。①含有苯环的α-氨基酸;
②1H-NMR谱表明分子中共有6种不同化学环境的氢原子。
(5)、已知R-NH2易被氧化。写出以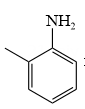 和H2C=CH2为原料合成
和H2C=CH2为原料合成 的合成线路(有机溶剂和无机试剂任选)。
的合成线路(有机溶剂和无机试剂任选)。 -
19、铈可用作优良的环保材料。现以氟碳铈矿(CeFCO3 , 含Fe2O3、FeO等杂质)为原料制备碳酸铈的工艺流程如下:
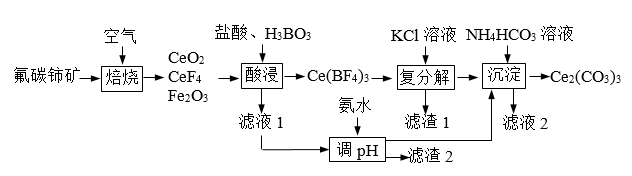 (1)、在对流空气氧化炉中比暴露在空气中“焙烧”大大缩短氧化时间的原因是。(2)、“酸浸”步骤中产生的气体为 (化学式)。(3)、“滤液1”中c(Ce3+)=0.1 mol·L-1 , 用氨水调pH的范围是(已知Ksp[Fe(OH)3] = 8×10-38;Ksp[Ce(OH)3] = 1×10-22;lg2 = 0.3,离子浓度小于1×10-5mol/L认为沉淀完全)。(4)、“沉淀”步骤中发生反应的离子方程式为。(5)、Ce2(CO3)3在空气中焙烧可制得CeO2 , 该反应的化学方程式为。(6)、用过量铝粉还原CeO2即可得Ce。铝粉必须过量的原因是:使CeO2充分被还原,提高Ce的产率;。
(1)、在对流空气氧化炉中比暴露在空气中“焙烧”大大缩短氧化时间的原因是。(2)、“酸浸”步骤中产生的气体为 (化学式)。(3)、“滤液1”中c(Ce3+)=0.1 mol·L-1 , 用氨水调pH的范围是(已知Ksp[Fe(OH)3] = 8×10-38;Ksp[Ce(OH)3] = 1×10-22;lg2 = 0.3,离子浓度小于1×10-5mol/L认为沉淀完全)。(4)、“沉淀”步骤中发生反应的离子方程式为。(5)、Ce2(CO3)3在空气中焙烧可制得CeO2 , 该反应的化学方程式为。(6)、用过量铝粉还原CeO2即可得Ce。铝粉必须过量的原因是:使CeO2充分被还原,提高Ce的产率;。 -
20、一定条件下,将一定量的CO2和H2混合气体通过装有催化剂的反应器可得到甲烷。
已知:Ⅰ.CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41 kJ·mol-l
Ⅱ.CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH=-165 kJ·mol-1
在两种不同催化剂作用下反应相同时间,CO2转化率和生成CH4选择性随温度变化关
系如图所示(CH4选择性=×100%)。

下列说法不正确的是( )
A、反应CO(g)+3H2(g)=CH4(g)+H2O(g)的ΔH=-206 kJ·mol-1 B、在280 ℃条件下反应制取CH4 , 选择催化剂A的效果较好 C、260~300 ℃间,使用催化剂A或B,升高温度时CH4的产率都增大 D、M点可能是该温度下的平衡点,延长反应时间,不一定能提高CH4的产率