相关试卷
-
1、某同学设计如图的原电池装置,下列说法错误的是
 A、Fe极为电池的负极 B、一段时间后溶液质量增加 C、电子从C极经导线流向Fe极 D、C极的电极反应式为Fe3++e-=Fe2+
A、Fe极为电池的负极 B、一段时间后溶液质量增加 C、电子从C极经导线流向Fe极 D、C极的电极反应式为Fe3++e-=Fe2+ -
2、下列说法错误的是A、在常温下可以发生的反应不一定是放热反应 B、中和反应中,反应物的总能量比生成物的总能量低 C、通过调控反应条件,可以提高该反应进行的程度 D、化学反应中能量变化的大小与反应物的质量多少有关
-
3、下列实验能达到目的的是


A.检验Na2O2与水反应生成的气体
B.测定氯水的pH


C.制备纯净的Fe(OH)2
D.配制一定物质的量浓度的硫酸溶液
A、A B、B C、C D、D -
4、劳动创造美好生活。下列关于劳动项目与所涉及的化学知识不相符的是
选项
劳动项目
化学知识
A
工人用铁制容器来盛装浓硝酸
铁与浓硝酸不反应
B
模具须充分干燥后才注入熔融钢水
铁与H2O高温下会反应
C
用HF的水溶液溶蚀玻璃生产磨砂玻璃
HF可与SiO2发生反应
D
用铁片、石墨棒和柠檬为原料制作水果电池
铁与柠檬中酸性物质发生反应
A、A B、B C、C D、D -
5、下列关于硫及其化合物的叙述,正确的是A、SO2能使酸性KMnO4溶液褪色,说明SO2有漂白性 B、浓硫酸能与木炭在加热时反应,说明浓硫酸有强氧化性 C、硫与铜在加热时反应生成硫化铜,说明硫有还原性 D、葡萄酒中添加二氧化硫,说明二氧化硫可以在食品中大量使用
-
6、下列关于氮及其化合物的说法正确的是A、可用向上排空气法收集NO B、NO在与水的反应中只做氧化剂 C、将大气中游离态的氮转化为氮的化合物的过程叫氮的固定 D、N2的化学性质稳定,任何情况下不与O2、H2等发生反应
-
7、用NA表示阿伏加德罗常数的值,下列说法正确的是A、28gCO所含的分子数目为NA B、1mol镁原子中含有的电子数为2NA C、标准状况下,22.4LH2O含有的分子数目为NA D、1mol/LNa2SO4溶液中含有的Na+的数目为2NA
-
8、材料是人类赖以生存和发展的基础,下列有关说法错误的是A、传统的无机非金属材料多为硅酸盐材料 B、高纯硅广泛应用于信息技术和新能源技术领域 C、碳纳米材料在信息,医药等领域有广阔应用前景 D、SiC因含有离子键而具有优异的高温抗氧化性能
-
9、下列关于分离或提纯说法正确的是A、可用饱和食盐水溶液除去Cl2中的HCl气体 B、粗盐提纯过程中涉及过滤、蒸发、分液等操作 C、除去SO2中的H2S,可以通入酸性高锰酸钾溶液洗气 D、除去FeCl2溶液中少量FeCl3 , 可以加入足量铜粉后过滤
-
10、柳州市博物馆是我市的文化名片。下列有关展品主要成分为合金的是A、兽骨
 B、青铜器
B、青铜器 C、纸张
C、纸张 D、青花瓷
D、青花瓷
-
11、“碳中和”是指二氧化碳的排放总量和减少总量相当。下列有关说法错误的是A、植树造林,可降低空气中二氧化碳含量 B、大量排放二氧化碳气体会形成酸雨 C、研发太阳能、氢能等新能源,可以构建绿色低碳的能源体系 D、我国科学家实现从二氧化碳到淀粉的全合成,有助于实现“碳中和”
-
12、利用下列装置进行相关实验,能达到实验目的的是
A
B
C
D




比较的热稳定性
除中的杂质
观察钾的焰色试验
沉淀的过滤
A、A B、B C、C D、D -
13、下列有关钠及其化合物的说法正确的是A、电解饱和食盐水可制取金属钠 B、钠着火时使用泡沫灭火器灭火 C、钠燃烧生成氧化钠 D、焰色式验,火焰呈黄色,说明含有钠元素
-
14、2023年9月23日第19届亚运会在杭州盛大开幕!开幕式上主火炬首次使用废碳再生的绿色燃料甲醇 , 从物质类别来看,关于甲醇说法正确的是A、属于有机物 B、属于碱 C、属于氧化物 D、属于混合物
-
15、下列实验操作不合理的是A、
 切割金属钠
B、
切割金属钠
B、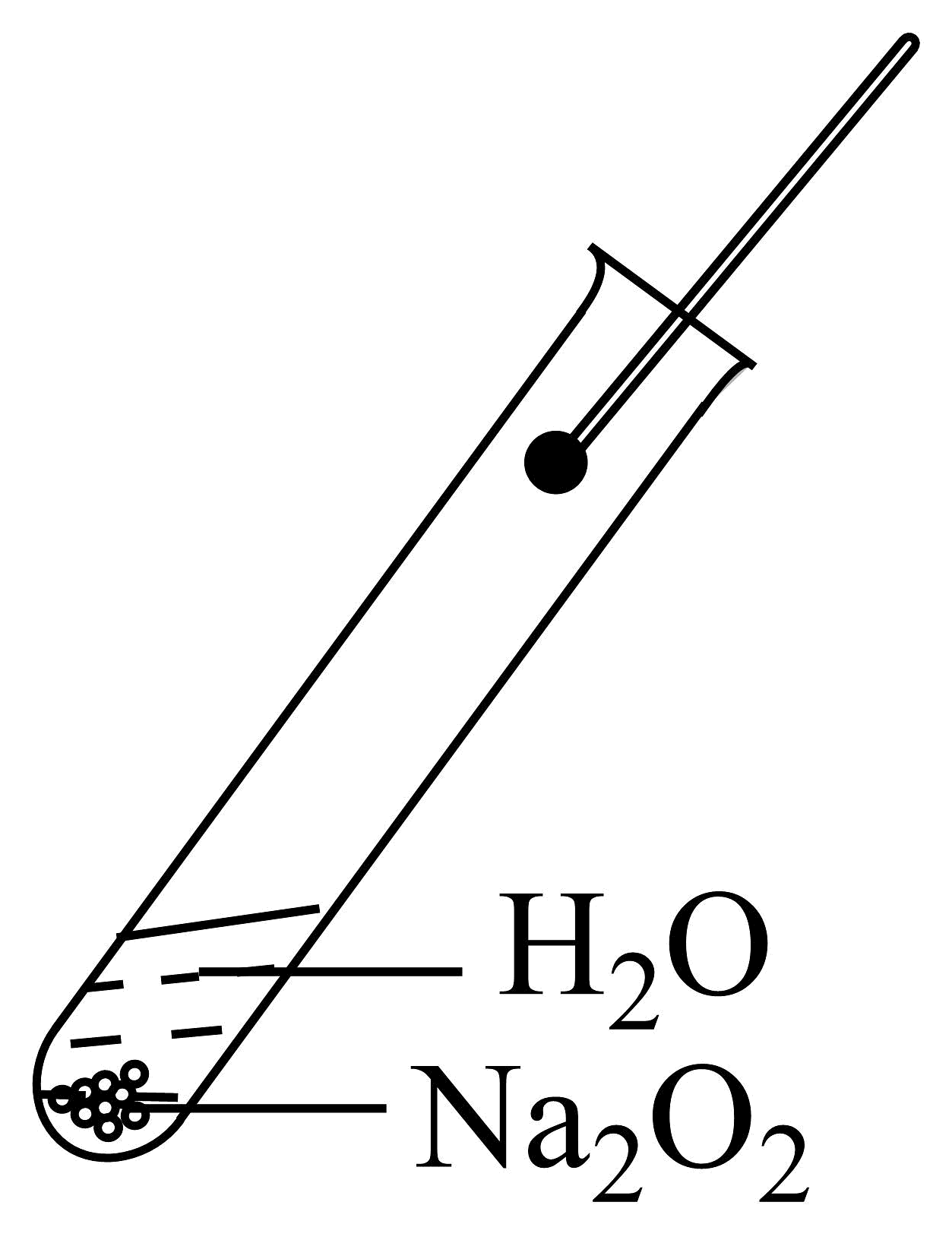 过氧化钠与水反应
C、
过氧化钠与水反应
C、 铜丝在氯气中燃烧
D、
铜丝在氯气中燃烧
D、 收集
收集
-
16、实验室欲配制的溶液.下列操作及误差分析正确的是A、用托盘天平称取固体 B、定容时俯视容量瓶刻度线,所得溶液浓度偏高 C、加水时不慎超过了刻度线,用胶头滴管直接吸出多余液体 D、使用容量瓶时,容量瓶内残留有少量水分,所得溶液浓度偏低
-
17、有机物G的合成流程图如图:


已知:
 (1)、化合物D中官能团的名称 , A生成B的反应类型为。(2)、B与C反应生成D的化学方程式为。(3)、G的核磁共振氢谱共有组吸收峰。(4)、某烃的分子式为 , 能使溴水和酸性溶液褪色,分子结构中所有的碳原子在一个平面上,该有机物的名称(系统命名法);该烃与A(填“是”或“不是”)同系物。(5)、流程中物质B的同分异构体有种(不考虑顺反异构)。
(1)、化合物D中官能团的名称 , A生成B的反应类型为。(2)、B与C反应生成D的化学方程式为。(3)、G的核磁共振氢谱共有组吸收峰。(4)、某烃的分子式为 , 能使溴水和酸性溶液褪色,分子结构中所有的碳原子在一个平面上,该有机物的名称(系统命名法);该烃与A(填“是”或“不是”)同系物。(5)、流程中物质B的同分异构体有种(不考虑顺反异构)。 -
18、科学家预测21世纪中叶将进入“氢能经济”时代,许多化合物或合金都是具有广阔应用前景的储氢材料。(1)、基态Li原子核外电子有种不同的运动状态,占据最高能级电子的电子云轮廓图形状为。(2)、咔唑(
 )的沸点比芴(
)的沸点比芴( )高的主要原因是。 (3)、(氨硼烷,熔点104℃)与(写出一种烃类分子)互为等电子体,中B的杂化轨道类型为。(4)、一种储氢合金的晶胞结构如图所示。在晶胞中Cu原子处于面心,Au原子处于顶点位置。该晶体中,存在的化学键为。实现储氢功能时,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为。已知该晶胞的晶胞参数为anm,阿伏加德罗常数值为 , 则密度ρ为(用和a的代数式表示)
)高的主要原因是。 (3)、(氨硼烷,熔点104℃)与(写出一种烃类分子)互为等电子体,中B的杂化轨道类型为。(4)、一种储氢合金的晶胞结构如图所示。在晶胞中Cu原子处于面心,Au原子处于顶点位置。该晶体中,存在的化学键为。实现储氢功能时,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中心(如图),若所有四面体空隙都填满,该晶体储氢后的化学式为。已知该晶胞的晶胞参数为anm,阿伏加德罗常数值为 , 则密度ρ为(用和a的代数式表示)
-
19、
实验小组制备 , 并探究其性质。
Ⅰ.制备

(1)仪器a的名称是;气体b是空气的组成成分,其化学式为。
(2)为检验B中制得 , 甲进行以下实验:
序号
试管
操作
现象
①
2mLB中溶液
加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液
不变蓝
②
2mLB中溶液
滴加几滴溶液至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液
变蓝
③
2mL
滴加几滴溶液至pH=5,加2mL0.1mol/LKI溶液,滴加几滴淀粉溶液
不变蓝
乙认为上述3组实验无法证明B中一定含 , 理由是B溶液中可能还有(填离子符号)干扰。
Ⅱ.探究的性质
装置
操作
现象

取10mL1mol/L溶液于试剂瓶中,加入几滴溶液酸化,再加入10mL1mol/L溶液,迅速塞上橡胶塞,缓缓通入足量
ⅰ.溶液迅速变为棕色
ⅱ.溶液逐渐变浅,有无色气泡产生,溶液上方为浅红棕色
ⅲ.最终形成棕褐色溶液
资料:ⅰ.在溶液中呈棕色。
ⅱ.在溶液中不稳定,易分解产生NO和气体。
(3)溶液迅速变为棕色的原因是;现象ⅱ中无色气泡变为浅红棕色的化学方程式是。
(4)最终棕褐色溶液的成分是 , 测得装置中混合溶液体积为20mL,设计如下实验测定其组成。
资料:①充分反应后,全部转化为。
②为无色离子。

加掩蔽剂KF的目的是(掩蔽的颜色除外)。由上述数据可知中x=(用含、的代数式表示)。
-
20、常温下,用的NaOH溶液滴定20.00mL等浓度的某酸HX,滴定曲线如图所示。下列说法正确的是
 A、HX为强酸 B、c点溶液中: C、需用甲基橙作指示剂 D、d点溶液中:
A、HX为强酸 B、c点溶液中: C、需用甲基橙作指示剂 D、d点溶液中: