相关试卷
-
1、快速阅读下列材料,判断说法错误的一项是
Nature Chemistry在2025年发表的新型水系锌-碘电池研究引发关注。该电池正极采用的碳纳米管复合电极具备特殊的表面电荷分布,能对不同离子产生差异化的静电作用,进而精准调控离子在电极表面的吸附与反应活性。电池以含的水溶液为电解质溶液,充放电过程涉及、与之间复杂的转化,锌电极发生的溶解与沉积。放电时总反应为 , 正极存在副反应(未配平),且副反应程度与电极-电解液界面的电场强度、离子浓度梯度密切相关。碳纳米管复合电极对离子的吸附符合Langmuir吸附等温式: , 其中是吸附量,是饱和吸附量,为吸附平衡常数,为离子浓度。
A、放电时,正极发生的副反应的电极方程为: B、放电时,不论和消耗的速率之比如何变化,电路中每转移电子,负极减小的质量总是 C、若用铅酸蓄电池给该电池充电,电极应当与碳纳米管复合电极相接 D、碳纳米管复合电极对的吸附程度随着浓度的增大而线性增大 -
2、纳米碗是一种奇特的碗状共轭体系。高温条件下,可以由分子经过连续5步氢抽提和闭环脱氢反应生成。其中第一步反应的反应机理和能量变化如下。下列说法错误的是
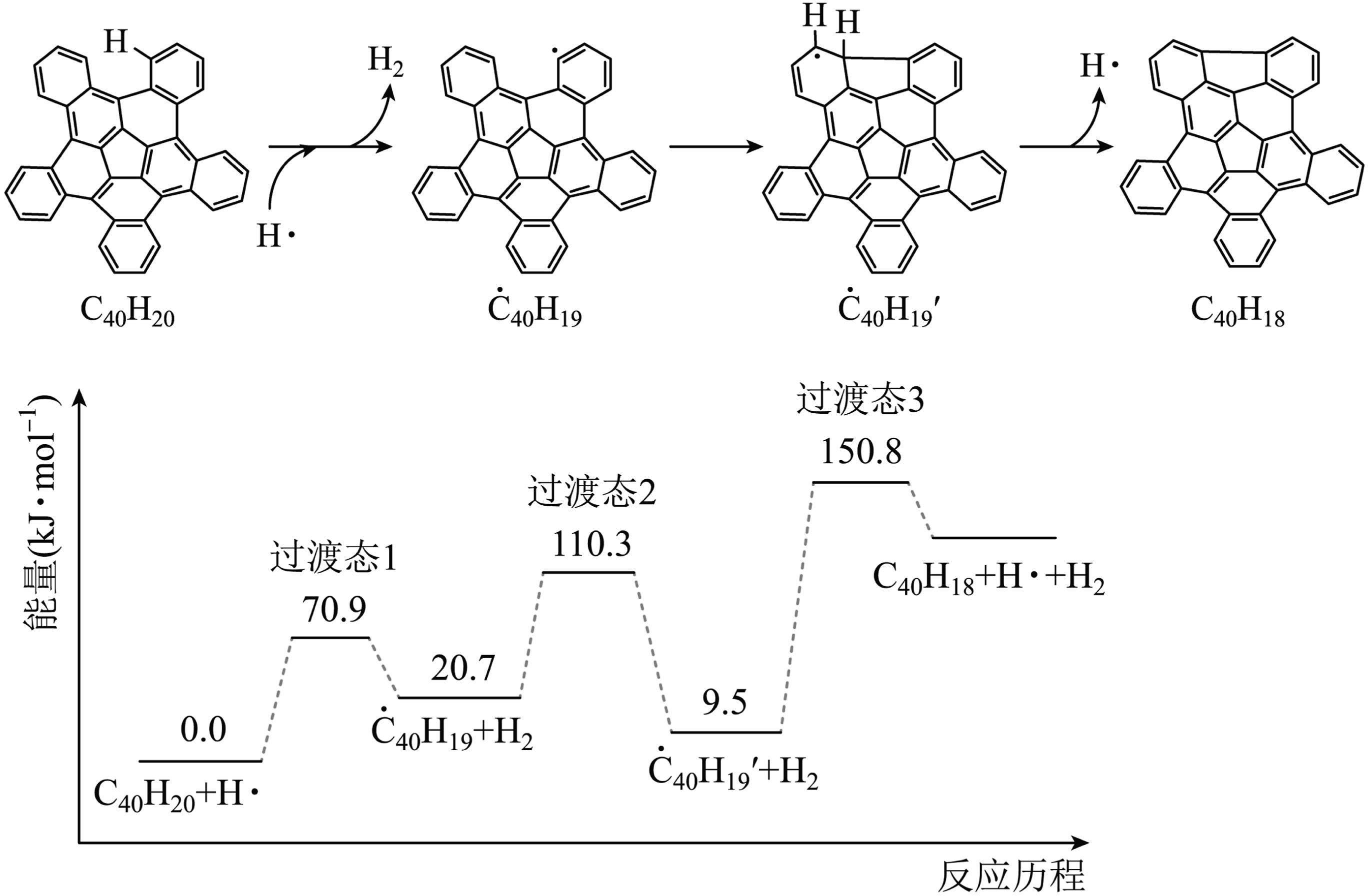 A、该反应共有3个基元反应,其中决速步反应为第三步 B、纳米碗中五元环结构的数目为5 C、反应过程中生成了具有手性异构的中间产物 D、生成的五步反应,每步反应的焓变近似相等
A、该反应共有3个基元反应,其中决速步反应为第三步 B、纳米碗中五元环结构的数目为5 C、反应过程中生成了具有手性异构的中间产物 D、生成的五步反应,每步反应的焓变近似相等 -
3、用如图所示的分馏装置使用乙酰乙酸乙酯( , A)制取脱氢醋酸(
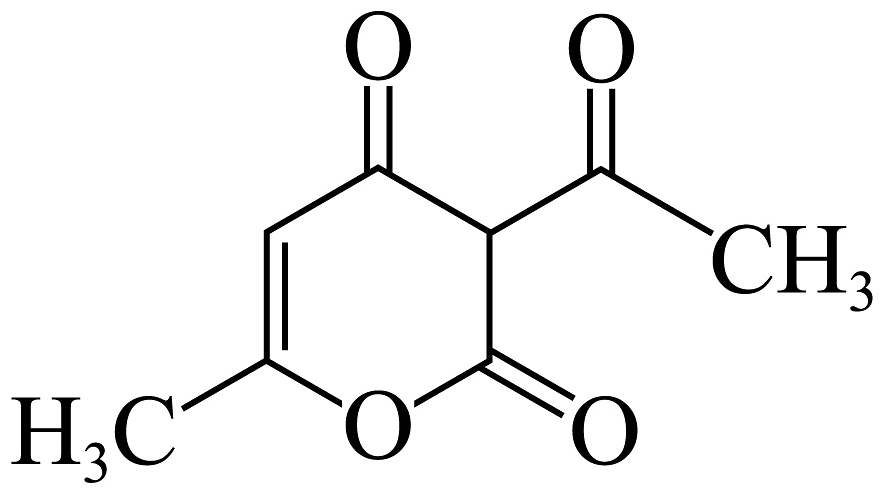 , B)时,发生可逆反应。
, B)时,发生可逆反应。已知的沸点为181℃,的沸点为270℃。以下说法错误的是
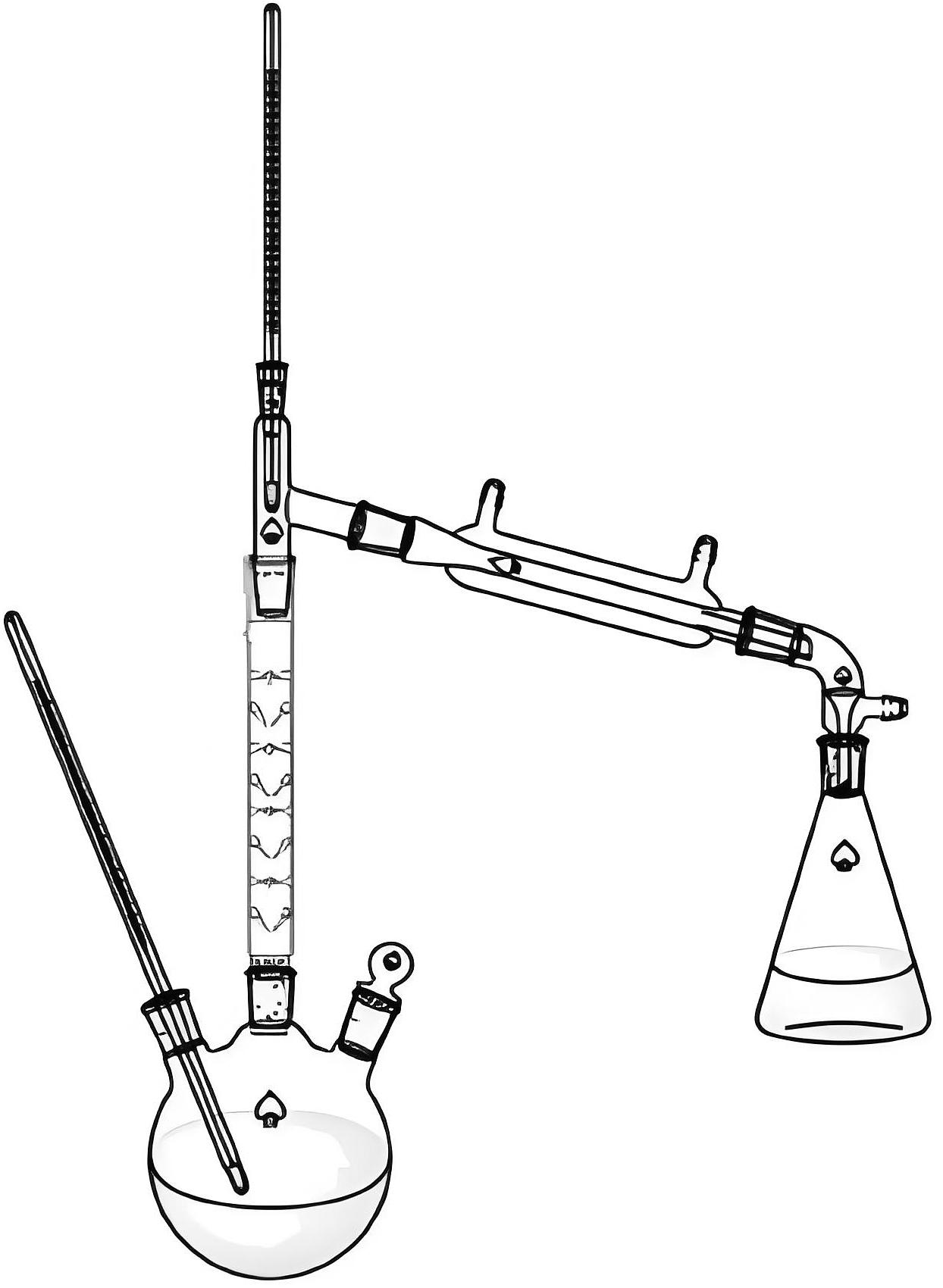 A、刺形分馏柱上缠绕棉绳的目的是减少热量散失 B、为确保实验安全,宜选用量程更大的水银温度计来代替酒精温度计 C、反应过程中除去乙醇有利于提高产率 D、可选用水作为脱氢醋酸重结晶的溶剂
A、刺形分馏柱上缠绕棉绳的目的是减少热量散失 B、为确保实验安全,宜选用量程更大的水银温度计来代替酒精温度计 C、反应过程中除去乙醇有利于提高产率 D、可选用水作为脱氢醋酸重结晶的溶剂 -
4、科学家曾在-100℃的低温下合成了如图所示的化合物 , 下列关于的说法错误的是
 A、分子的化学式为 B、分子中所有原子均共平面 C、分子中有1种化学环境的原子和2种化学环境的原子 D、温度升高时迅速分解,这可能与其键角较小而导致的不稳定性有关
A、分子的化学式为 B、分子中所有原子均共平面 C、分子中有1种化学环境的原子和2种化学环境的原子 D、温度升高时迅速分解,这可能与其键角较小而导致的不稳定性有关 -
5、下列方程式书写不正确的是A、氢氧化钙溶液与足量小苏打溶液发生反应: B、黄铜矿在大量空气中充分焙烧: C、将亚硫酸钠溶液倒入酸性重铬酸钾溶液中: D、由高锰酸钾出发制备氟气时,需要先将高锰酸钾氟化为:
-
6、物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选项
结构或性质
用途
A.
钠原子半径较大,金属键较弱,导致钠的熔点较低,且钠是热的良导体
钠可被用作原子反应堆的循环导热剂
B.
立方氮化硼与金刚石的晶体结构相似
立方氮化硼可用于制作切削刀具
C.
1-丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,具有良好的导电性
1-丁基-3-甲基咪唑六氟磷酸盐可被用作更安全的有机合成溶剂
D.
酚醛树脂具有网状结构,受热后不能软化或熔化
酚醛树脂可用于生产烹饪器具的手柄与集成电路板的底板
A、A B、B C、C D、D -
7、自然资源部于2025年1月19日宣布在甘肃安坝里北矿区发现超大规模金矿,这将增加我国黄金资源战略储备量,降低对外部黄金资源的依赖,为芯片制造、航空航天等高端制造业提供关键原材料支持。关于金元素及其化合物的性质,下列说法正确的是A、刘禹锡“千淘万漉虽辛苦,吹尽狂沙始到金。”这句诗描述了收集自然界单质金的传统方法——淘金法,原理是利用了金砂与河沙的化学性质不同 B、氰化法是从含金矿石中炼金的常用方法: , , 则理论上每提炼出 , 转移电子数为 C、根据氰化法的反应原理可知,氧化性: D、和可直接接触反应生成铯汞齐(一种合金),与在特定条件下能够反应生成金化铯(一种盐),据此可以推断出电负性:
-
8、小明是一位高一新生,有一天他看见饮用水中有些许水垢(含、等) , 于是他想起刚刚学过的“氯及其化合物”一章,新制氯水中含有、等微粒 , 可与水垢反应使其消失,并且可用于饮用水的杀菌消毒。于是他通过类比认为有效成分为的“84”消毒液同样可以,便取出厕所中的“84”消毒液,欲加入饮用水中。母亲一把夺过,并告诫他:“氯水中有大量有毒的 , 所以也有毒 , 不可用于饮用水的杀菌消毒,但是可用于物品清洁。”上述划线的说法中,错误的有A、2个 B、3个 C、4个 D、5个
-
9、短周期元素、、、的相对原子质量依次递增,其形成的一种化合物结构如图所示。下列说法正确的是
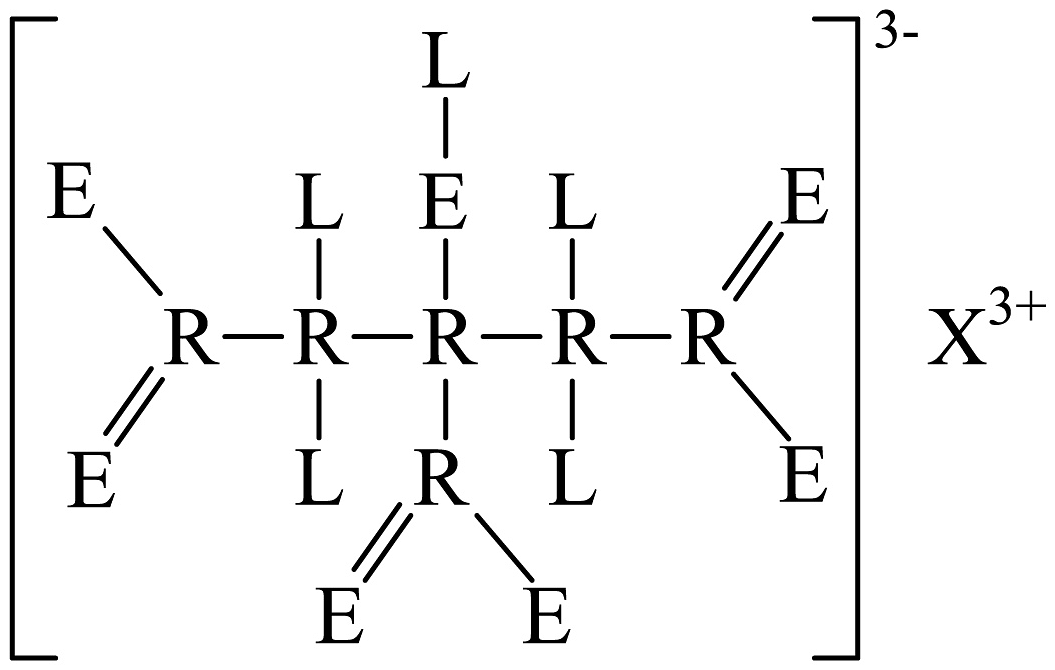 A、R、L、E可以组成最简单的蛋白质 B、形成的某种化合物可用于治疗胃酸过多 C、和是同族元素 D、分子是非极性分子
A、R、L、E可以组成最简单的蛋白质 B、形成的某种化合物可用于治疗胃酸过多 C、和是同族元素 D、分子是非极性分子 -
10、年关将至,Flawless成员准备对房间进行大扫除,下列说法正确的是A、准备清理厕所时,可以将84消毒液和洁厕灵混合使用来提高效率 B、清理厨房油污时,可以使用热的碳酸钠溶液 C、整理书柜时发现,一些书籍发生了变黄的现象,这是由于阳光照射引发的还原反应 D、在一些地方有贴灶王爷的习俗,可以使用加热的面糊进行粘贴,该过程中没有发生化学反应
-
11、以下化学用语不正确的是A、的俗名是氯仿 B、葡萄糖的实验式: C、基态原子的价电子排布式: D、的电子式为
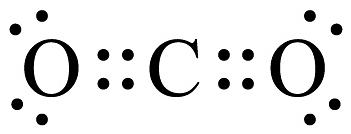
-
12、对以下物质性质的描述正确的是A、晶体是离子晶体 B、分子是非极性分子 C、中阴阳离子数目比为 D、的空间结构为形
-
13、下列有关物质结构和性质的说法,正确的是A、与的中心原子杂化轨道类型均为杂化 B、和都是单质,在中溶解度几乎一样 C、可燃冰()中甲烷分子与水分子之间并没有氢键 D、分子晶体都存在分子间作用力和共价键
-
14、下列化学用语表述正确的是A、镁原子由1s22s22p63s13p1→1s22s22p63s2时,是原子激发态转化成基态,释放能量 B、F2的p-p键形成过程:
 C、基态铍原子最外层电子的电子云图为:
C、基态铍原子最外层电子的电子云图为: D、BF3的空间构型:三角锥形
D、BF3的空间构型:三角锥形
-
15、挥发性有机化合物的减排与控制已成为我国当前阶段大气污染治理的重点工作之一,通过催化氧化法去除其中乙酸乙酯的过程如下:
I.CH3COOCH2CH3(g)+5O2(g)4CO2(g)+4H2O(g)∆H1<0(主反应)
II.CH3COOCH2CH3(g)+H2O(g)CH3COOH(g)+CH3CH2OH(g)∆H2>0
III.CH3COOH(g)+2O2(g)2CO2(g)+2H2O(g)∆H3<0
IV.CH3CH2OH(g)+3O2(g)2CO2(g)+3H2O(g)∆H4<0
(1)、反应CH3COOCH2CH3(g)+H2O(g)CH3COOH(g)+CH3CH2OH(g)∆H2=(用含∆H1、∆H3和∆H4的代数式表示)。(2)、在绝热恒容的条件下,将1mol乙酸乙酯和2mol水蒸气通入刚性容器中,只发生反应Ⅱ.下列叙述能证明此反应达到平衡状态的是(填字母)。
a.混合气体的平均相对分子质量保持不变
b.混合气体的密度保持不变
c.乙酸乙酯与水蒸气的物质的量之比保持不变
d.反应的温度保持不变
(3)、将反应Ⅱ生成的气体以一定流速通过含Cu+修饰的吸附剂,分离其中的CH3COOH(g)和CH3CH2OH(g),Cu+能与π键电子形成作用力较强的配位键。测得两种气体的出口浓度(c)与进口浓度(c0)之比随时间变化关系如图1所示。20~40min,CH3CH2OH(g)浓度比增大而CH3COOH(g)浓度比几乎为0的原因是。(4)、压强一定时,将n(乙酸乙酯):n(氧气):n(水)=1:5:1的混合气体通入装有催化剂的密闭容器中,发生反应Ⅰ、Ⅱ、Ⅲ、Ⅳ.不同温度下,平衡时各含碳物质(CH3COOCH2CH3、CH3COOH、CH3CH2OH和CO2)的百分含量S随温度变化如图所示,曲线c代表S(CH3COOH)随温度的变化。已知:。

①代表S(CH3COOCH2CH3)随温度变化的曲线是(填“a”“b”或“d”),S(CH3COOCH2CH3)在温度T2至T3间变化的原因是。
②温度为T2时,二氧化碳的体积分数是(保留一位小数)。
③若n(CH3COOCH2CH3):n(O2):n(H2O)=1:10:1,则将(填“增大”“减小”或“不变”)。
-
16、托吡司他是用于治疗高尿酸血症的常用药物,一种合成路线如下(部分试剂和条件省略):

已知:
请回答下列问题:
(1)、化合物A中的含氧官能团名称是。(2)、B→C的反应类型为。(3)、E→F的化学方程式为。(4)、已知:含氮物质的碱性随N原子电子云密度的增大而增强,则a、b、c三种物质的碱性顺序由大到小为 , 其中a物质的孤电子对位于轨道上。 (5)、I是C的同系物,其相对分子质量比C多14,在I的同分异构体中同时满足下列条件的有种。
(5)、I是C的同系物,其相对分子质量比C多14,在I的同分异构体中同时满足下列条件的有种。①遇FeCl3溶液显紫色;②取代基不超过3个,且分子中存在—CONH2
(6)、以 和甲醇为有机原料,设计
和甲醇为有机原料,设计 的合成路线(无机试剂任选) 。
的合成路线(无机试剂任选) 。 -
17、以硫铁矿(主要成分是FeS2 , 含少量Al2O3和SiO2)为原料制备纳米Fe3O4的流程如下:

已知:Asp[Fe(OH)3]=10-39Ksp[Fe(OH)2]=10-17Ksp[Al(OH)3]=10-33
(1)、“酸浸”时能够加快浸取速率的操作有(任写两种);基态Fe原子的价电子排布式是。(2)、“滤渣1”的成分是。(3)、“还原”过程发生反应的离子方程式是;假设还原后的溶液中金属离子的浓度均为0.1mol•L-1 , 则“调pH”的范围为。(保留两位有效数字)(4)、若不经“还原”,直接“调pH”,会导致。(5)、工业上用电解法制备Fe3O4 , 工作原理如图所示,已知:低共熔溶剂可传导O2- , 阳极由Cl-进行放电。
①甲电极为极;
②电解过程中若乙电极生成Cl2的体积是3.36L(标准状况下),则理论上甲电极生成的Fe3O4的质量为。
-
18、三硝酸六氨合钴(Ⅲ)[Co(NH3)6](NO3)3在配位化学、分析化学和工业催化中起到重要作用,某实验小组制备三硝酸六氨合钴(Ⅲ)[Co(NH3)6](NO3)3的过程分为两步:

Ⅰ.以CoCl2为原料来制备[Co(NH3)6]Cl3 , 化学方程式为: , 其设计如图装置(夹持仪器及加热装置已省略)。已知:Co2+在pH为7.6时开始生成Co(OH)2沉淀。
Ⅱ.制备[Co(NH3)6](NO3)3:待I反应结束后,过滤,向滤液中加入硝酸铵,冷却结晶、洗涤、干燥,最终得到产品。
回答下列问题:
(1)、装置B中盛放H2O2溶液的仪器名称为。(2)、多孔球泡的作用是。(3)、装置B中反应温度不宜过高的原因是。(4)、装置B中的NH4Cl溶液除做反应物外,另一个作用是。(5)、在[Co(NH3)6](NO3)3中,比较NH3键角键角(填“>、<或=”),试说明原因。(6)、现有样品[Co(NH3)6]Cl3•nH2O,为测定n值进行如下实验:①实验I:称取m1g产品,加入足量NaOH溶液蒸出NH3 , 再加入稀硫酸充分溶解,得到含Co3+溶液。
②向含Co3+溶液加入过量KI溶液将Co3+还原成Co2+ , 再滴加几滴淀粉溶液,并用cmol/LNa2S2O3标准溶液滴定Co2+达终点时消耗VmL(滴定过程中I2将S2O氧化为S4O , Cl-不反应)。
③实验Ⅱ:另取m1g样品,在坩埚中加热至恒重(整个过程没有刺激性气味的气体产生),得到固体质量为m2g。则n=(用含c、V、m1、m2的代数式表示);实验②中滴定至终点的现象是。
-
19、1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(
 );第二步Br—进攻碳正离子完成1,2-加成或1,4-加成,反应进程中的能量变化如下图所示,已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是
);第二步Br—进攻碳正离子完成1,2-加成或1,4-加成,反应进程中的能量变化如下图所示,已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。下列说法正确的是 A、从0℃升至40℃,1,3-丁二烯的平衡转化率增大 B、从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小 C、0℃时,两种产物的比例为“70:30”是由于生成1,2-加成产物的活化能比生成1,4-加成产物的活化能小而导致的 D、40℃时,1,3-丁二烯与HBr在该体系下反应,1,2-加成产物的浓度会缓慢增大
A、从0℃升至40℃,1,3-丁二烯的平衡转化率增大 B、从0℃升至40℃,1,2-加成正反应速率增大,1,4-加成正反应速率减小 C、0℃时,两种产物的比例为“70:30”是由于生成1,2-加成产物的活化能比生成1,4-加成产物的活化能小而导致的 D、40℃时,1,3-丁二烯与HBr在该体系下反应,1,2-加成产物的浓度会缓慢增大 -
20、常温下,向10.0mL0.1mol·L-1H3PO3溶液中滴加0.1mol·L-1氨水VmL,溶液中含P或含N粒子分布系数(δ)与pH的关系如图所示。已知:

下列叙述正确的是
A、常温下,Kb(NH3·H2O)=10-9.24 B、当氨水的体积V=5.0mL时,c(H2PO)>c(H3PO3) C、b点溶液中:c()=c(OH—)+3c(HPO) D、d点溶液中:c(H2PO)>c(H3PO3)>c()>c(OH—)