相关试卷
-
1、苯氧乙酸是制备除草剂(2,4-D)的原料。某小组设计方案制备苯氧乙酸,制备原理:

实验步骤:
步骤1:如图1装置(部分夹持及加热装置省略),在三颈瓶中加入3.8g氯乙酸和5mL水,开动搅拌,慢慢滴加饱和溶液(约需8mL),至溶液pH为7~8.然后加入2.5g苯酚,再慢慢滴加35%的NaOH溶液至反应混合液pH为12。

步骤2:将反应物在沸水浴中加热约0.5h.反应过程中pH会下降,应补加NaOH溶液,保持pH为11~12,在沸水浴上再继续加热30min,使反应完全。
步骤3:反应完毕后,将三口瓶移出水浴,趁热转入锥形瓶中,在搅拌下用浓盐酸酸化至pH为2~3。
步骤4:在冰浴中冷却,析出固体,待结晶完全后,抽滤(如图2所示),粗产物用冷水洗涤2~3次,在60~65℃干燥,产量约3.0g。

回答下列问题:
(1)、图1仪器A名称是 , 进水口为(填“a”或“b”)。(2)、步骤1中滴加试剂要“缓慢”,其原因是;能否用NaOH溶液替代溶液?答:(填“能”或“不能”),理由是。(3)、本实验多次调节pH,其目的是。(4)、相对酒精灯直接加热,步骤2用沸水浴加热的优点是。步骤3“趁热”转移的目的是。(5)、步骤4抽滤的优点是;抽滤操作部分步骤如下:①过滤完成后,先关闭抽气泵,然后再断开抽气泵和吸滤瓶之间的橡皮管。
②将准备好的液体缓慢地倒入布氏漏斗中。
③开启抽气泵,抽气以帮助滤纸紧贴在漏斗的内壁,防止液体泄漏。
④从漏斗中取出固体时,应小心地将漏斗从抽滤瓶上移除,并将漏斗管倒置,利用手的力量将固体和滤纸一同脱落到干净的表面上。
正确的先后操作顺序是(填序号)。
(6)、本实验产率最接近____(填字母)。A、46% B、58% C、75% D、81% -
2、铼(Re)被誉为“金属之王”,用于航空航天发动机制造等领域。以含铼废料(主要含、、CuO等)为原料制备铼的流程如下:

已知:过铼酸铵()是白色片状晶体,微溶于冷水,溶于热水。
回答下列问题:
(1)、下列状态Zn的最外层电子排布式中,能量最高的是____(填字母)。A、 B、
B、 C、
C、 D、
D、 (2)、根据上述流程图预测:铼在金属活动顺序表中位置在____(填字母)。A、Na之前 B、Mg、Al之间 C、Zn、Cu之间 D、Ag之后(3)、是酸性氧化物。“还原”中主要离子方程式为。“热解”中得到的化学方程式:。(4)、“沉铼”中,用(填“热水”或“冰水”)洗涤过铼酸铵,确认洗涤干净的方法是。(5)、用制备的另一种方案是:第1步,用有机溶剂萃取得到含铼有机相;第2步,用氨水反萃取得到溶液。相对“沉铼”法,该工艺优点是。
(2)、根据上述流程图预测:铼在金属活动顺序表中位置在____(填字母)。A、Na之前 B、Mg、Al之间 C、Zn、Cu之间 D、Ag之后(3)、是酸性氧化物。“还原”中主要离子方程式为。“热解”中得到的化学方程式:。(4)、“沉铼”中,用(填“热水”或“冰水”)洗涤过铼酸铵,确认洗涤干净的方法是。(5)、用制备的另一种方案是:第1步,用有机溶剂萃取得到含铼有机相;第2步,用氨水反萃取得到溶液。相对“沉铼”法,该工艺优点是。 -
3、常温下,在柠檬酸(记)和的混合液中滴加NaOH溶液,混合液中pX[ , X代表、、、]与pH的关系如图所示。下列叙述错误的是( )
 A、直线表与pH关系 B、 C、0.1 溶液呈碱性 D、的K>1000
A、直线表与pH关系 B、 C、0.1 溶液呈碱性 D、的K>1000 -
4、钒的某种氧化物的立方晶胞结构如图所示。已知:为阿伏加德罗常数的值,晶体密度为d 。下列叙述正确的是( )
 A、基态V的电子占11个能级 B、该晶体的化学式为 C、1个晶胞含2个钒离子 D、晶胞参数a为
A、基态V的电子占11个能级 B、该晶体的化学式为 C、1个晶胞含2个钒离子 D、晶胞参数a为 -
5、中南大学刘又年团队提出发展炔烃、醛、胺等工业大宗原料和炉烟二氧化碳的四组分串联反应,来实现恶唑烷酮及其衍生物的高效合成,如图所示(Path a代表反应历程a,Ph代表苯基,Bn代表苯甲基)。下列叙述正确的是( )
 A、Path a和Path b的最终产物相同 B、4→6和5→4的反应类型相同 C、上述循环中,只断裂了键 D、物质1、4、5、6都具有亲水性
A、Path a和Path b的最终产物相同 B、4→6和5→4的反应类型相同 C、上述循环中,只断裂了键 D、物质1、4、5、6都具有亲水性 -
6、实验室常用(铁氰化钾)检验。一种制备铁氰化钾的流程如下:
已知:
下列叙述错误的是( )
A、NaCN中健和键数之比为1∶2 B、中轨道和轨道以“头对头”重叠成键 C、中的配位数为6 D、稳定性: -
7、湖北省十堰地区发现大量铌、钽等稀土矿产。萃取剂P204用于萃取稀土金属铌的反应为。某温度下,萃取铌离子的溶液中与时间变化关系如图所示。

下列叙述正确的是( )
A、其他条件不变,时萃取反应已停止 B、增大,萃取平衡向左移动,平衡常数减小 C、萃取反应的正反应速率: D、段平均反应速率 -
8、近日,科学家开发///NiOOH光阳极用于持续太阳能制氢,装置如图所示。下列叙述正确的是( )
 A、能量转化形式太阳能→化学能→电能 B、阳极材料涉及元素均为前四周期元素 C、电极N的反应式为 D、阴极区越大,产率越高
A、能量转化形式太阳能→化学能→电能 B、阳极材料涉及元素均为前四周期元素 C、电极N的反应式为 D、阴极区越大,产率越高 -
9、浙江大学化学系史炳锋教授开发荧光材料分子,结构如图所示。

下列叙述错误的是( )
A、该分子属于芳香烃 B、该分子所有原子不可能共平面 C、该分子中苯环含6原子和6电子大键 D、该分子晶体的熔点由范德华力大小决定 -
10、下列实验方案中元素价态转化正确的是( )
选项
实验方案
同元素不同价态之间转化
A
向粉末中滴加70%硫酸,将气体通入氯水
S:+6→+4→+6
B
向稀硝酸中加入少量铁粉,再加入过量铜粉
Fe:0→+3→+2
C
加热和混合物,将气体通入浓硫酸中
N:-3→0→+4
D
在中加入浓盐酸,将气体通入KI淀粉溶液中
Cl:-1→0→+5
A、A B、B C、C D、D -
11、短周期主族元素X、Y、Z、W的原子序数依次增大,Z和W位于同主族,X、Y的原子序数之和等于Z的原子序数,化合物是一种净水剂,且、的VSEPR模型均为正四面体形。下列叙述正确的是( )A、原子半径:W>X>Z B、简单氢化物沸点:Z>Y C、第一电离能:W>Y>Z D、分子为极性分子
-
12、阅读下列材料,完成问题。(1)、污水中N、P过高会造成水体富营养化,脱N、P的常见方法有两种:
化学法。在含和的废水中加入石灰,生成和;也可以加铝盐或铁盐除磷。
生物法。生物脱氦是由硝化和反硝化两个生化过程完成的。污水先在耗氧池进行硝化使含氦有机物被细菌分解成氨,氨进一步转化成硝态氦;被氧化成 , 进而氧化成。在缺氧池中进行反硝化,硝态氦还原成氦气逸出。
已知: ,
下列叙述正确的是( )
A、是直线形离子 B、和中心原子杂化类型不同 C、的键角为120° D、N的电负性大于P,故氧化性比强(2)、污水中N、P过高会造成水体富营养化,脱N、P的常见方法有两种:化学法。在含和的废水中加入石灰,生成和;也可以加铝盐或铁盐除磷。
生物法。生物脱氦是由硝化和反硝化两个生化过程完成的。污水先在耗氧池进行硝化使含氦有机物被细菌分解成氨,氨进一步转化成硝态氦;被氧化成 , 进而氧化成。在缺氧池中进行反硝化,硝态氦还原成氦气逸出。
已知: , 。
下列离子方程式错误的是( )
A、在含的废水中依次加入和 , 可能发生反应: B、生物法—耗氧池中: , C、生物法—缺氧池中: D、化学法中,可能发生反应: -
13、最新研究表明:反式不饱和脂肪酸反油酸(9-trans)及其脂肪酸活化酶ACSL5促进肿瘤抗原呈递,在癌症免疫中发挥独特功能,反油酸的结构如图所示。下列叙述错误的是( )
 A、顺油酸与反油酸互为同分异构体 B、1mol 9-trans最多能消耗2mol C、9-trans能使酸性溶液褪色 D、9-trans能发生加聚、取代反应
A、顺油酸与反油酸互为同分异构体 B、1mol 9-trans最多能消耗2mol C、9-trans能使酸性溶液褪色 D、9-trans能发生加聚、取代反应 -
14、下列有关物质用途及性质都正确但是二者不匹配的是( )
选项
用途
性质
A
做豆腐时加卤水“点卤”
卤水能使蛋白质聚沉
B
口服小苏打水可缓解服用阿司匹林引发的酸中毒
能与酸反应
C
脲醛塑料(电玉,UF)作电器开关和插座
UF绝缘性好、耐溶剂性好
D
丁基羟基菌香醚(BHA)作脂肪制品的抗氧化剂
BHA具有可燃性
A、A B、B C、C D、D -
15、化学中广泛存在哲学中“量变引起质变”规律。下列变化过程不符合这一规律的是( )A、铁粉和硝酸反应 B、Al和NaOH溶液反应 C、石灰乳吸收废气中 D、向溶液中滴加氨水
-
16、“地标”是湖北名片。下列建筑材料成分变化不属于氧化还原反应的是( )A、“黄鹤楼”中的钢材在潮湿空气中生锈 B、将“武当山”香炉表面铜绿转化成Cu C、“三峡大坝”使用的高标号水泥中加入石膏调节凝固速率 D、“武汉长江大桥”的钢梁采用牺牲阳极法进行保护
-
17、延胡索乙素具有镇痛及催眠作用,其中间体E的合成路线如图。回答下列问题:
 (1)、B的结构简式为;中键与键的个数比为。(2)、已知为六元环状结构,核磁共振氢谱显示为1组峰,则其结构简式为。(3)、C中含氧官能团的名称为。(4)、写出C→D反应的化学方程式: , 该反应的反应类型为。(5)、已知化合物F是
(1)、B的结构简式为;中键与键的个数比为。(2)、已知为六元环状结构,核磁共振氢谱显示为1组峰,则其结构简式为。(3)、C中含氧官能团的名称为。(4)、写出C→D反应的化学方程式: , 该反应的反应类型为。(5)、已知化合物F是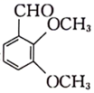 的芳香族同分异构体,则符合下列条件的F的结构有种;其中核磁共振氢谱显示有6组氢(氢原子数之比为)的结构简式为。
的芳香族同分异构体,则符合下列条件的F的结构有种;其中核磁共振氢谱显示有6组氢(氢原子数之比为)的结构简式为。①苯环上只有2个取代基
②能与溶液发生显色反应
③能发生水解反应
-
18、GaN是研制高温大功率电子器件和高频微波器件的重要材料。以废旧太阳能电池(主要成分为)为原料制备GaN的流程如图。请根据所学知识回答问题。

已知: , 。
(1)、在315℃开始凝华成有光泽的针状结晶,试推测该结晶的晶体类型:。(2)、“酸浸氧化”时,温度不宜超过50℃,原因为。(3)、加氨水调pH的目的是除铜,该步骤中分两步进行,第一步: , 第二步是生成的溶解于氨水。①根据所给信息,计算第一步反应的平衡常数。
②写出溶解于氨水的离子方程式:。
(4)、“回流过滤”中,(一种液态化合物,遇水易发生水解)与反应的化学方程式为;该工序分离和利用的原理是。(5)、气体在270℃左右以二聚物存在,请写出该二聚物的结构:。(6)、“高温气相沉积”需要将蓝宝石基板(温度高达1000℃)放在沉积炉内,然后以很低的流速将氮化镓气体从上面吹入炉内。研究发现平放基板时氮化镓分子无法稳定沉积到基板上,而将基板按倾角斜放,却获得了非常均匀的氮化镓结晶,试分析其原因:。 -
19、、(主要指和)是大气主要污染物之一、有效去除大气中的、是环境保护的重要课题。
已知:
反应1:
反应2:
反应3:
反应4:
回答下列问题:
(1)、计算 , 已知反应3的 , 则该反应自发进行的最高温度为(取整数)K。(2)、已知反应4在某催化剂作用下的反应历程如图。
①(填“”或“”)0.
②该反应历程的决速步骤为。
③可提高该反应中平衡转化率的措施有(填两条)。
(3)、向密闭容器中充入一定量的和 , 保持总压为 , 发生反应4.当时的平衡转化率随温度以及下NO的平衡转化率随投料比的变化关系如图:
①能表示此反应已经达到平衡状态的是(填标号)。
A.气体的密度保持不变
B.的浓度不变
C.
②表示时的平衡转化率随温度的变化关系曲线是(填“"或“II"),理由是。
③a、d两点对应的平衡常数大小比较为(填“>”“<”或“=”)。
④b点对应条件下的压强平衡常数(为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
-
20、氧钒(Ⅳ)碱式碳酸铵晶体{化学式为 , }是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
溶液氧钒(Ⅳ)碱式碳酸铵晶体
已知:+4价钒在弱酸性条件下具有还原性。
回答下列问题:
(1)、N2H4为二元弱碱,其在水中的电离过程与NH3类似,其第一步电离方程式为 , 第二步电离方程式为;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:。(2)、步骤ii可通过如图装置完成。
①装置的优点为 , 检查其气密性的操作为。
②实验开始时,先打开(填“K1”或“K2”)。
③盛装NH4HCO3溶液的仪器名称为。
(3)、测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度。实验步骤:粗产品wg再重复实验两次。
已知:。
①滴入NaNO2溶液的目的是除去KMnO4 , 写出其反应的离子方程式:。
②若平均消耗cmol/L(NH4)2Fe(SO4)2标准溶液的体积为amL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为。
③若其他操作均正确,但NaNO2的加入量不足,会引起测定结果(填“偏大”“偏小”或“无影响”)。