相关试卷
-
1、如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(式中为阿伏加德罗常数)A、 B、 C、 D、
-
2、硫化氢的转化是资源利用和环境保护的重要研究课题将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS溶于水)。下列说法正确的是
 A、过程①中,Cu2+起催化剂作用 B、过程②中,发生反应为S2-+2Fe3+=S↓+2Fe2+ C、过程③中,氧气被还原 D、回收S的总反应为H2S+O2=H2O+S↓
A、过程①中,Cu2+起催化剂作用 B、过程②中,发生反应为S2-+2Fe3+=S↓+2Fe2+ C、过程③中,氧气被还原 D、回收S的总反应为H2S+O2=H2O+S↓ -
3、下列图示实验装置和原理能达到实验目的的是
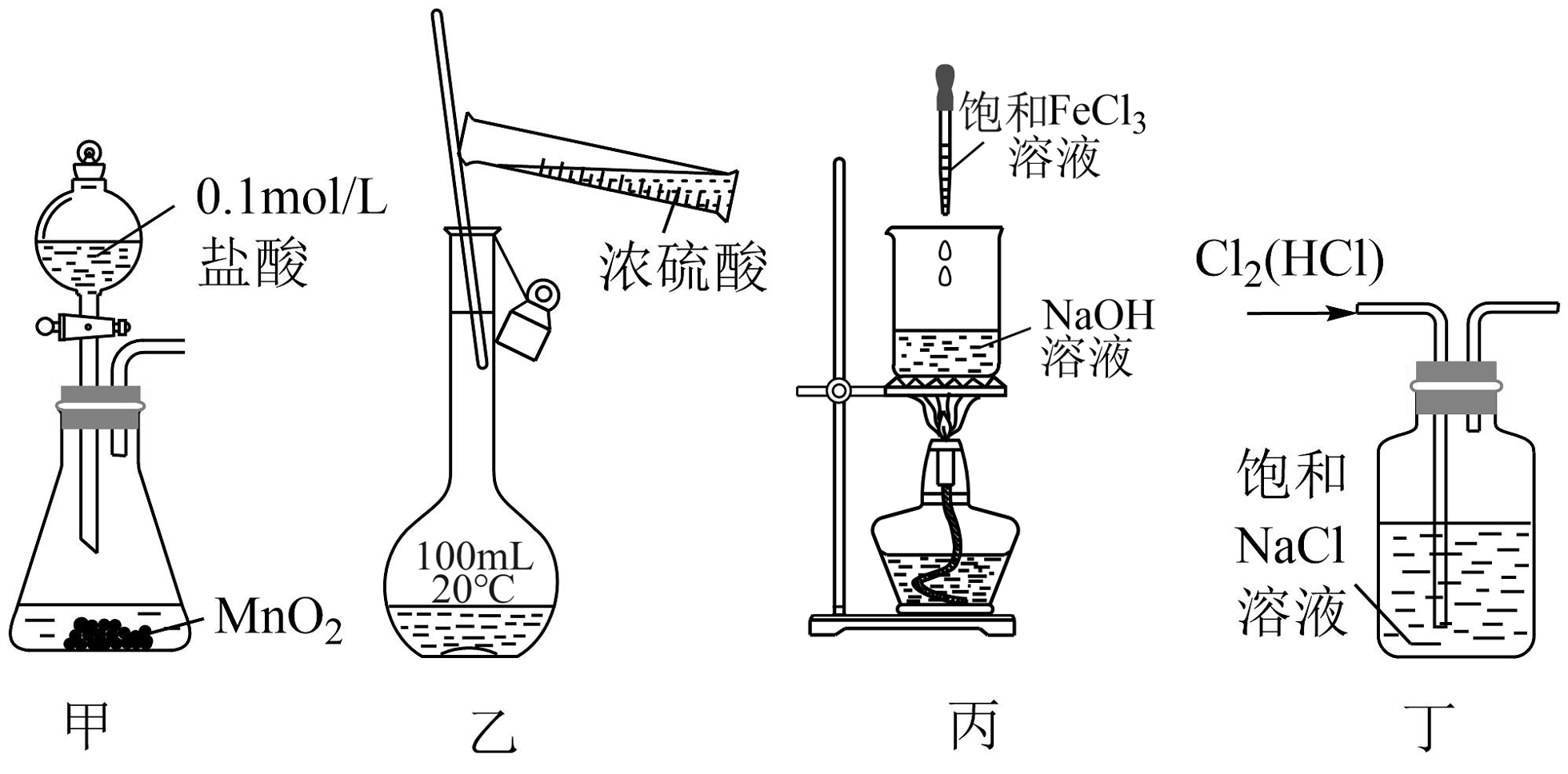 A、装置甲:实验室制取少量Cl2 B、装置乙:用浓硫酸配制一定物质的量浓度的稀硫酸 C、装置丙:制备氢氧化铁胶体 D、装置丁:除去氯气中混有的少量HCl
A、装置甲:实验室制取少量Cl2 B、装置乙:用浓硫酸配制一定物质的量浓度的稀硫酸 C、装置丙:制备氢氧化铁胶体 D、装置丁:除去氯气中混有的少量HCl -
4、下列关于Na2CO3和NaHCO3的性质说法正确的是A、碳酸氢钠晶体中加少量水会溶解,并伴有放热现象 B、碳酸钠溶液中逐滴滴加稀盐酸,开始无明显现象,一段时间后产生大量气泡 C、等物质的量的碳酸钠和碳酸氢钠固体分别与足量盐酸反应,相同条件下产生CO2体积后者多 D、可用澄清石灰水鉴别Na2CO3和NaHCO3溶液
-
5、下列有关描述对应的离子方程式书写正确的是A、食醋除去瓶胆内的水垢: B、碳酸氢钙溶液与过量的澄清石灰水混合: C、向中投入固体: D、乙醇被酸性溶液氧化成乙酸:
-
6、
将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一,煤转化为水煤气的主要化学反应为:。C(s)、CO(g)和完全燃烧的热化学方程式分别为:
① ;
② ;
③ 。
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和的热化学方程式:。(2)比较反应热数据可知,和完全燃烧放出的热量之和,比完全燃烧放出的热量(填“多”或“少”)。甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量”。
乙同学根据盖斯定律作出了下列循环图
 (3)请你写出、、、之间存在的关系式。(4)乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是。
(3)请你写出、、、之间存在的关系式。(4)乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是。 -
7、超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为: , 下列说法正确的是A、AlN是氧化产物 B、C在反应中被还原 C、Al2O3在反应中得到电子 D、生成1mol AlN时,转移3mol电子
-
8、25℃时,用0.1000mol/L的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是
 A、点①和点②所示溶液中:c(CH3COO﹣)﹣c(CN﹣)═c(HCN)﹣c(CH3COOH) B、④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 C、HCN酸性比CH3COOH弱,所以点①溶液中水的电离程度小于点②溶液 D、点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)
A、点①和点②所示溶液中:c(CH3COO﹣)﹣c(CN﹣)═c(HCN)﹣c(CH3COOH) B、④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 C、HCN酸性比CH3COOH弱,所以点①溶液中水的电离程度小于点②溶液 D、点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) -
9、反应H2O2+H2S=2H2O+S中,氧化剂是A、H2O2 B、H2S C、H2O D、S
-
10、如图所示为氟利昂破坏臭氧层的过程,下列说法不正确的是
 A、过程Ⅳ中既有极性共价键的断裂又有非极性共价键的形成 B、整个过程可用方程式表示为 C、的电子式为
A、过程Ⅳ中既有极性共价键的断裂又有非极性共价键的形成 B、整个过程可用方程式表示为 C、的电子式为 D、上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂
D、上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂
-
11、将图2中的物质补充到图1中,可得到一个氧化还原反应的离子方程式(未配平)。下列对该反应的说法不正确的是
 A、具有氧化性,在该反应中作氧化剂 B、发生了还原反应,每生成转移个电子 C、随着反应的进行,溶液酸性减弱 D、和的化学计量系数之比为
A、具有氧化性,在该反应中作氧化剂 B、发生了还原反应,每生成转移个电子 C、随着反应的进行,溶液酸性减弱 D、和的化学计量系数之比为 -
12、已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是A、a=b B、混合溶液的pH=7 C、混合溶液中,c(H+)=mol.L-1 D、混合溶液中c(H+)+c(B+)=c(OH-)+c(A-)
-
13、下列变化一定不涉及电子转移的是A、天然气燃烧 B、用生石灰干燥氢气 C、食物变质 D、KClO3分解制氧气
-
14、下列离子在指定条件下的溶液中,一定能大量共存的是A、无色澄清溶液中:K+、Fe3+、SO、Mg2+ B、使石蕊变红色的溶液中:NO、Cl-、K+、SO C、含有大量Ba2+的溶液:NH、Na+、CO、I- D、加入Na2O固体的溶液中:Ba2+、Cu2+、NO、Cl-
-
15、英菲替尼(化合物L)是治疗胆管癌的新型药物,其合成路线如下。

回答下列问题:
(1)、A的化学名称是。(2)、由A生成C的反应类型是。(3)、E的结构简式为。(4)、由G→J的转化过程可知,G转化为H的目的是(5)、符合下列条件的B的同分异构体共有种,其中一种的结构简式为。①分子中含环状结构 ②核磁共振氢谱显示2组峰
(6)、L中氮原子的杂化方式为。(7)、1,3-二苯基脲( )是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。
)是某些药物分子的重要结构单元。参照上述合成路线,写出以苯为原料制备1,3-二苯基脲的合成路线(无机试剂任选)。 -
16、下列有关化学用语表述正确的是A、和离子结构示意图均可以表示为
 B、HClO的结构式: H-Cl-O
C、的电子式:
B、HClO的结构式: H-Cl-O
C、的电子式: D、用电子式表示的形成过程为
D、用电子式表示的形成过程为
-
17、有4种碳骨架如图所示的烃,下列说法正确的是
 A、a和b、d互为同分异构体 B、a和b都能发生加成反应 C、b和c互为同系物 D、只有b和c能发生取代反应
A、a和b、d互为同分异构体 B、a和b都能发生加成反应 C、b和c互为同系物 D、只有b和c能发生取代反应 -
18、实验室用等原料制取少量的实验流程如下。下列说法正确的是
 A、“熔融”时,应先将和混合加热一段时间后再加入KOH B、通入“歧化”时,氧化剂与还原剂的物质的量之比为2:1 C、“过滤”时,为加快分离速率可采用减压过滤 D、制得的粗品可能会含有 , 可以向粗品中滴加盐酸观察是否有气泡来检验是否含有
A、“熔融”时,应先将和混合加热一段时间后再加入KOH B、通入“歧化”时,氧化剂与还原剂的物质的量之比为2:1 C、“过滤”时,为加快分离速率可采用减压过滤 D、制得的粗品可能会含有 , 可以向粗品中滴加盐酸观察是否有气泡来检验是否含有 -
19、我国科学家侯德榜发明了联合制碱法。联合以氯化钠、氨及二氧化碳为原料,同时生产纯碱和氯化铵两种产品,又称“侯氏制碱法”,对世界制碱工业做出了卓越贡献。下列是“侯氏制碱法”制备纯碱的工艺流程,回答下列问题。
 (1)、纯碱的化学式为 , 他的类别是(填“单质”、“氧化物”、“酸”、“碱”或“盐”),其常见用途有。(2)、请写出“侯氏制碱法”中,往饱和食盐水中通入和发生的化学反应方程式该反应(填“属于”或“不属于”)氧化还原反应。(3)、粗盐水中含大量、、 , “除杂”时依次加入过量的、、提纯。用离子方程式说明加入的目的。(4)、若在实验室中进行“分离”操作,用到的玻璃仪器有烧杯、。(5)、循环Ⅰ中参与循环的物质是。(6)、制得的纯碱可能含少量 , 检验含有该杂质的方法及现象是。
(1)、纯碱的化学式为 , 他的类别是(填“单质”、“氧化物”、“酸”、“碱”或“盐”),其常见用途有。(2)、请写出“侯氏制碱法”中,往饱和食盐水中通入和发生的化学反应方程式该反应(填“属于”或“不属于”)氧化还原反应。(3)、粗盐水中含大量、、 , “除杂”时依次加入过量的、、提纯。用离子方程式说明加入的目的。(4)、若在实验室中进行“分离”操作,用到的玻璃仪器有烧杯、。(5)、循环Ⅰ中参与循环的物质是。(6)、制得的纯碱可能含少量 , 检验含有该杂质的方法及现象是。 -
20、数字化实验是利用传感器和信息处理终端进行数据采集与分析的实验手段。下图是利用数字化实验测定光照氯水过程中得到的图像,该图像表示的意义是
 A、氯离子浓度随时间的变化 B、氧气体积分数随时间的变化 C、氯水的pH随时间的变化 D、氯水导电能力随时间的变化
A、氯离子浓度随时间的变化 B、氧气体积分数随时间的变化 C、氯水的pH随时间的变化 D、氯水导电能力随时间的变化