相关试卷
-
1、设为阿伏加德罗常数的值,下列说法正确的是A、将0.1mol完全溶于稀氨水中使溶液呈中性,溶液中的数目等于 B、1mol完全水解生成的胶体粒子数目为 C、标准状况下5.6L与5.6L混合后光照,充分反应后生成个 D、5.8g完全裂解,可得到0.1mol
-
2、酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药,其结构如图所示,下列有关说法不正确的是
 A、该分子结构中含有3种官能团 B、该物质的分子式是 C、该分子结构中所有碳原子不可能共平面 D、该物质可发生取代反应、还原反应、氧化反应
A、该分子结构中含有3种官能团 B、该物质的分子式是 C、该分子结构中所有碳原子不可能共平面 D、该物质可发生取代反应、还原反应、氧化反应 -
3、下列表示正确的是A、丙氨酸的结构简式: B、基态氧原子的价电子排布图为:
 C、天然橡胶的结构简式:
C、天然橡胶的结构简式: D、中子数为34的锌原子:
D、中子数为34的锌原子:
-
4、一些化学物质在其包装上应贴上相应的安全使用标识,下列物质对应的标识不正确的是
物质
浓
安全使用标识
 腐蚀类物质
腐蚀类物质 毒性物质
毒性物质
爆炸类物质

易燃类物质
选项
A
B
C
D
A、A B、B C、C D、D -
5、下列物质属于纯净物的是A、酒精 B、漂白粉 C、胶体 D、汽油
-
6、仿生催化反应是未来发展的重要方面,我国仿生催化反应研究走在世界前列。化合物V是一种重要的仿生催化剂,合成路线如图所示:

回答下列问题:
(1)、化合物II的同分异构体中,核磁共振氢谱只有1组吸收峰的结构简式为;化合物III的分子式为。(2)、化合物I的化学名称为 , 其同分异构体中含有-CHBr-CHO结构的有种(不考虑立体异构),根据化合物I的结构特征,分析预测其可能的化学性质,完成表格。序号
反应试剂、条件
反应形成的新结构
反应类型
a
NaOH乙醇溶液、加热
b
氧化反应(生成有机产物)
(3)、关于反应③的说法中,正确的有(填选项序号)。A、反应过程中,既有C-O键的断裂,又有C-O键的形成 B、反应过程中,既有C=O键的断裂,又有C=O键的形成 C、化合物III和IV都是极性分子,碳原子之间均以“头碰头”方式形成化学键 D、反应③是加成反应(4)、反应⑤方程式为 +R3-CH2-CHO
+R3-CH2-CHO ,以乙烯和乙醛为原料,无机试剂任选,利用反应②、③和⑤的原理合成化合物VI(
,以乙烯和乙醛为原料,无机试剂任选,利用反应②、③和⑤的原理合成化合物VI( )。
)。①第一步反应是乙烯在Ag催化下与O2反应,产物的结构简式为。
②最后一步的化学方程式为。
-
7、R是一种亲氯有机物,属于非电解质,易溶于水,在含Cl-的溶液中能发生如下反应。
反应I:R(aq)+Cl-(aq)RCl-(aq)
反应II:RCl-(aq)+Cl-(aq)RCl(aq)
回答下列问题:
(1)、常温下,向NaCl溶液中加入R,15s末测得c(RCl-)=0.07mol/L,c(RCl)=0.04mol/L。①0~15s内,Cl-的平均消耗速率v(Cl-)=。
②待反应充分进行,达到平衡状态时溶液的体积为V0 , 加蒸馏水稀释至溶液体积为V,达到新平衡时,Cl-的物质的量浓度为c平衡(Cl-),RCl的物质的量浓度为c平衡(RCl)。写出反应I平衡常数的表达式KI= , 稀释过程中平衡常数KI的值(填“变大”、“变小”或“不变”),请在答题卡坐标内画出随1g的变化趋势曲线。
(2)、室温下,向Cl-初始浓度c0(Cl-)=amol/L的NaCl溶液中加入不同量的R,用数据传感器测得平衡时(X表示Cl-、RCl- , RCl随变化的数据,记录如表所示(b和d代表数字,忽略溶液体积变化):0
0.25
0.50
0.75
1.00
Cl-
1.00
0.79
0.64
0.54
0.46
RCl-
0
0.09
0.16
0.22
0.28
RCl
0
0.06
b
d
0.13
①从表格中数据可看出关系式:++2×=1,则d=;此关系式也可从理论上推导,下列理论依据中,可推导该关系式的有(填选项序号)。
A.能量守恒定律
B.电荷守恒定律
C.质量守恒定律
D.氧化还原反应遵循还原剂失去的电子总数和氧化剂得到的电子总数相等的规律
②=0.50时,R的转化率为(写出计算过程)。
(3)、R的分子结构可表示为M-COOH,M为有机分子部分结构。补充完整方程式:R+CH3CH2OHM-COOCH2HC3+。 -
8、22号元素钛(Ti)的单质被誉为未来金属。工业冶炼Ti后的废渣中有SiO2和含Ti、Ca、Fe、Cu、Mg的化合物,从该废渣中回收Ti,并获得高附加值化工产品(MgF2、活性CaCO3、K2FeO4、X)的一种生产工艺如图所示:
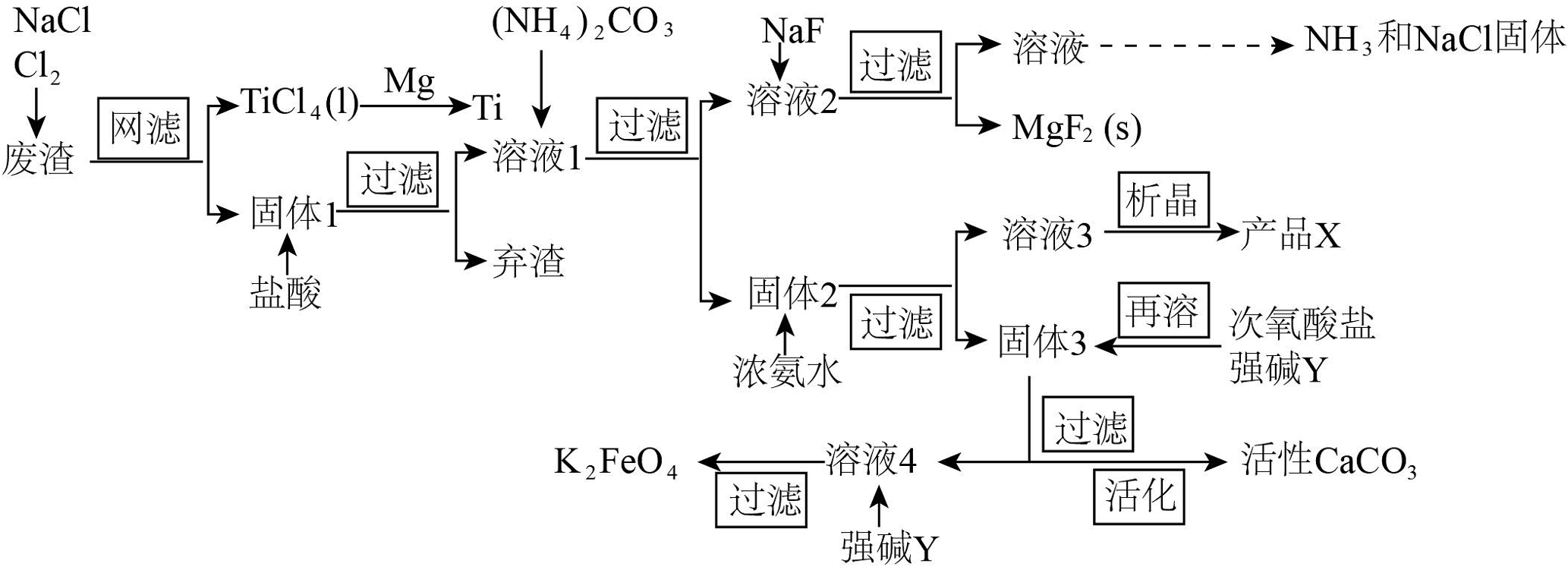
已知:生产条件下MgF2的溶度积为9.0×10-9;NH4+时存在时,不易生成MgCO3沉淀,固体2中有CaCO3、Cu2(OH)2CO3和某含铁化合物。
(1)、写出基态Ti原子的价电子排布式:。(2)、工艺设计要准确分析物质成分,科学加入试剂,准确把握用量,离子物质的量浓度≤1.0×10-5mol/L时,一般认为该离子沉淀完全。①选择向固体1中加入盐酸而不加入硫酸的原因是。
②“析晶”过程是向深蓝色溶液3中先加入适量70%的H2SO4中和过量的氨水,再加入适量乙醇,得到深蓝色品体X,产品X的化学式是。
③“再溶”过程中加入强碱Y的稀溶液,溶液4中加入适量强碱Y的固体,强碱Y的化学式是;写出固体3“再溶”过程的离子方程式:。
④测得溶液2中c(Mg2+)=0.030mol/L,要确保Mg2+沉淀完全,1L溶液2至少需加入NaF的物质的量为mol(忽略溶液体积变化)。
(3)、以上生产工艺中可循环利用的物质有NH3和(填化学式)。(4)、活性炭酸钙晶胞为正方体结构,晶胞结构如图所示,黑点代表Ca2+ , 白色小圈代表CO , 晶胞边长为anm。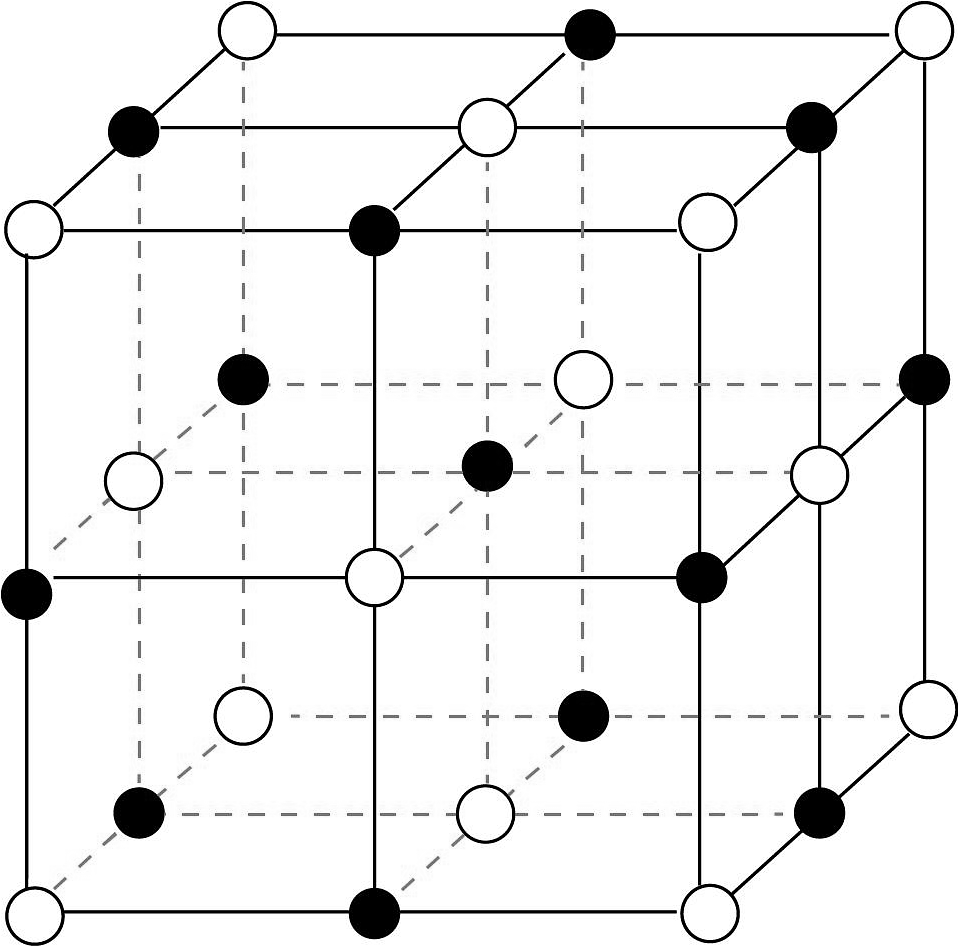
①活性炭酸钙晶体中一个CO周围与其最近且等距的Ca2+的个数为。
②最近两个Ca2+之间的距离为nm(用含a的代数式表示)。
-
9、醋酸(用HAc表示)是生活中常见的有机弱酸。某小组欲借助传感器探究醋酸的电离过程。查阅资料:一定条件下,按=1配制的溶液中,c(H+)的值等于HAc的Ka;稀溶液中,H+(aq)+OH-(aq)=H2O(1) △H=-57.300kJ/mol。(1)、配制0.10mol/LHAc溶液:
①配制250mL0.10mol/L的HAc溶液,需5.0mol/LHAc溶液的体积为mL。
②配制250mL0.10mol/LHAc溶液,下列仪器中不需要的是(填仪器名称)。
 (2)、探究电离程度:量取20.00mL所配HAc溶液于锥形瓶中,加入指示剂,用0.1000mol/LNaOH溶液滴定,恰好完全反应时消耗NaOH溶液21.20mL,用pH传感器测滴定过程的pH(部分数据如表所示)。
(2)、探究电离程度:量取20.00mL所配HAc溶液于锥形瓶中,加入指示剂,用0.1000mol/LNaOH溶液滴定,恰好完全反应时消耗NaOH溶液21.20mL,用pH传感器测滴定过程的pH(部分数据如表所示)。V(NaOH)/mL
0.00
10.00
15.00
19.00
20.00
pH
2.87
4.70
5.12
5.70
6.02
①指示剂适宜选用(填“酚酞”或“甲基橙”)。
②该HAc溶液浓度为mol/L。
③根据表格数据,得出该温度下HAc的Ka10-4.70(填“>”、“<”或“=”)。
(3)、探究电离过程热效应:取上述HAc和NaOH溶液各100mL于量热装置中反应,测得反应前后体系的温度值变化△T,重复操作3次,记录实验数据如表所示:实验
I
II
III
△T/℃
0.59
0.61
0.60
①重复操作3次的目的是。
②平均每次HAc和NaOH溶液反应放出的热量为J【c和p分别取4.18J/(g•℃)、1.0g/mL,忽略水以外各物质吸收的热量,保留两位小数,下同】。
③根据所学原理,可推知的热效应△H=kJ/mol。
(4)、写出一种生活中常见的无机弱酸及其用途:。 -
10、利用镁-次氯酸盐电池为电源,模拟电浮选凝聚法处理污水示意图如图所示,通过铁和石墨电极在污水中电解,利用污水中溶解的氧将生成的Fe2+转化为Fe(OH)3沉淀吸附污染物,气泡把污水中悬浮物带到水面形成浮渣层,从而达到净水的目的。下列说法错误的是
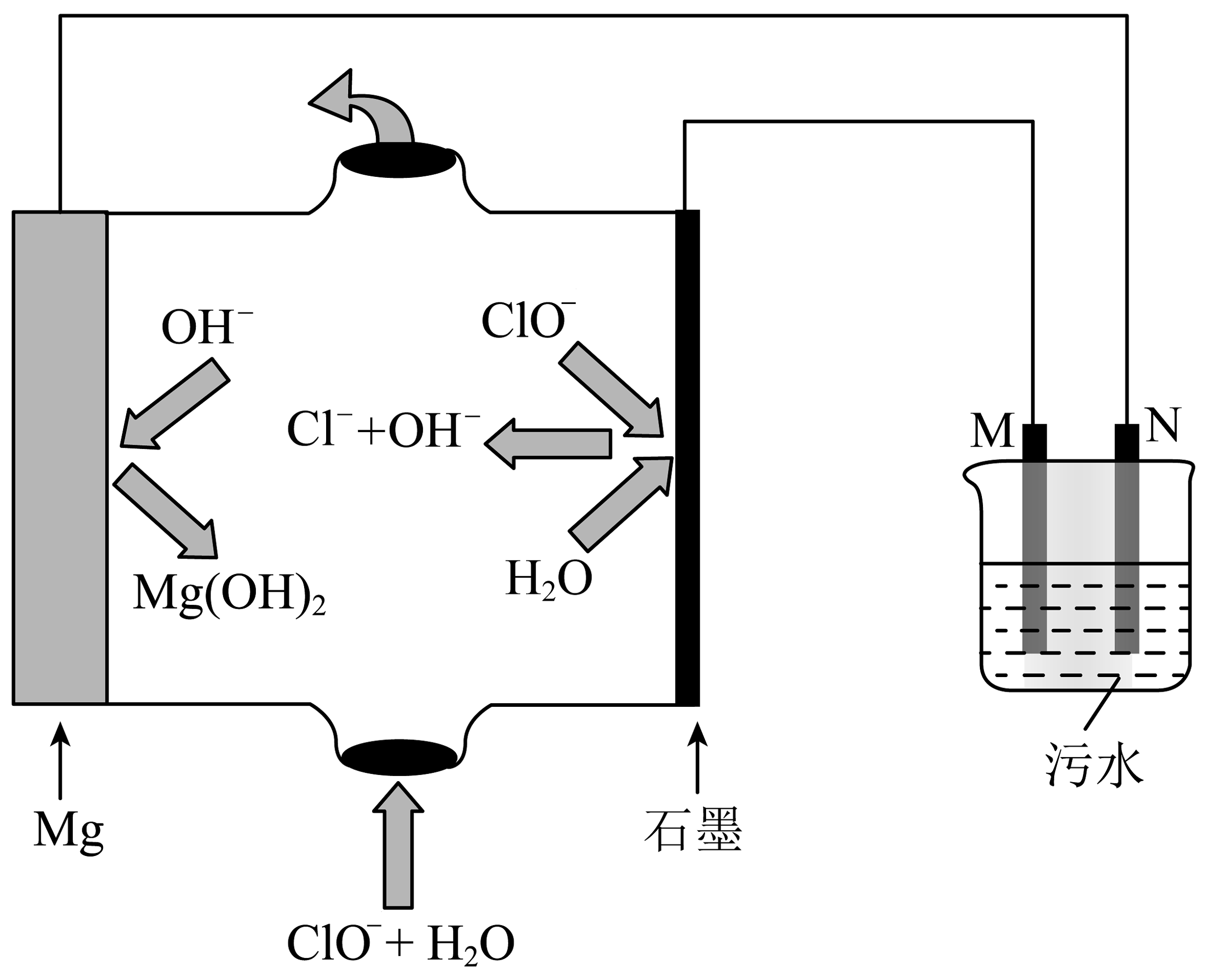 A、镁-次氯酸盐电池总反应的离子方程式为Mg+ClO-+H2O=Mg(OH)2+Cl- B、M应是石墨电极,N应是铁电极 C、生成Fe(OH)3 , 沉淀反应的离子方程式为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ D、将污水中悬浮物带到水面形成浮渣层的气泡成分主要是H2
A、镁-次氯酸盐电池总反应的离子方程式为Mg+ClO-+H2O=Mg(OH)2+Cl- B、M应是石墨电极,N应是铁电极 C、生成Fe(OH)3 , 沉淀反应的离子方程式为4Fe2++10H2O+O2=4Fe(OH)3↓+8H+ D、将污水中悬浮物带到水面形成浮渣层的气泡成分主要是H2 -
11、在Fe2O3的催化作用下,向200℃的恒温恒容密闭容器中充入1molCH4和2molNO2 , 发生反应CH4(g)+2NO2(g)CO2(g)+N2(g)+2H2O(g),反应过程及能量变化示意图如图所示。下列说法正确的是
 A、容器内气体的密度不再发生变化时,该反应达到平衡状态 B、反应一段时间后(未达平衡),Fe3O4会远远多于Fe2O3 C、起始条件相同,其他条件不变,仅改为绝热密闭容器,CH4和NO2的转化率降低 D、使用更高效的催化剂能提高该反应平衡时的转化率
A、容器内气体的密度不再发生变化时,该反应达到平衡状态 B、反应一段时间后(未达平衡),Fe3O4会远远多于Fe2O3 C、起始条件相同,其他条件不变,仅改为绝热密闭容器,CH4和NO2的转化率降低 D、使用更高效的催化剂能提高该反应平衡时的转化率 -
12、化合物WV4Y(ZX4)2用途广泛,所含5种短周期元素V、W、X、Y、Z的原子序数依次增大,每个短周期均有分布,X与W处于同周期,X与Z同主族,W的基态原子价层p轨道半充满,基态Y原子最高能级的电子排布式为npn-2 , 基态Z原子最高能层p轨道均有电子且有2个未成对电子。下列说法正确的是A、ZX3和WX的空间结构相同 B、第一电离能:W<X<Z C、简单氢化物稳定性:X<Z D、W简单气态氢化物的溶液和最高价氧化物对应水化物的溶液,都能溶解Y最高价氧化物对应水化物
-
13、甲醇能与乙酸发生酯化反应:CH3COOH+CH3OHCH3COOCH3+H2O。下列说法错误的是
 A、该反应过程中,甲醇分子中O-H键断裂 B、如图所示可表示甲醇分子中C-H键成键过程 C、其他条件一定时,适当增大投料比【n(乙酸):n(甲醇)】可提高甲醇转化率 D、加入浓硫酸和加热能加快酯化反应速率
A、该反应过程中,甲醇分子中O-H键断裂 B、如图所示可表示甲醇分子中C-H键成键过程 C、其他条件一定时,适当增大投料比【n(乙酸):n(甲醇)】可提高甲醇转化率 D、加入浓硫酸和加热能加快酯化反应速率 -
14、设NA为阿伏加德罗常数的值,硫酸工业涉及S→SO2→SO3→H2SO4的转化过程。下列说法正确的是A、标准状况下,含NA个硫原子的硫单质体积为22.4L B、将2molSO2和1molO2混合于密闭容器中,充分反应后,转移的电子数为4NA C、1molSO2和SO3混合气体通入过量NaOH溶液中,所得溶液中SO和SO离子总数为NA D、1mol/L的H2SO4溶液中:c(H+)>2c(SO)
-
15、含Fe物质的分类与相应化合价关系如图所示,c和f均为盐酸盐,其中f晶体熔点为306℃,沸点为316℃。下列推断不合理的是
 A、检验f溶液中是否含c,可向f溶液中依次加入KSCN溶液和双氧水 B、a与Cl2可直接化合生成f,f为分子晶体,含有共价键 C、含d矿石可冶炼a,f可用于制作印刷电路板 D、向盛有c溶液的烧杯中滴加NaOH溶液,存在c→b→e的转化
A、检验f溶液中是否含c,可向f溶液中依次加入KSCN溶液和双氧水 B、a与Cl2可直接化合生成f,f为分子晶体,含有共价键 C、含d矿石可冶炼a,f可用于制作印刷电路板 D、向盛有c溶液的烧杯中滴加NaOH溶液,存在c→b→e的转化 -
16、甲和丙是2-羟基环己基甲酸(乙)的上下游产品(甲、乙、丙的结构简式如图所示),在生态研究中具有重要作用。下列说法错误的是
 A、乙能与氨基酸或蛋白质反应 B、1mol丙最多能与2molNaOH反应 C、相同物质的量浓度和温度下,甲水溶液的酸性比乙强 D、甲和乙分子中手性碳原子数目相同
A、乙能与氨基酸或蛋白质反应 B、1mol丙最多能与2molNaOH反应 C、相同物质的量浓度和温度下,甲水溶液的酸性比乙强 D、甲和乙分子中手性碳原子数目相同 -
17、幸福生活是劳动创造的,同学们要积极参与劳动。下列劳动项目没有运用相关原理的是
选项
劳动项目
相关原理
A
家务劳动:利用消毒碗柜高温消毒
加热使蛋白质变性,失去生理活性
B
体育比赛志愿者:向伤者受伤部位喷氯乙烷降温镇痛
氯乙烷易挥发,挥发过程吸热
C
环保活动:宣传使用无磷洗涤剂
含磷洗涤剂伤皮肤
D
清洁活动:用NaOH溶液除污剂清洗抽油烟机
油脂在碱性条件下易水解为可溶物
A、A B、B C、C D、D -
18、在触媒作用下,利用电化学原理处理酸性溶液中有机物的原理如图所示。下列分析正确的是
 A、B电极是负极 B、A电极的电极反应式为C13H8N2O2+2e-=C13H10N2O2+2OH- C、若有机物是甲酸(HCOOH),处理1mol甲酸,理论上需要11.2LO2(标准状况) D、电子从A电极区通过离子交换膜进入B电极区
A、B电极是负极 B、A电极的电极反应式为C13H8N2O2+2e-=C13H10N2O2+2OH- C、若有机物是甲酸(HCOOH),处理1mol甲酸,理论上需要11.2LO2(标准状况) D、电子从A电极区通过离子交换膜进入B电极区 -
19、如图所示是配制某物质的量浓度NaOH溶液的某些步骤。下列说法错误的是
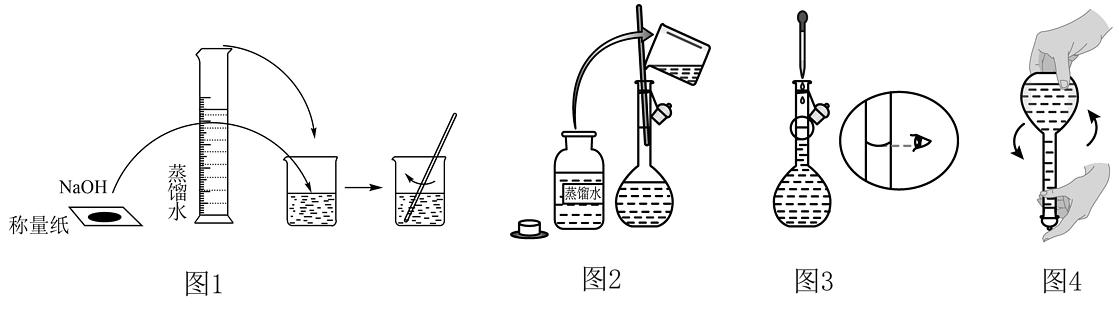 A、图1:称量并溶解NaOH B、图2:转移洗涤液 C、图3:定容 D、图4:定容后反复上下颠倒摇匀
A、图1:称量并溶解NaOH B、图2:转移洗涤液 C、图3:定容 D、图4:定容后反复上下颠倒摇匀 -
20、打造特色产业是持续推进乡村振兴战略的重要举措。下列说法正确的是A、云南九乡利用区域内溶洞大力发展旅游业,溶洞的形成过程中发生了化学变化 B、河南中牟发展葡萄种植和酿酒业,葡萄糖可水解为乙醇 C、广东电白依托大面积种植花生发展食用油产业,花生油属于天然有机高分子化合物 D、黑龙江安达市以奶酪为载体打造畜牧产业链,奶酪的主要成分属于糖类