相关试卷
-
1、化学在生产生活中有着广泛的应用,下列两项内容说法正确且存在因果关系的是( )
物质性质
实际应用
A
硅为半导体材料
SiO2用于光纤通讯
B
Cl2具有氧化性
氯水可以漂白有色布条
C
Al表面易形成致密的氧化物薄膜
可以用铝槽车运送热的浓硫酸
D
乙醇可以使蛋白质变性
乙醇用于制作医用酒精
A、A B、B C、C D、D -
2、“空气变面包,氨功不可没”。下列说法错误的是A、液氨可用作制冷剂 B、是平面三角形的极性分子 C、可以还原CuO D、合成氨是人工固氮最重要途径
-
3、化学与生活、生产密切相关,下列说法正确的是A、为增强“84”消毒液的消杀新冠肺炎病毒效果,可加入浓盐酸 B、从石墨中剥离出的石墨烯薄片能导电,因此是电解质 C、油脂、糖类以及蛋白质在人体内均能发生水解反应 D、嫦娥五号返回器带回的月壤中含有 , 它与地球上的属于同位素
-
4、氯喹是合成一种抑制病毒药物的中间体,其合成路线如下图:
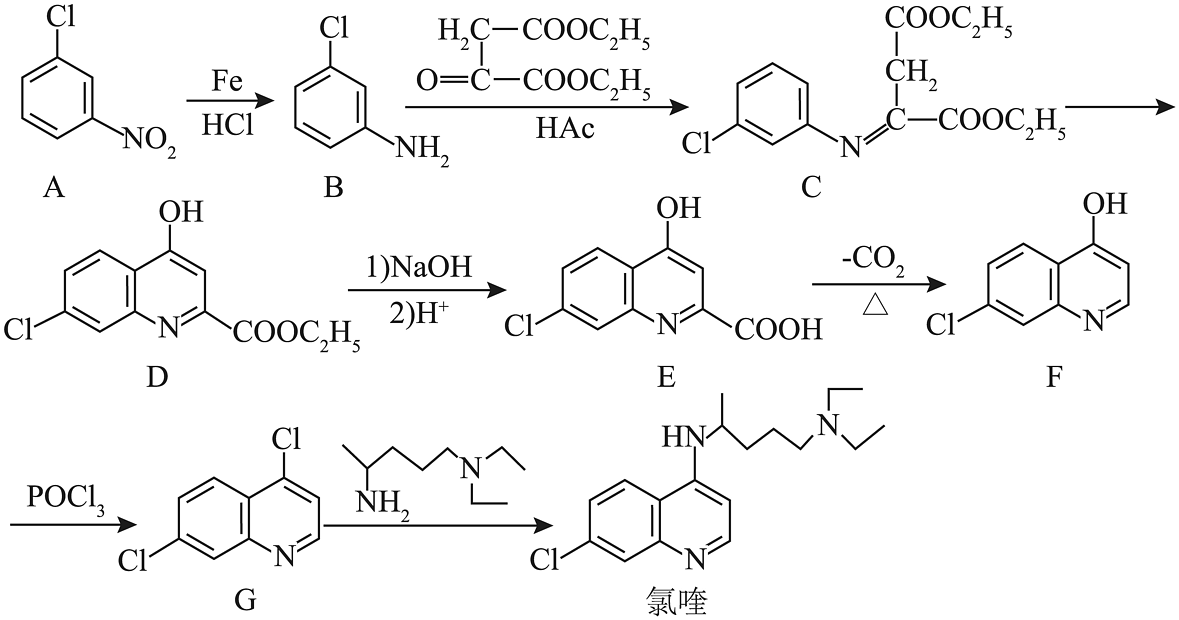 (1)、D分子中含氧官能团的名称是。(2)、的反应需经历两步,其反应类型依次为、。(3)、CD反应过程中有副产物X(与D互为同分异构体)生成,X的结构简式为。(4)、E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。
(1)、D分子中含氧官能团的名称是。(2)、的反应需经历两步,其反应类型依次为、。(3)、CD反应过程中有副产物X(与D互为同分异构体)生成,X的结构简式为。(4)、E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:。①酸性条件下水解得两种均能发生银镜反应的有机产物,其中一种与溶液发生显色反应;②分子中有氰基(-CN);③分子中有4种不同化学环境的氢;④分子中有一个手性碳原子。
(5)、写出以1,3-丁二烯( )和
)和 为原料制备
为原料制备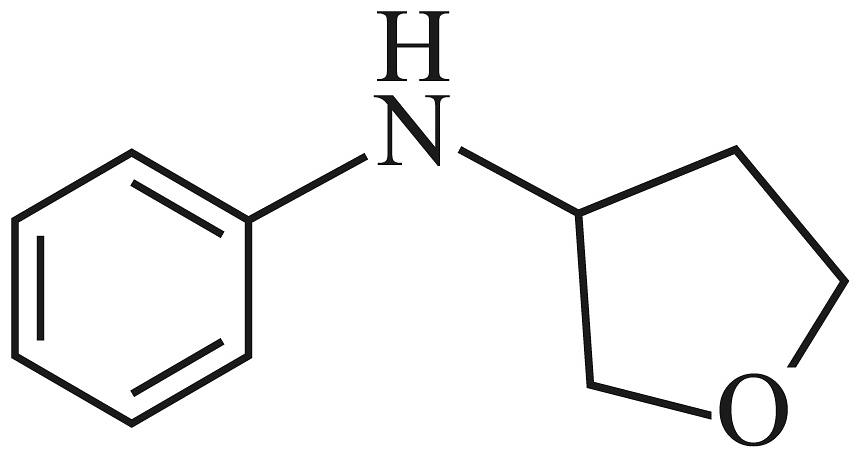 的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。 -
5、溴苯主要用于溶剂、分析试剂和有机合成等。合成溴苯所用原料苯、溴及溴苯的部分物理性质数据及实验装置如下所示。
苯
溴
溴苯
密度/g·cm-3
0.88
3.10
1.50
沸点/℃
80
59
156
水中溶解度
微溶
微溶
微溶
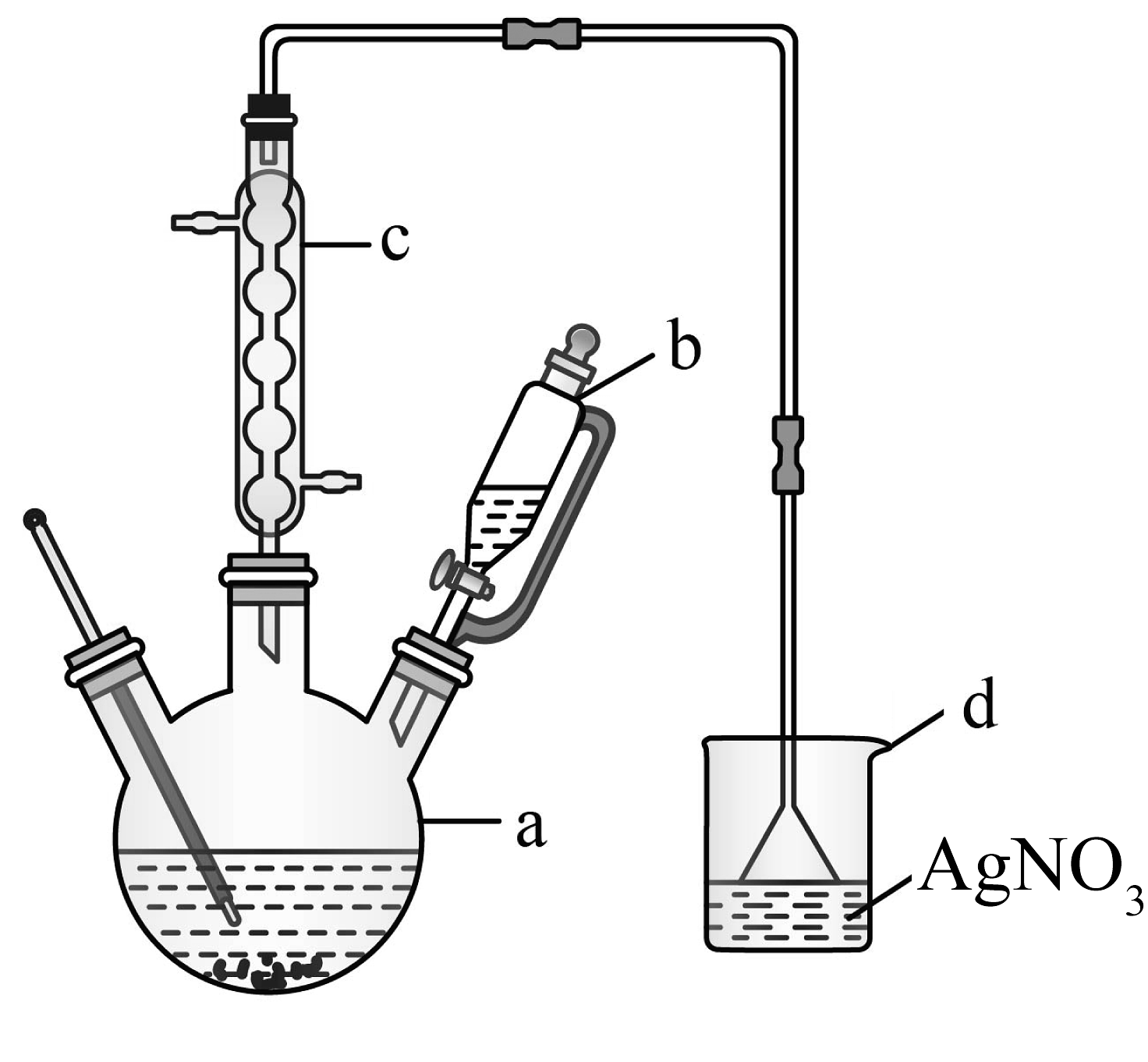 (1)、装置a名称是。(2)、在a中加入少量铁屑和苯,将b中液溴缓慢加入a,发生反应的化学方程式为 , 能说明该反应所属类型的实验现象是。装置c的作用是 , 水流方向是(填“下进上出”或“上进下出”)。(3)、若反应温度过高会生成二溴代苯,写出其中一种主要产物的结构简式。(4)、待反应结束后,从a中混合液分离、提纯产物。
(1)、装置a名称是。(2)、在a中加入少量铁屑和苯,将b中液溴缓慢加入a,发生反应的化学方程式为 , 能说明该反应所属类型的实验现象是。装置c的作用是 , 水流方向是(填“下进上出”或“上进下出”)。(3)、若反应温度过高会生成二溴代苯,写出其中一种主要产物的结构简式。(4)、待反应结束后,从a中混合液分离、提纯产物。①向a中加入水,过滤除去未反应的铁屑。
②补充完整由滤液提取溴苯的实验方案。(实验中可选用的设备和试剂:蒸馏水、10%的NaOH溶液、无水氯化钙、通风橱)
-
6、有机化合物是一种可用于小面积轻度创面镇痛的医用常见麻醉剂,对有机物A进行质谱分析、红外光谱分析,结果如图所示。
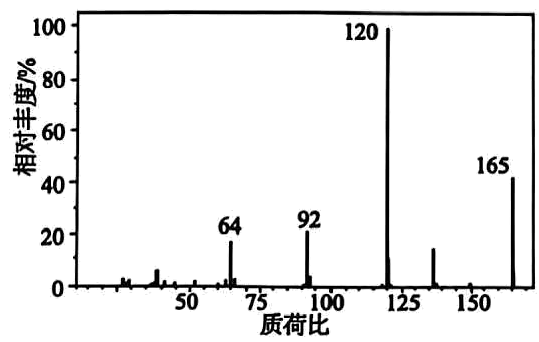
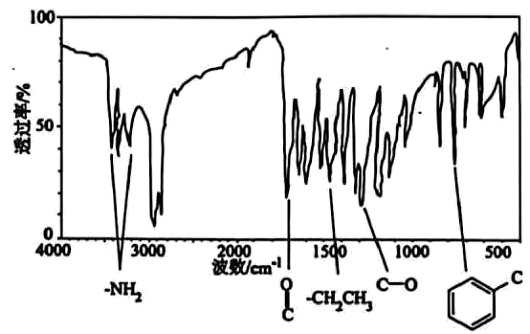 (1)、有机物完全燃烧生成二氧化碳、水和氮气,求该有机物的分子式(写出计算过程)。(2)、有机物A的核磁共振氢谱有5个峰且面积之比为3:2:2:2:2:2,该有机物的结构简式为。(3)、有机物A与氢氧化钠溶液反应的化学方程式为。(4)、有机物的一种芳香族同分异构体具有三种不同化学环境的氢,写出两种满足条件的同分异构体结构简式。
(1)、有机物完全燃烧生成二氧化碳、水和氮气,求该有机物的分子式(写出计算过程)。(2)、有机物A的核磁共振氢谱有5个峰且面积之比为3:2:2:2:2:2,该有机物的结构简式为。(3)、有机物A与氢氧化钠溶液反应的化学方程式为。(4)、有机物的一种芳香族同分异构体具有三种不同化学环境的氢,写出两种满足条件的同分异构体结构简式。 -
7、按要求回答下列问题:(1)、用系统命名法命名:
①
 :。②
:。②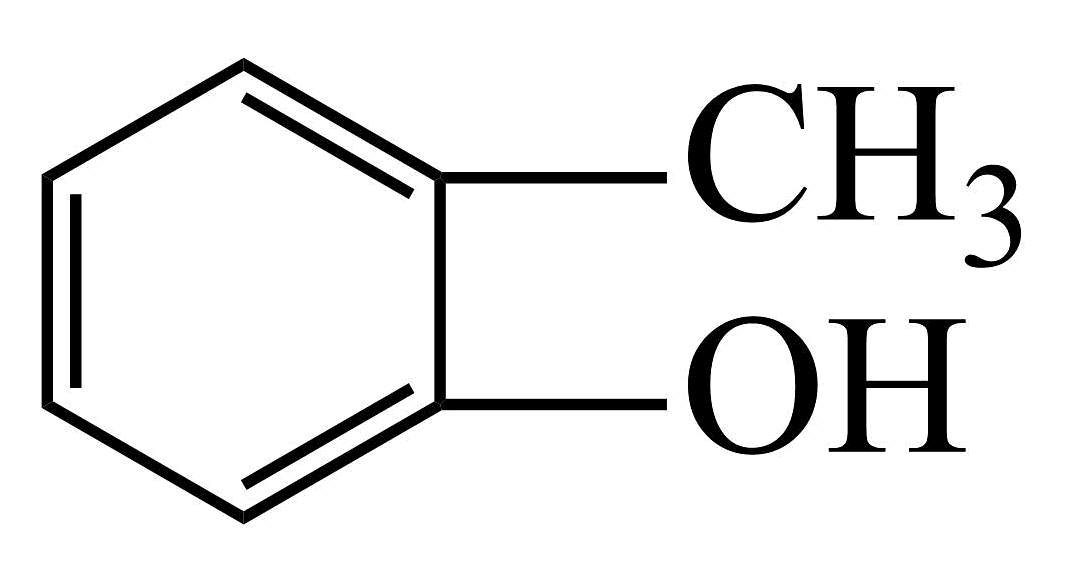 :。(2)、分子式为的芳香烃,苯环上的二氯代物有3种,其结构简式是。(3)、完成下列反应的化学方程式。
:。(2)、分子式为的芳香烃,苯环上的二氯代物有3种,其结构简式是。(3)、完成下列反应的化学方程式。①1,3-丁二烯与氯气发生1,4-加成:。
②甲苯与浓硫酸、浓硝酸的混合酸在100℃共热制得TNT:。
③向苯酚钠溶液中通入少量:。
④对苯二甲酸与乙二醇合成高分子化合物聚对苯二甲酸乙二酯:。
(4)、已知: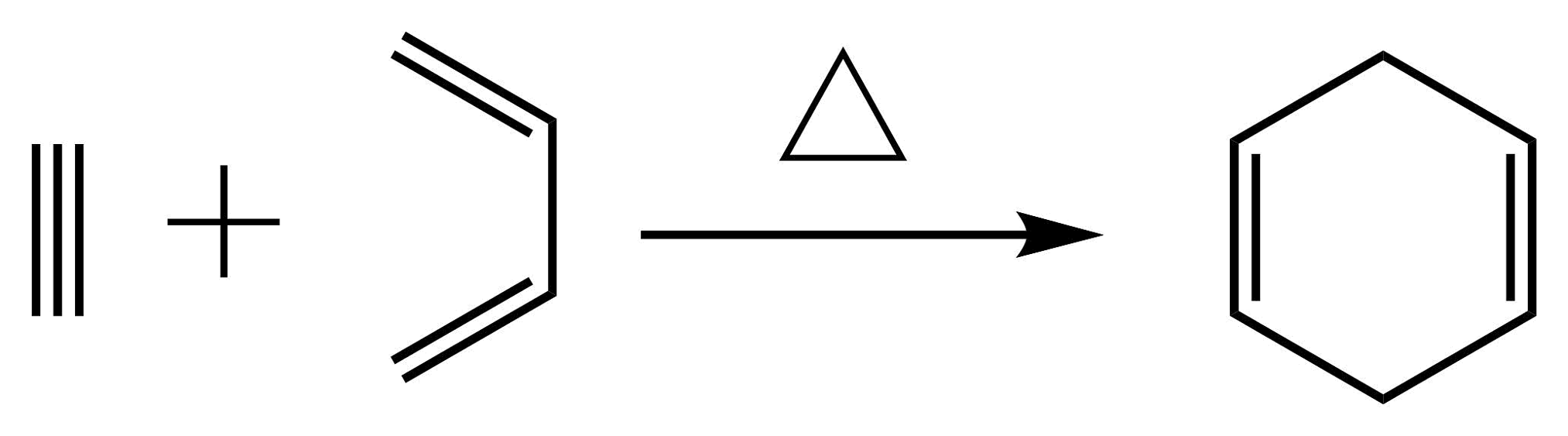 , 合成
, 合成 所用的原料是(用键线式表示)。
所用的原料是(用键线式表示)。 -
8、药品是一种免疫调节剂,其合成路线如下。下列说法正确的是
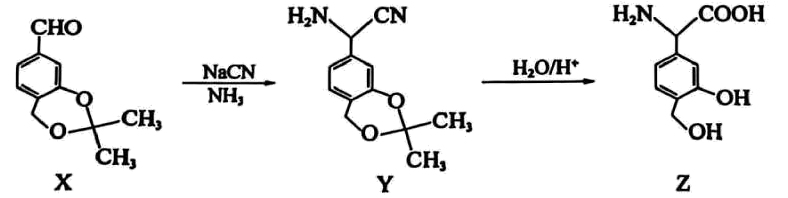 A、X分子中所有原子可能共平面 B、分子中含有2个手性碳原子 C、最多能与反应 D、可以用酸性溶液检验中是否含有
A、X分子中所有原子可能共平面 B、分子中含有2个手性碳原子 C、最多能与反应 D、可以用酸性溶液检验中是否含有 -
9、葫芦脲在超分子化学和材料科学中发挥着重要的作用。葫芦[7]脲的合成路线如下图所示,试剂和试剂均能发生银镜反应。

下列说法不正确的是
A、E与试剂a反应中二者消耗的物质的量之比为2:1 B、F、G互为同系物 C、试剂a、b的核磁共振氢谱均仅有一组峰 D、由为原料制取生成 -
10、根据下列实验操作和现象得出的结论正确的是
选项
实验操作和现象
结论
A
将少量某卤代烃与溶液混合共热,充分反应并冷却后,向溶液中加稀酸化,再滴加溶液,产生淡黄色沉淀
该卤代烃含溴元素
B
向可能含有少量苯酚的苯中滴加过量的浓溴水,未出现白色沉淀
苯中不含苯酚
C
在试管中取约溶液,加入5滴溶液,振荡后加入有机物溶液并加热,无砖红色沉淀产生
X中不含醛基
D
在试管中取少量滴有酚酞的氢氧化钠溶液,向其中滴入有机液体直至过量,溶液颜色褪去
X中含有羧基
A、A B、B C、C D、D -
11、下列有关乙酸乙酯制备实验的说法正确的是
 A、加热有利于加快反应速率,应尽可能提供较高温度 B、反应一段时间后红色溶液上方出现油状液体,其中不含密度比水大的乙酸 C、取出试管B并充分振荡后上层油状液体体积减少,部分乙酸乙酯溶解于下层溶液 D、向振荡后红色褪去的下层溶液中滴入酚酞后又出现红色,说明酚酞溶于乙酸乙酯
A、加热有利于加快反应速率,应尽可能提供较高温度 B、反应一段时间后红色溶液上方出现油状液体,其中不含密度比水大的乙酸 C、取出试管B并充分振荡后上层油状液体体积减少,部分乙酸乙酯溶解于下层溶液 D、向振荡后红色褪去的下层溶液中滴入酚酞后又出现红色,说明酚酞溶于乙酸乙酯 -
12、酸性条件下,环氧乙烷水合法制备乙二醇涉及的机理如图:
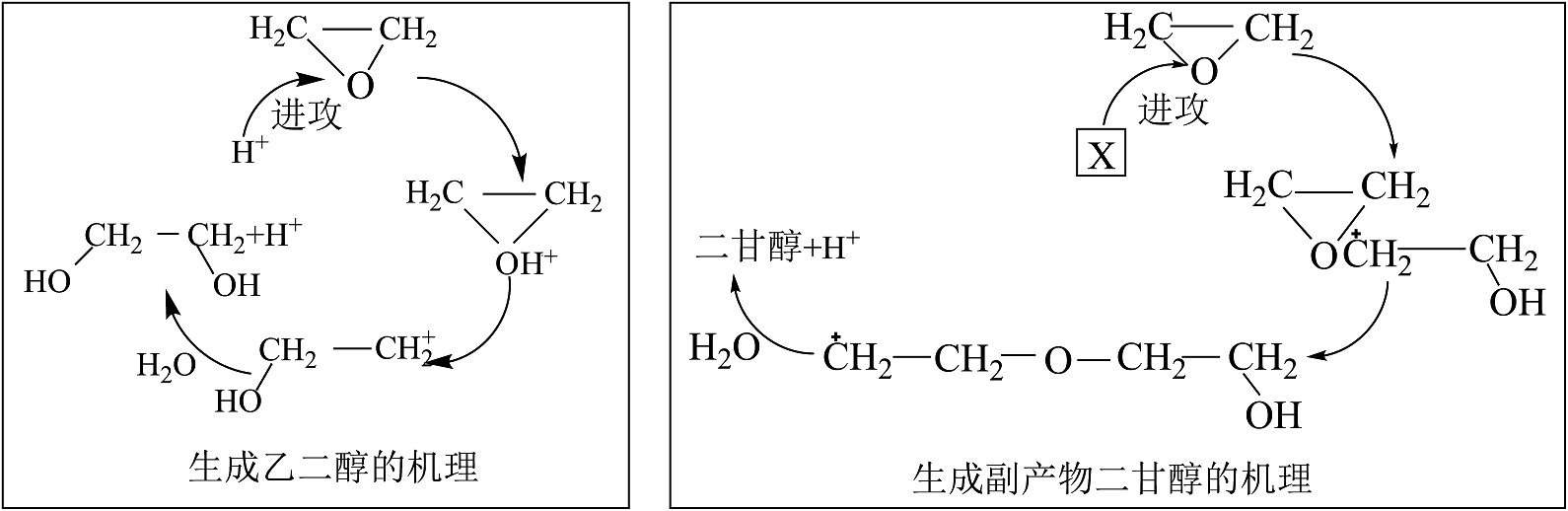
下列说法不正确的是
A、的结构简式为: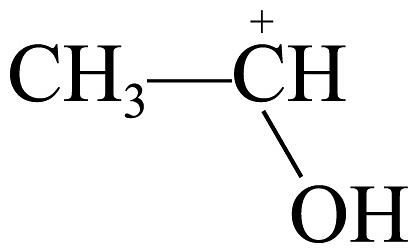 B、进攻环氧乙烷中的氧原子是因为碳氧键的共用电子对偏向氧
C、在制备乙二醇的反应中起催化作用
D、二甘醇是乙二醇发生分子间脱水反应的产物
B、进攻环氧乙烷中的氧原子是因为碳氧键的共用电子对偏向氧
C、在制备乙二醇的反应中起催化作用
D、二甘醇是乙二醇发生分子间脱水反应的产物
-
13、有机小分子通过选择性催化聚合可分别得到聚合物和 , 下列说法不正确的是
 A、X的结构简式为
A、X的结构简式为 B、Z中含有的官能团为酯基和碳碳双键
C、由生成的反应为缩聚反应
D、能在溶液中降解为小分子而不能
B、Z中含有的官能团为酯基和碳碳双键
C、由生成的反应为缩聚反应
D、能在溶液中降解为小分子而不能
-
14、按下图实验装置(部分装置略)对有机样品进行元素分析。样品完全灼烧并将所有气体产物充分吸收后,管增重管增重。质谱法测得该有机物的相对分子质量为118。下列说法正确的是
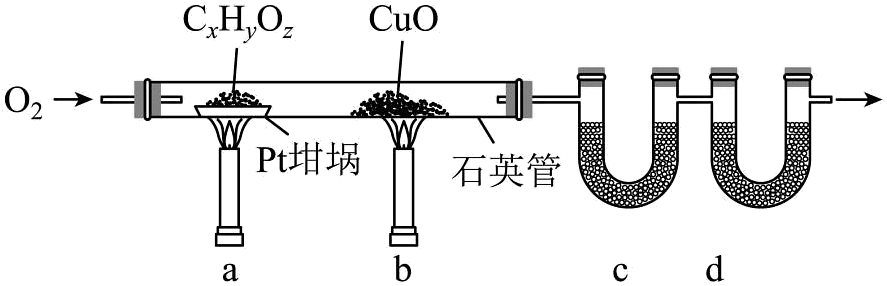 A、先通入氧气,再先后点燃a、b处煤气灯 B、中使用碱石灰吸收反应产生的 C、若撤去可能导致测得中值偏大 D、该有机物的分子式为
A、先通入氧气,再先后点燃a、b处煤气灯 B、中使用碱石灰吸收反应产生的 C、若撤去可能导致测得中值偏大 D、该有机物的分子式为 -
15、乙烯使溴水快速褪色的反应历程如图所示:

已知:①乙烯使溴的四氯化碳溶液褪色比该反应慢得多;②完全反应后两种产物含量分别为10.2%和89.8%。下列说法不正确的是
A、对乙烯与溴加成生成1,2-二溴乙烷的反应具有催化作用 B、中间产物 中所有原子最外层均达到稳定结构
C、反应Ⅱ得到两种产物含量不同的原因是溴水中浓度大于
D、乙烯与溴水反应产物应有1-溴乙醇次溴酸酯
中所有原子最外层均达到稳定结构
C、反应Ⅱ得到两种产物含量不同的原因是溴水中浓度大于
D、乙烯与溴水反应产物应有1-溴乙醇次溴酸酯
-
16、下列有机物的命名正确的是
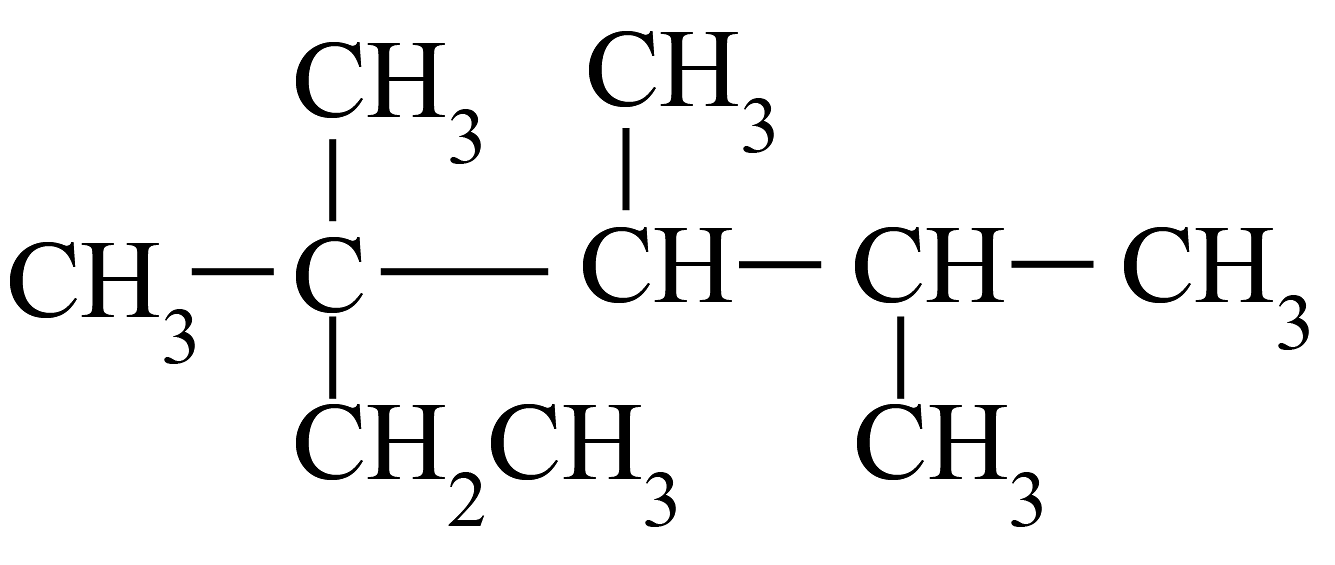

A.2,3,4-三甲基-2-乙基戊烷
B.1,3-二丙醇
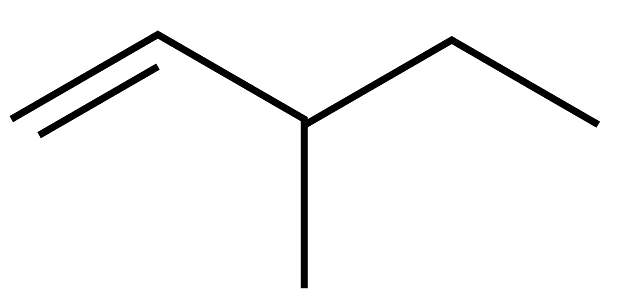
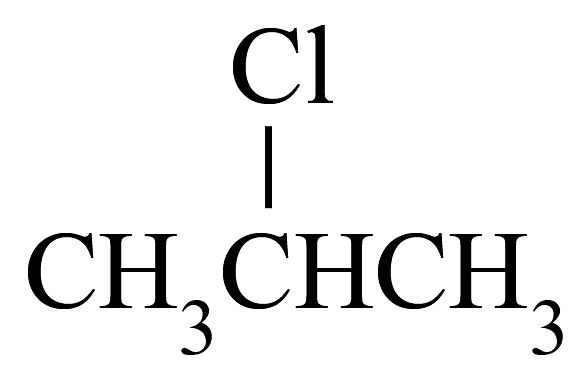
C.3-乙基-1-丁烯
D.2-氯丙烷
A、A B、B C、C D、D -
17、下列装置或操作能达到相应实验目的的是
 A、配制银氨溶液 B、比较碳酸与苯酚酸性强弱 C、制取少量乙二酸 D、分离硝基苯和苯
A、配制银氨溶液 B、比较碳酸与苯酚酸性强弱 C、制取少量乙二酸 D、分离硝基苯和苯 -
18、有关石油和煤的说法不正确的是A、石油加工可获得乙烯 B、煤加工可获得苯 C、石油的分馏、裂化裂解均为物理变化 D、煤的干馏、气化和液化均为化学变化
-
19、下列化学用语错误的是A、甲醛分子的电子式:
 B、聚丙烯的结构简式:
B、聚丙烯的结构简式: C、2-乙基-1,3-丁二烯的键线式:
C、2-乙基-1,3-丁二烯的键线式: D、丙烷分子的球棍模型:
D、丙烷分子的球棍模型: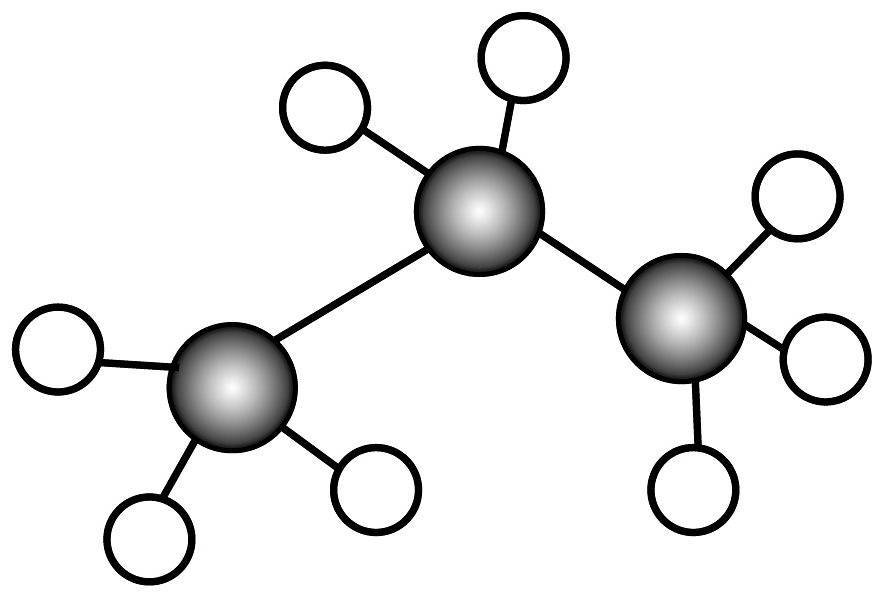
-
20、化学与生产、生活、环境等密切相关,下列说法正确的是A、推广使用可降解塑料制品是为了防止白色污染 B、医疗上用95%的酒精或福尔马林稀溶液杀菌消毒 C、“泡腾片实验”中柠檬酸与小苏打反应是因为柠檬酸具有强还原性 D、制作户外运动服装所需要高强度和耐磨性的锦纶(聚酰胺纤维)是纯净物