相关试卷
-
1、某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 , 进一步处理得到产品和 , 实验流程如图,下列说法正确的是( )
 A、步骤①离子方程式为: B、步骤①获得的操作为蒸发、结晶、过滤、洗涤、干燥 C、煅烧制是的非氧化还原反应 D、流程中只有能循环使用
A、步骤①离子方程式为: B、步骤①获得的操作为蒸发、结晶、过滤、洗涤、干燥 C、煅烧制是的非氧化还原反应 D、流程中只有能循环使用 -
2、羟醛缩合反应是一种常用的增长碳链的方法。一种合成目标产物
 (图中⑦)的反应机理如图所示,下列说法错误的是( )
(图中⑦)的反应机理如图所示,下列说法错误的是( ) A、①与酸或碱均能发生反应 B、③是该反应的中间产物 C、⑥到⑦的过程中有非极性键的断裂和生成 D、总反应的原子利用率为
A、①与酸或碱均能发生反应 B、③是该反应的中间产物 C、⑥到⑦的过程中有非极性键的断裂和生成 D、总反应的原子利用率为 -
3、下列实验装置可以达到实验目的的是( )
A
B
C
D




蒸干CuCl2溶液可制得CuCl2固体
量取20.00mL未知浓度的草酸
实验室制NH3
比较非金属性:Cl>C>Si
A、A B、B C、C D、D -
4、一种工业洗涤剂中间体结构式如图所示,其中短周期元素X、Q、Z、Y、W原子序数依次增大,X和W同主族但不相邻,Y和Q最外层电子数之和是Z原子L层电子数的二倍,下列说法正确的是( )
 A、X2Y和X2Y2均为极性分子 B、第一电离能:Y>Z>Q C、原子半径:Y>Z>Q D、W与Y形成的化合物中只含离子键
A、X2Y和X2Y2均为极性分子 B、第一电离能:Y>Z>Q C、原子半径:Y>Z>Q D、W与Y形成的化合物中只含离子键 -
5、我国学者开发了一种新型高效的催化剂,大幅度降低了电解所需的电压,同时可将气体变废为宝,其工作原理如图所示,下列说法正确的是( )
 A、电极与电源负极相连 B、吸收的反应的离子方程式为 C、交换膜为质子交换膜,电解时由流向 D、标况下,若电极上生成 , 理论上中可处理分子
A、电极与电源负极相连 B、吸收的反应的离子方程式为 C、交换膜为质子交换膜,电解时由流向 D、标况下,若电极上生成 , 理论上中可处理分子 -
6、下列关于物质结构或性质及解释存在错误的是( )
选项
物质结构或性质
解释
A
键角:
CO2中C原子为sp杂化,为直线形分子;CH4中C原子为sp3杂化,为正四面体形分子
B
稳定性:
分子间可以形成氢键,没有氢键
BF3与NH3形成[H3N→BF3]
中的有空轨道接受中的孤电子对
D
冠醚能加快KMnO4与环己烯的反应速率
冠醚上不同大小的空穴适配不同大小的碱金属离子,冠醚通过与K+结合将带入有机相,起到催化剂的作用
A、A B、B C、C D、D -
7、MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为:

下列说法正确的是( )
A、中所有原子均可共面 B、TOME与足量加成后,手性碳原子数目增加 C、甲醇和乙二醇互为同系物,两者的核磁共振氢谱均有2组峰 D、三种物质均可和溶液反应 -
8、管道工人曾经用浓氨水检验氯气管道是否漏气: , 设为阿伏加德罗常数的值,下列说法正确的是( )A、中含有个键 B、每生成 , 转移个电子 C、氧化剂与还原剂数目比为 D、溶液中含有数目为
-
9、下列“类比”、“推理”合理的是( )A、与反应生成 , 则与反应可生成 B、工业上通过电解熔融的冶炼 , 则可以通过电解熔融的冶炼 C、是酸性氧化物,则也是酸性氧化物 D、与反应生成和 , 则与反应生成和
-
10、下列物质的应用或鉴别与氧化还原反应无关的是( )A、用食醋除水垢 B、用溶液检验是否变质 C、工业上用硅石制取粗硅 D、加热条件下用银氨溶液检验中是否混有
-
11、下列化学用语表达正确的是( )A、胆矾的化学式为 B、的结构示意图:
 C、的电子式
C、的电子式 D、的球棍模型:
D、的球棍模型:
-
12、化学与生活密切相关,下列说法正确的是( )A、活性炭具有杀菌消毒的作用 B、小苏打的主要成分是碳酸钠 C、芯片主要成分为高纯度硅 D、塑料属于天然高分子材料
-
13、水合肼在储氢领域有广阔的应用前景,其水溶液呈弱碱性。(1)、分子有顺式、反式和交互式三种比较稳定的空间构型。下列结构能表示分子交互式的是(填序号)。
 (2)、肼分解制氢的主要反应为 , 肼的理论储氢密度。测得肼实际分解时产生的气体中含 , 肼实际储氢密度小于理论值的原因是(用化学方程式表示)。(3)、水合肼制氢过程中涉及肼在催化剂表面分解,如图1所示。
(2)、肼分解制氢的主要反应为 , 肼的理论储氢密度。测得肼实际分解时产生的气体中含 , 肼实际储氢密度小于理论值的原因是(用化学方程式表示)。(3)、水合肼制氢过程中涉及肼在催化剂表面分解,如图1所示。
图1
①X的结构简式为。
②催化剂表面存在和两种活性位点,两种活性位点分别带不同电性的电荷。肼中的氢原子吸附于(填“”或“”)活性位点。已知:键、键的键能分别是。肼在该催化剂表面反应断裂的化学键不是键,而是键,原因是。
③催化剂存在下,不同浓度的分解时,测得随时间的变化如图2所示。当浓度从增加到时,反应速率加快;从增加到时,反应速率几乎不变。其原因是。

图2
-
14、深共晶溶剂(DESs)可从中回收锂。(1)、DESs的制备。将乙二醇()与氯化胆碱(
 )按一定比例混合搅拌至形成均一透明液体,制得DESs。
)按一定比例混合搅拌至形成均一透明液体,制得DESs。
图1
①DESs由含氢键供体(能形成氢键的氢原子)的组分与含氢键受体(能与氢原子形成氢键的原子)的组分混合。乙二醇分子中氢键供体的数目为。
②不同配比氯化胆碱与乙二醇混合的二元相图如图1所示。相同条件下,氯乙二醇的熔点乙二醇的熔点(填“>”“二”或“<”)。制备熔点达到最低值的DESs时,氯化胆碱与乙二醇的物质的量之比为。
(2)、氧化浸出锂。将与按照一定比例混合,再通入。实验装置如图所示。①冷凝管的作用为。
图2
 图3
图3
②主要反应机理如图3所示:
Ⅰ中碳原子轨道杂化类型的变化为;M的化学式为。
(3)、碳酸锂的制备。已知: , 完全沉淀时离子浓度小于;易溶于水;的溶解度:为为为。补充完整由粗溶液(含少量)制备的实验方案:向粗溶液中 , 得到固体。
(须使用的试剂:溶液、溶液)
-
15、化合物是合成一种激酶抑制剂的中间体,其合成路线如下:
 (1)、反应涉及的反应物有;a.溶液;b.盐酸;c.浓、浓。
(1)、反应涉及的反应物有;a.溶液;b.盐酸;c.浓、浓。①加入反应物的正确顺序是:c、、(填字母)。
②硝化反应的机理可表示为:

反应中浓硫酸的作用是。
(2)、的分子式为 , 结构简式为。(3)、已知: , TEA为 , 能促进该反应的进行。能促进反应进行的原因是。(4)、写出同时满足下列条件的A的一种同分异构体的结构简式。碱性条件水解后酸化生成两种产物,产物之一能与溶液发生显色反应,两种产物的核磁共振氢谱中都有2个峰。
(5)、写出以 、
、 为原料制备
为原料制备 的合成路线流程图(无机试剂和有机溶剂任用)。
的合成路线流程图(无机试剂和有机溶剂任用)。 -
16、镓及其化合物在半导体、光电材料等领域有广泛应用。(1)、以酸性含溶液(含少量)为原料通过除杂等一系列操作制得粗镓,粗镓经过电解精炼制得高纯镓。体系中含镓微粒的物质的量分数随的关系如图1所示。已知:。
①的基态核外电子排布式为.
②“除杂”包括加入溶液调节、加入足量除去和、过滤等步骤。调节溶液的目的为。
③“电解精炼”时,以粗镓为阳极,含的碱性溶液为电解液,阴极析出镓的电极反应式为;阴极同时有少量气体产生。测得电解过程溶液中镓浓度与电流效率()随时间的变化如图2所示。反应后,降低的原因是。
图1
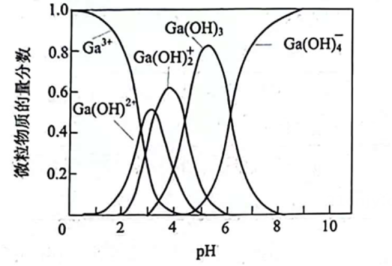 图2
图2 (2)、具有优异的光电性能,可由与发生反应制得。
(2)、具有优异的光电性能,可由与发生反应制得。①制得GaN时生成一种有机物的化学式为。
②的一种晶胞如图3所示。晶体中距离最近且相等的的数目为。

图3
③准确称取样品,加入溶液,加热使固体充分溶解,用足量溶液吸收产生的。向吸收液中滴加指示剂,用的盐酸滴定至终点,消耗盐酸。
过程中涉及反应:; , 计算样品的纯度(写出计算过程)。
-
17、为研究反应在不同条件下的转化率,向恒压反应器中通入含一定浓度与的气体,在无催化剂和有催化剂存在时,分别测得不同温度下反应器出口处NO的转化率如图中曲线a、b所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )
 A、反应的 B、曲线a中转化率随温度升高而增大,是由于催化剂的活性增强 C、曲线中从点到点,转化率随温度升高而减小,是由于反应速率减慢 D、催化剂存在时,其他条件不变,增大气体中 , NO转化率随温度的变化为曲线c
A、反应的 B、曲线a中转化率随温度升高而增大,是由于催化剂的活性增强 C、曲线中从点到点,转化率随温度升高而减小,是由于反应速率减慢 D、催化剂存在时,其他条件不变,增大气体中 , NO转化率随温度的变化为曲线c -
18、从炼钢粉尘(主要含)中回收锌的过程如图所示。“浸取”过程转化为 , 并有少量铁元素浸出。已知: , 。下列说法正确的是( )
 A、的溶液中: B、溶液中: C、“沉锌”过程中,溶液的减小 D、“沉锌”后的溶液中:
A、的溶液中: B、溶液中: C、“沉锌”过程中,溶液的减小 D、“沉锌”后的溶液中: -
19、 , 探究溶液的性质。下列实验方案能达到探究目的的是( )
选项
探究目的
实验方案
A
钾元素的焰色试验
用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色
B
是否有还原性
向溶液中滴加氯水,再滴入溶液,观察是否有白色沉淀产生
C
是否水解
向溶液中滴加2~3滴酚酞试液,观察溶液颜色的变化
D
比较溶液中与的大小
用计测量溶液的
A、A B、B C、C D、D -
20、化合物Y是合成丹参醇的中间体,其合成路线如下:

下列说法正确的是( )
A、X分子中含手性碳原子 B、X转化为的过程中 与反应生成
与反应生成 C、与以物质的量发生加成反应时可得3种产物
D、X、Y可用酸性溶液进行鉴别
C、与以物质的量发生加成反应时可得3种产物
D、X、Y可用酸性溶液进行鉴别