相关试卷
-
1、硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO
② Ksp(MgF2)=6.4×10-10(mol/L)3;Ksp(CaF2)=3.6×10-12(mol/L)3
③离子浓度≤10-5mol·L-1时,离子沉淀完全。请回答:
(1)、“氧化”时,发生反应的离子方程式为。(2)、“中和除杂”时,生成沉淀的主要成分为(填化学式)。(3)、“氟化除杂”时,使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于 mol/L。(4)、“碳化结晶”时,发生反应的离子方程式为。(5)、用惰性电极电解MnSO4溶液可制备MnO2 , 电解过程中阳极的电极反应式为。 -
2、12.5g CuSO4﹒5H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如下图所示。

请回答下列问题:
(1)、试确定200℃时固体物质的化学式。(2)、取270℃所得样品,于570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为。把该黑色粉末溶解于稀硫酸中,经浓缩、冷却,有蓝色晶体析出,该晶体的化学式为 , 其存在的最高温度是。(3)、若在0.05mol·L-1硫酸铜溶液中通入足量 H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的pH值约为。 -
3、磷化氢(PH3)是粮食储备常用的高效熏蒸杀虫剂。(1)、AlP遇水发生复分解反应生成PH3气体和(填化学式)。(2)、PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:。
□CuSO4+□PH3+□H2O = □Cu3P↓+□H3PO4+□H2SO4
(3)、工业制备PH3的原理如图所示:
①白磷和烧碱溶液反应的化学方程式为。
②从分类来看,NaH2PO2属于。
A.正盐B.酸式盐C.强电解质D.弱电解质
③NaH2PO2可将溶液中的Ag+还原为银,从而用于化学镀银。已知利用此原理进行化学镀银时氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为 (填化学式)。
-
4、常温下,均为2、体积均为的溶液,分别加水稀释至体积为 , 溶液随的变化关系如图所示,下列叙述错误的是( )
 A、常温下:Ka(HB) > Ka(HC) B、的电离度:a点< b点 C、当时,升高温度,减小 D、恰好中和均为2、体积均为V0的三种酸溶液,消耗的NaOH溶液一样多
A、常温下:Ka(HB) > Ka(HC) B、的电离度:a点< b点 C、当时,升高温度,减小 D、恰好中和均为2、体积均为V0的三种酸溶液,消耗的NaOH溶液一样多 -
5、可逆反应A(g)+xB(g)2C(g) 达平衡后,只改变反应的一个条件,测得容器中部分物质的浓度、反应速率随时间变化如下图所示。下列说法中正确的是( )
 A、8min时反应达到平衡状态 B、该反应正反应为吸热反应 C、x=1 D、30min~40min间使用了催化剂
A、8min时反应达到平衡状态 B、该反应正反应为吸热反应 C、x=1 D、30min~40min间使用了催化剂 -
6、图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误的是( )
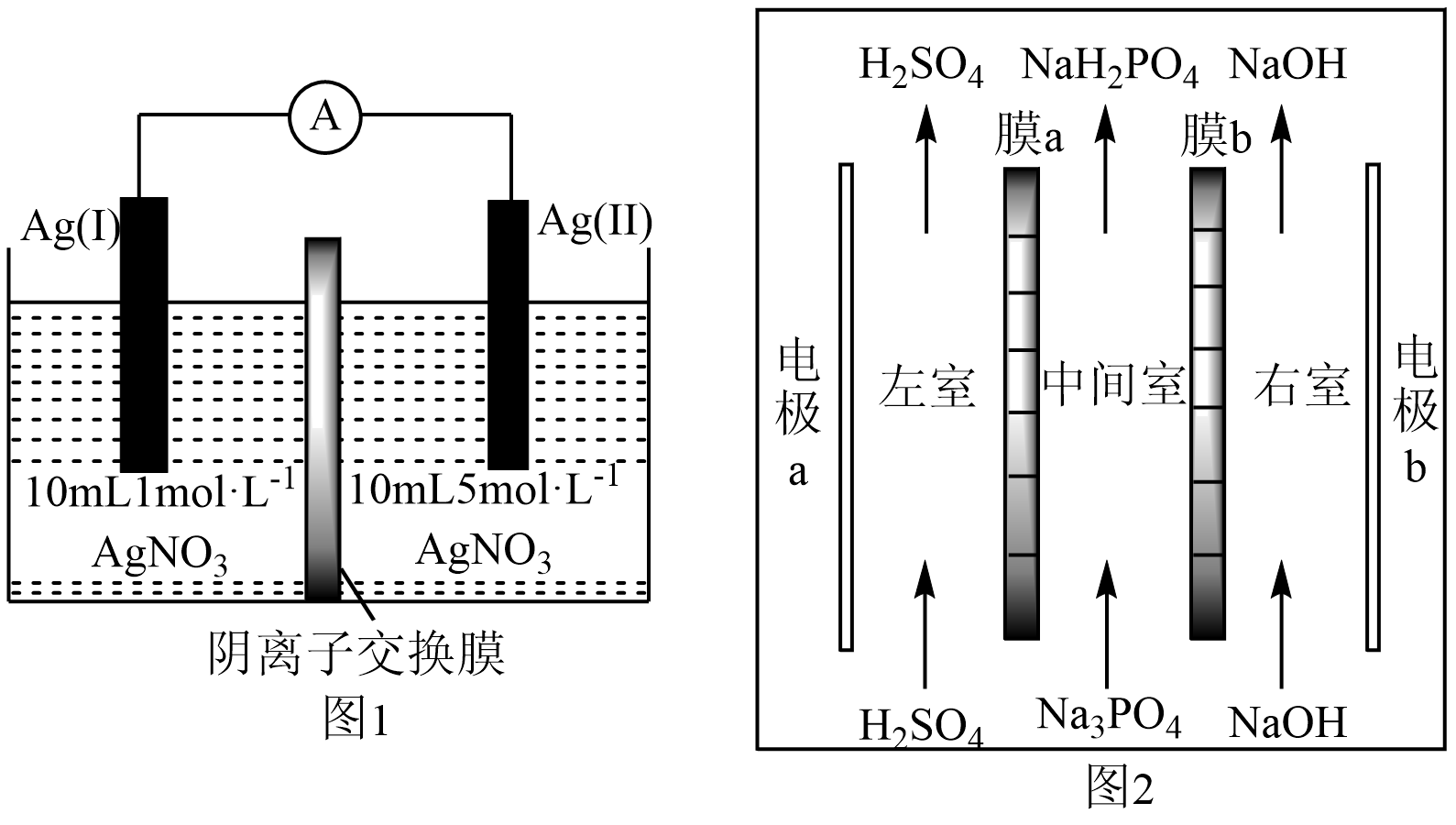 A、电极a应与Ag(II)相连 B、电渗析装置中膜b为阳离子交换膜 C、电渗析过程中左、右室中H2SO4和NaOH的浓度均增大 D、电池从开始到停止放电,理论上可制备2.4gNaH2PO4
A、电极a应与Ag(II)相连 B、电渗析装置中膜b为阳离子交换膜 C、电渗析过程中左、右室中H2SO4和NaOH的浓度均增大 D、电池从开始到停止放电,理论上可制备2.4gNaH2PO4 -
7、利用无机物离子[(L)RuⅢ(H2O)]5-和CeⅣ , 实现了利用水制氧气。用H218O进行同位素标记实验,证明了产物氧气中的氧原子完全来自水,其相关机理如图所示。下列说法错误的是( )
 A、CeⅣ在反应中作氧化剂 B、催化氧化水的反应为2H2O O2↑+2H2↑ C、进行同位素标记实验前需排尽体系中的空气 D、若H218O参与反应,则[(L)RuⅢOOH]6-中存在18O
A、CeⅣ在反应中作氧化剂 B、催化氧化水的反应为2H2O O2↑+2H2↑ C、进行同位素标记实验前需排尽体系中的空气 D、若H218O参与反应,则[(L)RuⅢOOH]6-中存在18O -
8、利用传感技术可探究压强对2NO2(g) N2O4(g)化学平衡移动的影响。往注射器中充入适量NO2气体如图甲所示;再分别在t1、t2时快速移动注射器活塞并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法中错误的是( )
 A、在B、E两点,对应的正反应速率: B、C到D点,平衡逆向移动,针筒内气体颜色比点深 C、在E,F,H三点中,H点的气体平均相对分子质量最大 D、B点处NO2的转化率为6%
A、在B、E两点,对应的正反应速率: B、C到D点,平衡逆向移动,针筒内气体颜色比点深 C、在E,F,H三点中,H点的气体平均相对分子质量最大 D、B点处NO2的转化率为6% -
9、除去括号内杂质所用试剂和方法均正确的是( )
选项
物质
所用试剂
方法
A
乙醇(水)
新制生石灰
蒸馏
B
甲烷(乙烯)
酸性高锰酸钾溶液
洗气
C
乙酸乙酯(乙酸)
氢氧化钠溶液
分液
D
饱和碳酸钠溶液
过滤
A、A B、B C、C D、D -
10、把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,首先观察到溶液变红的区域是( )
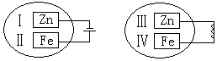 A、Ⅰ和Ⅲ附近 B、Ⅱ和Ⅲ附近 C、Ⅰ和Ⅳ附近 D、Ⅱ和Ⅳ附近
A、Ⅰ和Ⅲ附近 B、Ⅱ和Ⅲ附近 C、Ⅰ和Ⅳ附近 D、Ⅱ和Ⅳ附近 -
11、MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):

下列说法错误的是( )
A、ΔH1(MgCO3)>ΔH1(CaCO3)>0 B、ΔH2(MgCO3)=ΔH2(CaCO3)>0 C、ΔH1(CaCO3)-ΔH1(MgCO3)=ΔH3(CaO)-ΔH3(MgO) D、ΔH1+ΔH2>ΔH3 -
12、下列实验方案设计正确的是( )
选项
实验目的
实验方案
A
测定NaClO溶液的pH
取一张 pH 试纸放在表面皿上,用洁净的玻璃棒蘸取待测液滴于试纸的中部,与标准比色卡对比
B
探究浓度大小对反应速率的影响
取等体积不同浓度的KMnO4溶液,分别加入等体积等浓度的H2C2O4溶液,观察褪色的快慢
C
检验CH3CH2Br 中的溴原子
取少量CH3CH2Br与NaOH 水溶液共热,冷却,再加AgNO3溶液,观察产生沉淀的颜色
D
探究KI与FeCl3反应的限度
取5mL 0.1mol/L KI溶液于试管中,加入1mL 0.1 mol/L FeCl3溶液,充分反应后再加KSCN溶液,观察现象
A、A B、B C、C D、D -
13、以氯酸钠(NaClO3)等为原料制备亚氯酸钠(NaClO2)的工艺流程如下,下列说法中,不正确的是( )
 A、反应1中,每生成1molClO2有0.5molSO2被氧化 B、从母液中可以提取Na2SO4 C、反应2中,氧化剂与还原剂的物质的量之比为1∶2 D、采用减压蒸发可能是为了防止NaClO2受热分解
A、反应1中,每生成1molClO2有0.5molSO2被氧化 B、从母液中可以提取Na2SO4 C、反应2中,氧化剂与还原剂的物质的量之比为1∶2 D、采用减压蒸发可能是为了防止NaClO2受热分解 -
14、下列各组离子在指定溶液中可能大量共存的是( )A、中性溶液中:Fe3+、Al3+、、 B、lg=1010的溶液中:Na+、K+、CH3COO-、ClO- C、常温下由水电离出的c(H+)=10-13mol/L的溶液中:K+、Na+、、[Al(OH)4]- D、加入铝粉会产生H2的溶液中:Cu2+、Mg2+、、Cl-
-
15、如图是硫酸试剂瓶标签上的部分内容。下列说法正确的是( )
 A、该硫酸的物质的量浓度为9.2mol·L-1 B、该硫酸与等体积的水混合所得溶液的质量分数小于49% C、配制250mL 4.6mol·L-1的稀硫酸需取该硫酸62.5 mL D、用该硫酸配置250mL 4.6mol·L-1的稀硫酸,若量取该硫酸时仰视,则所配稀硫酸浓度偏小
A、该硫酸的物质的量浓度为9.2mol·L-1 B、该硫酸与等体积的水混合所得溶液的质量分数小于49% C、配制250mL 4.6mol·L-1的稀硫酸需取该硫酸62.5 mL D、用该硫酸配置250mL 4.6mol·L-1的稀硫酸,若量取该硫酸时仰视,则所配稀硫酸浓度偏小 -
16、下列指定反应的离子方程式错误的是( )A、向氢氧化镁悬浊液中加氯化铵溶液,加热沉淀溶解: B、用Na2CO3溶液处理水垢中的CaSO4: C、Na2SO3溶液吸收少量Cl2: D、Mg(HCO3)2溶液与过量NaOH溶液反应:
-
17、设NA为阿伏加德罗常数的值,下列说法错误的是( )A、标准状况下,2.24LCl2通入足量的水充分反应,溶液中N(Cl-)+N(HClO)+N(ClO-)的数目和为0.2NA B、反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol,若放出热量46.2kJ,则转移的电子数目为3NA C、常温下,1L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10-5NA D、将0.2 mol NH4Cl固体溶于一定量稀氨水,所得溶液呈碱性,则溶液中含数目大于0.2NA
-
18、下列叙述中,错误的是( )A、固体氯化钠不能导电,但氯化钠是电解质 B、纯水的pH值随温度的升高而降低 C、pH= (为水的离子积常数)的溶液一定呈中性 D、用大量水稀释溶液,溶液中所有离子浓度都要减小
-
19、环氧乙烷(
 , 简称EO)是在有机合成中常用的试剂。EO常温下易燃易爆,其爆炸极限为3~100%。近年来,常用以乙烯、氧气、氮气混合气投料的乙烯氧化法制备EO。部分涉及反应为:
, 简称EO)是在有机合成中常用的试剂。EO常温下易燃易爆,其爆炸极限为3~100%。近年来,常用以乙烯、氧气、氮气混合气投料的乙烯氧化法制备EO。部分涉及反应为:主反应:
副反应:
(1)、已知 , 则EO的燃烧热为。(2)、在温度为T,压强为的环境下,欲提高乙烯的平衡转化率,需体系中氮气分压(填“增大”或“减小”)。但在实际生产中并非如此,其可能原因是。(3)、向温度为T,体积为V的容器中加入投料比为2:3:28的乙烯、氧气、氮气。已知平衡后: , (其中二碳化合物为分子中含两个碳原子的化合物)。忽略其他反应,乙烯的平衡转化率为 , 副反应的平衡常数为。(4)、以Ag为催化剂的反应机理如下:反应Ⅰ: 慢
反应Ⅱ: 快
反应Ⅲ: 快
①定能够提高主反应反应速率的措施有(填标号)。
A.降低温度 B.通入惰性气体
C.增大浓度 D.增大浓度
②加入1,2-二氯乙烷会发生。一定条件下,反应经过一定时间后,EO产率及选择性与1,2-二氯乙烷浓度关系如图。1,2-二氯乙烷能使EO产量先增加后降低的原因是。

-
20、铋酸钠( , Mr=280g/mol)是一种新型有效的光催化剂,也被广泛应用于制药业。某兴趣小组设计实验制取铋酸钠并探究其应用。
Ⅰ.制取铋酸钠
利用白色且难溶于水的在NaOH溶液中,在充分搅拌的情况下与反应制备 , 实验装置如下图(加热和夹持仪器已略去)。
已知:粉末呈浅黄色,不溶于冷水,遇沸水或酸溶液迅速分解。
请按要求回答下列问题:
 (1)、仪器C的名称是。(2)、B装置盛放的试剂是。(3)、C中发生的反应化学方程式为:。(4)、当观察到C中白色固体消失时,应关闭和 , 并停止对A加热,原因是。(5)、反应结束后,为从装置C中获得尽可能多的产品,需要的操作是、过滤、洗涤、干燥。(6)、实验完毕后,打开 , 向A中加入NaOH溶液的主要作用是。(7)、Ⅱ.产品纯度的测定
(1)、仪器C的名称是。(2)、B装置盛放的试剂是。(3)、C中发生的反应化学方程式为:。(4)、当观察到C中白色固体消失时,应关闭和 , 并停止对A加热,原因是。(5)、反应结束后,为从装置C中获得尽可能多的产品,需要的操作是、过滤、洗涤、干燥。(6)、实验完毕后,打开 , 向A中加入NaOH溶液的主要作用是。(7)、Ⅱ.产品纯度的测定取Ⅰ中制取的产品xg,加入足量稀硫酸和稀溶液使其完全反应,再用0.1mol/L的标准溶液滴定生成的(已知:),当达到滴定终点时,消耗ymL。该产品的纯度为。