相关试卷
-
1、党的二十大报告强调科技创新是提高社会生产力和综合国力的战略支撑,化学科学与社会、生活息息相关。下列说法正确的是( )A、SiO2具有导电性,可用于制作光导纤维和光电池 B、国产大飞机一C919使用的碳纤维是一种有机高分子材料 C、海水提溴、煤的液化都涉及化学变化 D、汉朝淮南王刘安发明的“石膏点豆腐”,说明硫酸钙能使蛋白质变性
-
2、如图是苯和溴的取代反应的实验装置图,其中A为具支试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉。填写下列空白:
 (1)、向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生反应的化学方程式(有机化合物写结构简式):。(2)、要证明A中发生的是取代反应,而不是加成反应,试管C中苯的作用是。反应开始后,观察D和E两支试管,看到的现象分别是、。(3)、反应2~3min后,在B中的氢氧化钠溶液中可观察到的现象是、。(4)、苯是一种重要的化工原料,以下是用苯作为原料制备某些化合物的转化关系图:
(1)、向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生反应的化学方程式(有机化合物写结构简式):。(2)、要证明A中发生的是取代反应,而不是加成反应,试管C中苯的作用是。反应开始后,观察D和E两支试管,看到的现象分别是、。(3)、反应2~3min后,在B中的氢氧化钠溶液中可观察到的现象是、。(4)、苯是一种重要的化工原料,以下是用苯作为原料制备某些化合物的转化关系图:
已知:a.;
b.苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响:
c.
 。
。①A转化为B的化学方程式是。
②由C生成D的反应类型是 , D与H2反应的反应类型是。E的结构简式为。
-
3、如图所示装置是用燃烧法确定有机物化学式的装置,这种方法是电炉加热时利用纯氧氧化管内样品,根据产物的质量确定有机物的组成。回答下列问题:
 (1)、A装置是制备氧气的装置,仪器a的名称 , 若A中注入30%的H2O2溶液,写出A装置中反应的化学方程式。(2)、B装置中浓硫酸的作用是。(3)、D和E中的试剂不可调换,理由是。(4)、若样品中有机物只含C、H、O三种元素中的两种或三种,准确称取0.74g样品,经充分反应后,D管质量增加0.90g,E管质量增加1.76g。则该样品中有机物的最简式为。(5)、通过对样品进行分析,得到如下三张图谱。分析图谱可知,样品中有机物的相对分子质量为 , 官能团是 , 结构简式为。
(1)、A装置是制备氧气的装置,仪器a的名称 , 若A中注入30%的H2O2溶液,写出A装置中反应的化学方程式。(2)、B装置中浓硫酸的作用是。(3)、D和E中的试剂不可调换,理由是。(4)、若样品中有机物只含C、H、O三种元素中的两种或三种,准确称取0.74g样品,经充分反应后,D管质量增加0.90g,E管质量增加1.76g。则该样品中有机物的最简式为。(5)、通过对样品进行分析,得到如下三张图谱。分析图谱可知,样品中有机物的相对分子质量为 , 官能团是 , 结构简式为。 (6)、某同学认为在装置E后加一个盛有碱石灰的U形管,会减少测定误差,你认为这样做是否合理(填“合理”或“不合理”),理由是。
(6)、某同学认为在装置E后加一个盛有碱石灰的U形管,会减少测定误差,你认为这样做是否合理(填“合理”或“不合理”),理由是。 -
4、2022年10月18日《自然化学》发表我国科学家研究成果,发现AgCrS2(AMX2家族成员之一,A
 一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题: (1)、基态硫原子核外电子排布式为。(2)、氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是 , 科学家用亚硒酸盐和硫酸盐跟踪固氨酶,研究反应机理。中硫的杂化轨道类型是 , 的空间结构模型为。(3)、配合物中铬的化合价为 , 配离子为 , 中心离子配位数为。(4)、ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点(0,0,0),B点的坐标为 , 从该晶胞中找出距离B点Se2-最远的的位置(用分数坐标表示),该晶胞中晶胞中的个数为个,若晶胞中的边长为acm,阿伏加德罗常数的值为 , 请计算ZnSe晶胞的密度
一价金属,M为三价金属,X为氧族元素)在室温下具有超离子行为。回答下列问题: (1)、基态硫原子核外电子排布式为。(2)、氧族元素有氧、硫、硒、碲等元素,其中电负性最大的元素是 , 科学家用亚硒酸盐和硫酸盐跟踪固氨酶,研究反应机理。中硫的杂化轨道类型是 , 的空间结构模型为。(3)、配合物中铬的化合价为 , 配离子为 , 中心离子配位数为。(4)、ZnSe晶胞与ZnS晶胞相似(如图),ZnSe晶胞中部分原子的分数坐标为:A点(0,0,0),B点的坐标为 , 从该晶胞中找出距离B点Se2-最远的的位置(用分数坐标表示),该晶胞中晶胞中的个数为个,若晶胞中的边长为acm,阿伏加德罗常数的值为 , 请计算ZnSe晶胞的密度
-
5、如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
 (1)、⑨号元素在周期表的位置是 , 其最高能层的电子占据的原子轨道电子云轮廓为形。(2)、第二周期所有元素中第一电离能介于①②之间的有种。由②③④形成的简单离子半径由小到大顺序是(填化学用语)。(3)、元素②⑧可形成原子个数比为1∶3的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子的空间结构为 , 中心原子轨道杂化形式为 , 该分子为(填“极性分子”或“非极性分子”)。(4)、元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式 , 它的熔点高、硬度大、电绝缘性好、化学性质稳定,它的晶体类型是。(5)、下列有关性质的比较正确的是____(填标号)A、电负性:②>③ B、氢化物的稳定性:③>⑦ C、原子半径:⑤>④ D、氢化物的沸点:③>⑦(6)、⑩可形成的卤化物的熔点如下表:
(1)、⑨号元素在周期表的位置是 , 其最高能层的电子占据的原子轨道电子云轮廓为形。(2)、第二周期所有元素中第一电离能介于①②之间的有种。由②③④形成的简单离子半径由小到大顺序是(填化学用语)。(3)、元素②⑧可形成原子个数比为1∶3的共价化合物,分子中各原子最外层均达到8电子的稳定结构,该分子的空间结构为 , 中心原子轨道杂化形式为 , 该分子为(填“极性分子”或“非极性分子”)。(4)、元素②⑥可形成的化合物是一种性质优良的无机非金属材料,根据元素周期律知识,写出其化学式 , 它的熔点高、硬度大、电绝缘性好、化学性质稳定,它的晶体类型是。(5)、下列有关性质的比较正确的是____(填标号)A、电负性:②>③ B、氢化物的稳定性:③>⑦ C、原子半径:⑤>④ D、氢化物的沸点:③>⑦(6)、⑩可形成的卤化物的熔点如下表:卤化物
氟化物
氯化物
溴化物
熔点/℃
>1000
77.75
122.3
⑩的氟化物的熔点比氯化物熔点高很多的原因是。
-
6、乙烯和苯能够共同发生的反应类型有( )
①加成反应 ②消去反应 ③聚合反应 ④氧化反应
A、①④ B、②③ C、③④ D、①② -
7、工业上合成乙苯的反应如下。下列说法正确的是( )
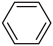 +CH2=CH2
+CH2=CH2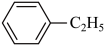 A、该合成反应属于取代反应 B、乙苯分子内的所有C、H原子可能共平面 C、乙苯的一溴代物有5种 D、苯、乙烯和乙苯均可使酸性高锰酸钾溶液褪色
A、该合成反应属于取代反应 B、乙苯分子内的所有C、H原子可能共平面 C、乙苯的一溴代物有5种 D、苯、乙烯和乙苯均可使酸性高锰酸钾溶液褪色 -
8、下列有关烷烃的叙述中,正确的是( )A、在烷烃分子中,可能会有碳碳双键 B、烷烃中除甲烷外,很多都能使紫色KMnO4溶液褪色 C、分子通式为的烃不一定是烷烃 D、烷烃跟卤素单质在光照条件下能发生取代反应
-
9、以下用于研究有机物的方法错误的是( )A、蒸馏法常用于分离提纯液态有机混合物 B、燃烧法是研究确定有机物成分的有效方法之一 C、核磁共振氢谱通常用于分析有机物的相对分子质量 D、对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团
-
10、下列实验有关叙述正确的是( )
 A、用装置①来分离苯和溴苯的混合物 B、用装置②蒸馏工业乙醇可得到无水乙醇 C、重结晶提纯苯甲酸过程中要用到装置③进行分离操作 D、用装置④进行萃取操作,实验者用左手托住分液漏斗活塞,右手抵住玻璃塞,将分液漏斗按图所示双手用力振荡,使液体混合
A、用装置①来分离苯和溴苯的混合物 B、用装置②蒸馏工业乙醇可得到无水乙醇 C、重结晶提纯苯甲酸过程中要用到装置③进行分离操作 D、用装置④进行萃取操作,实验者用左手托住分液漏斗活塞,右手抵住玻璃塞,将分液漏斗按图所示双手用力振荡,使液体混合 -
11、下列说法正确的是( )A、结构示意图:
 B、
B、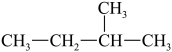 的名称为3-甲基丁烷
C、乙烯和1,3-丁二烯互为同系物
D、
的名称为3-甲基丁烷
C、乙烯和1,3-丁二烯互为同系物
D、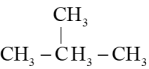 和
和 互为同系物
互为同系物
-
12、下列各组物质不属于同分异构体的是( )A、CH3CH2OH和CH3CHO B、
 和
和 C、
C、 和
和 D、正戊烷与异戊烷
D、正戊烷与异戊烷
-
13、下列物质的类别与所含官能团都正确的是( )A、
 酚类 -OH
B、
酚类 -OH
B、 羧酸 -CHO
C、
羧酸 -CHO
C、 醛类 -CHO
D、CH3-O-CH3醚类
醛类 -CHO
D、CH3-O-CH3醚类 
-
14、向由0.1molCoCl3·6H2O配成的溶液中加入足量AgNO3溶液,产生0.2mol沉淀。配合物CoCl3·6H2O的配位数为6,下列说法错误的是( )A、该配合物的中心离子是 B、该配合物的配体是H2O和 C、每1mol配离子中含有6NA个共价键 D、该配合物中存在的化学键有:共价键、配位键、离子键
-
15、下列各组物质的熔点均与所含化学键能有关的是( )A、CaO与CO2 B、NaCl与HCl C、SiC与Si D、Cl2与I2
-
16、纳米为无定形非晶态,白色粉末,颗粒尺寸小、微孔多、比表面积大、对紫外线反射能力强等特点。下列关于纳米的说法正确的是( )A、对光有各向异性 B、熔点与晶体相同 C、纳米具有自范性 D、可用X−射线衍射实验区分纳米与晶体
-
17、下列关于范德华力与氢键的叙述中正确的是( )A、范德华力比氢键的作用还要弱 B、范德华力与氢键共同决定物质的物理性质 C、范德华力与氢键的强弱都只与相对分子质量有关 D、任何物质中都存在范德华力,而氢键只存在于含有、、的物质中
-
18、下列化合物中,化学键的类型和分子的极性(极性或非极性)皆相同的是( )A、CO2和SO2 B、CH4和H2O C、BF3和NH3 D、HCl和HI
-
19、用VSEPR模型预测下列分子或离子的立体结构,其中不正确的是( )A、NH 为正四面体形 B、CS2为直线形 C、CH2O为V形 D、PCl3为三角锥形
-
20、氨气分子的空间结构是三角锥形,而甲烷分子的空间结构是正四面体形,这是因为( )A、两种分子的中心原子的杂化轨道类型不同,中原子为杂化,而中原子是杂化 B、分子中氮原子形成3个杂化轨道,分子中碳原子形成4个杂化轨道 C、分子中中心原子上有一对未成键
 孤电子对,它对成键电子对的排斥作用较强
D、氨气是四原子化合物,甲烷为五原子化合物
孤电子对,它对成键电子对的排斥作用较强
D、氨气是四原子化合物,甲烷为五原子化合物