相关试卷
-
1、工业上以铬铁矿(主要成分是FeCr2O4 , 含Al、Si的氧化物等杂质)为主要原料制备红矾钠(Na2Cr2O7·2H2O)的工艺流程如图。

注:“焙烧”的目的:①将FeCr2O4转化为Na2CrO4、Fe2O3;
②将Al,Si的氧化物分别转化为NaAlO2和Na2SiO3。
回答下列问题:
(1)、“焙烧”时气体与矿料逆流而行,目的是。(2)、“焙烧”时FeCr2O4发生了氧化还原反应,其氧化剂和还原剂的物质的量之比为。(3)、“中和”步骤产生的滤渣的主要成分为Al(OH)3和(写化学式)。(4)、“酸化”的目的是(用离子方程式表示)。(5)、“蒸发结晶”所需的主要仪器有三角架、酒精灯、玻璃棒、(填仪器名称)。(6)、矿物中相关元素可溶性组分的物质的量浓度的对数值与pH的关系如图:
溶液中微粒浓度c≤1.0×10-5mol/L时可认为已除尽。由图中数据计算Ksp[Fe(OH)3]=;“中和”时调pH的范围为。
-
2、酮基布洛芬(D)是用于治疗各种关节炎、强直性脊柱炎引起的关节肿痛以及痛经、牙痛、术后痛和癌性痛的非处方药,其有多种合成路线,其中一种如图所示。

回答下列问题:
(1)、A的分子式为 , A→B的反应类型为。(2)、C中的官能团名称为。(3)、B→C的反应方程式为。(4)、下列关于D的说法中错误的是。a.可以发生氧化反应,加成反应、取代反应
b.分子中sp3杂化的碳原子只有1个
c.该分子中所有原子可以共平面
d.通过成酯修饰可缓解其酸性较强对胃肠的刺激
(5)、在A的同分异构体中,同时满足下列条件的共有种。①属于芳香族化合物;②苯环上有两个取代基且其中一个是醛基(-CHO)。其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的结构简式为。
-
3、人体血液中存在H2CO3/和/等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值lgx[x表示或]与pH的关系如图所示。下列说法正确的是( )
 A、曲线Ⅰ表示lg与pH的关系 B、a→b的过程中,水的电离程度减小 C、Ka()的数量级为10-7 D、当pH增大时,逐渐减小
A、曲线Ⅰ表示lg与pH的关系 B、a→b的过程中,水的电离程度减小 C、Ka()的数量级为10-7 D、当pH增大时,逐渐减小 -
4、汽车尾气治理可用碳在催化剂的条件下还原NO2:2C(s)+2NO2(g)N2(g)+2CO2(g)。在恒压密闭容器中加入等量的碳和NO2气体,保持温度不变,测得相同时间内NO2的转化率在不同压强下的变化如图所示。下列说法错误的是( )
 A、b、e两点转化率相同,反应速率不同 B、最高点之前,NO2的转化率升高是因为压强增大使平衡正向移动 C、e点CO2的体积分数约为33.3% D、向e点添加体积比为1:2的N2和CO2达新平衡,CO2的体积分数不变
A、b、e两点转化率相同,反应速率不同 B、最高点之前,NO2的转化率升高是因为压强增大使平衡正向移动 C、e点CO2的体积分数约为33.3% D、向e点添加体积比为1:2的N2和CO2达新平衡,CO2的体积分数不变 -
5、己二腈[NC(CH2)4CN]在工业上用量很大,某小组用甲烷燃料电池作为电源电合成己二腈,下列说法错误的是( )
 A、KOH溶液中OH-移向电极a B、电极c的电势高于电极d C、当电路中转移1mole-时,阳极室溶液质量减少8g D、电极d的电极反应为:2CH=CHCN+2H++2e-=NC(CH2)4CN
A、KOH溶液中OH-移向电极a B、电极c的电势高于电极d C、当电路中转移1mole-时,阳极室溶液质量减少8g D、电极d的电极反应为:2CH=CHCN+2H++2e-=NC(CH2)4CN -
6、Mg2Fe是目前储氢密度最高的材料之一,其晶胞结构如图所示,晶胞边长为apm,储氢后H2分子占据晶胞的棱心和体心,化学式为Mg2Fe(H2)x。下列说法正确的是( )
 A、储氢时0<x≤1 B、晶胞中距离Fe最近的Mg有4个 C、H2储满后,H2和H2的最短距离为pm D、Mg填充在Fe形成的八面体空间中
A、储氢时0<x≤1 B、晶胞中距离Fe最近的Mg有4个 C、H2储满后,H2和H2的最短距离为pm D、Mg填充在Fe形成的八面体空间中 -
7、气相硝化法制备硝基烷经的反应机理如下:
①R-HR·+H· ②R"一R'R”·+R'· ③R·+HO-NO→R一NO2+HO·
④R'·+HO-NO2→R'一NO2+HO· ⑤R"·+HO-NO:→R"-NO2+HO·
如丙烷气相硝化可得到4种一硝基取代产物:CH3CH2CH2NO2、CH3CH(NO)CH3、CH3CH2NO2、
CH3NO2。据此推理正丁烷气相硝化可得到一硝基取代产物的种数为( )
A、7种 B、6种 C、5种 D、4种 -
8、由γ-羟基丁酸生成γ-丁内酯的反应:HOCH2CH2CH2COOH
 +H2O。在25℃时,水溶液中γ-羟基丁酸的初始浓度为0.18mol/L,随着反应的进行,测得γ-丁内酯的浓度随时间的变化如下表所示:
+H2O。在25℃时,水溶液中γ-羟基丁酸的初始浓度为0.18mol/L,随着反应的进行,测得γ-丁内酯的浓度随时间的变化如下表所示:t/min
21
50
80
100
120
160
220
∞
c/(mol/L)
0.024
0.050
0.071
0.081
0.090
0.104
0.116
0.132
下列说法错误的是( )
A、γ-丁内酯和丁烯酸(CH2=CHCHCOOH)互为同分异构体 B、及时移出γ-丁内酯,可使γ-羟基丁酸的转化率提高,反应速率加快 C、在50~80min,以γ-丁内酯的浓度变化表示的反应速率为7.00×10-4mol/(L·min) D、在25℃时,该反应的平衡常数K=2.75 -
9、化合物Z是合成药物艾氟康唑的中间体,下列说法错误的是( )
 A、X分子含3种官能团 B、Y分子存在对映异构现象 C、Z可以发生加聚反应 D、Z有4种处于不同化学环境的氢原子
A、X分子含3种官能团 B、Y分子存在对映异构现象 C、Z可以发生加聚反应 D、Z有4种处于不同化学环境的氢原子 -
10、某化合物通过界面埋人可提高太阳能电池的稳定性,其结构如图,X、Y、Z、W、M是原子序数依次增大的前四周期主族元素,X与Z的原子序数之和与W的原子序数相等。下列说法正确的是( )
 A、最高化合价:Z>Y B、第一电离能:Y>X>W C、WY2和WY3的VSEPR模型名称均为平面三角形 D、基态时与M原子最外层电子数相同的同周期元素还有三种
A、最高化合价:Z>Y B、第一电离能:Y>X>W C、WY2和WY3的VSEPR模型名称均为平面三角形 D、基态时与M原子最外层电子数相同的同周期元素还有三种 -
11、在合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前需经铜氨溶液除去CO,其反应为[Cu(NH3)2]++CO+NH3[Cu(NH3)3CO]+ △H<0。下列说法中正确的是( )A、原料气需净化是为了防止催化剂“中毒” B、铜氨溶液吸收CO适宜的条件是高温高压 C、[Cu(NH3)3CO]+中提供孤对电子形成配位键的原子是N和О D、[Cu(NH3)3CO]+中H一N一H的键角小于NH3分子中H一N一H的键角
-
12、下列实验装置能达到实验目的的是( )
 A、用乙醇萃取CCl4中的碘 B、除去甲烷中混有的乙烯 C、制备乙炔 D、验证苯与液溴发生取代反应
A、用乙醇萃取CCl4中的碘 B、除去甲烷中混有的乙烯 C、制备乙炔 D、验证苯与液溴发生取代反应 -
13、三甲基家[(CH3)3Ga]是一种金属有机化合物,广泛用作制备LED等新型半导体光电产品,可通过该反应来制备:GaCl3+(CH3)3Al(CH3)3Ga+AlCl3。下列说法正确的是( )A、14C原子的中子数为6 B、基态31Ga原子的价电子排布式为4s24p1 C、Cl-核外三个能层均充满电子 D、Al核外有13种空间运动状态不同的电子
-
14、哲学思想在自然科学中有许多体现,下列叙述与对应的哲学观点不相符的是( )
选项
叙述
哲学观
A
铁丝与稀硫酸、浓硫酸反应的现象不同
量变到质变
B
沸点:H2O>H2Te>H2Se>H2S
事物性质的变化规律既有普遍性又有特殊性
C
石灰乳中存在沉淀溶解平衡
对立与统一
D
苯硝化时生成硝基苯而甲苯硝化时生成三硝基甲苯
相互影响
A、A B、B C、C D、D -
15、化学用语是化学专业语言,是学习化学的工具。下列有关化学用语的说法错误的是( )A、PCl3的价层电子对互斥模型:
 B、HCl分子中的σ键电子云轮廓图:
B、HCl分子中的σ键电子云轮廓图: C、顺式聚-1,3-丁二烯的结构简式:
C、顺式聚-1,3-丁二烯的结构简式: D、NH3中N的杂化轨道表示式:
D、NH3中N的杂化轨道表示式:
-
16、“宏观辨识与微观探析”是化学学科核心素养之一,下列说法错误的是( )A、稠环芳香经萘(
 )易溶于苯是因为其为极性分子
B、聚乙炔具有导电性的重要原因是其存在共轭大π键体系
C、晶体具有自范性是因为晶体中粒子在微观上呈现有序排列
D、离子液体的熔点较低是因为其含有体积很大的阴、阳离子
)易溶于苯是因为其为极性分子
B、聚乙炔具有导电性的重要原因是其存在共轭大π键体系
C、晶体具有自范性是因为晶体中粒子在微观上呈现有序排列
D、离子液体的熔点较低是因为其含有体积很大的阴、阳离子
-
17、文物承载着中华优秀传统文化的血脉,下列关于湖北省博物馆中收藏的相关文物描述错误的是( )
 A、图甲“云梦睡虎地秦简”主要成分为纤维素 B、图乙“曾侯乙编钟”是一种青铜器,青铜属于合金 C、图丙“元青花四爱图梅瓶”的生产原料为黏土 D、图丁“玉璇玑”是一种玉器,其主要成分为有机高分子材料
A、图甲“云梦睡虎地秦简”主要成分为纤维素 B、图乙“曾侯乙编钟”是一种青铜器,青铜属于合金 C、图丙“元青花四爱图梅瓶”的生产原料为黏土 D、图丁“玉璇玑”是一种玉器,其主要成分为有机高分子材料 -
18、化合物M是一种具有茉莉花香味的无色油状液体,结构简式是
 , 其合成路线如下(部分反应条件未注明):
, 其合成路线如下(部分反应条件未注明): (1)、G中所含官能团的名称为。(2)、B→C反应的试剂及条件为。(3)、有机物C的结构简式为。(4)、E→F反应的化学方程式为 , 反应类型为。(5)、若将A加入少量酸性高锰酸钾溶液中,振荡后可使其褪色,其原因是____(填字母)。A、A属于不饱和烃,可被酸性高锰酸钾溶液氧化 B、苯环受侧链影响,可被酸性高锰酸钾溶液氧化 C、侧链受苯环影响,可被酸性高锰酸钾溶液氧化 D、A催化高锰酸钾在酸性溶液中分解.(6)、在M的同分异构体中,同时满足下列条件的共有种(不考虑立体异构);
(1)、G中所含官能团的名称为。(2)、B→C反应的试剂及条件为。(3)、有机物C的结构简式为。(4)、E→F反应的化学方程式为 , 反应类型为。(5)、若将A加入少量酸性高锰酸钾溶液中,振荡后可使其褪色,其原因是____(填字母)。A、A属于不饱和烃,可被酸性高锰酸钾溶液氧化 B、苯环受侧链影响,可被酸性高锰酸钾溶液氧化 C、侧链受苯环影响,可被酸性高锰酸钾溶液氧化 D、A催化高锰酸钾在酸性溶液中分解.(6)、在M的同分异构体中,同时满足下列条件的共有种(不考虑立体异构);①含有苯环且苯环上只有两个取代基②能与NaHCO3溶液反应放出CO2
其中核磁共振氢谱显示为5组峰,且峰面积之比为3:2:2:2:1的同分异构体的结构简式为(任意写一种)。
-
19、工业上利用废镍催化剂(主要成分为NiO,还含有一定量的ZnO、Fe2O3、SiO2、CaO等)制备一水合氢氧化氧镍(2NiOOH·H2O)的工艺流程如下:

相关金属离子[c0(Mn+)=0.1 mol/L]开始形成氢氧化物沉淀的pH如下(当c(M+)≤10-5mol/L,可以认为Mn+沉淀完全):
金属离子
Ca2+
Zn2+
Ni2+
Fe3+
开始沉淀时的pH
10.6
7.6
7.1
1.5
回答下列问题:
(1)、写出一种能提高“酸浸”速率的措施: , 试剂X用于调节溶液的pH,为使Fe3+沉淀完全,需调控pH的范围是(保留一位小数)。(2)、废渣1的主要成分是 , “ 萃取”操作中用到的玻璃仪器有。(3)、基态Ni原子的价电子排布式为。(4)、“氧化”过程中加入的试剂Y是NaClO,写出加入NaClO反应生成一水合氢氧化氧镍(2NiOOH·H2O)的离子方程式:。(5)、已知工业上也可以用Ni(OH)2作为阳极、NaOH溶液为电解质溶液,通过电解氧化法制备NiOOH,其阳极的电极反应式为。 -
20、氨基乙酸铜被广泛应用于染料、涂料、塑料和电池等领域,其化学式为(H2N-CH2-COO)2Cu,结构如图所示。
 (1)、该结构中C原子的杂化方式为。(2)、原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+表示,与之相反的用-表示,称为电子的自旋磁量子数。对于基态C原子,其价电子自旋磁量子数的代数和为。(3)、氨基乙酸铜可由碳酸铜、氨乙酸、乙二胺等制得,碳酸铜中的空间结构为 , 氨基(-NH2)的电子式为。(4)、C、N、O三种元素最简单氢化物的键角由大到小的顺序为(用分子式表示)。(5)、基态N原子电子占据最高能级的电子云在空间有个伸展方向。(6)、一价铜及其化合物能催化以“Huisgen叠氮化物—环加成反应”为代表的许多反应。如图所示为CuCl结构的一部分,其余结构中各微粒相对位置与该部分类似。以下描述中正确的是____(填字母)。
(1)、该结构中C原子的杂化方式为。(2)、原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+表示,与之相反的用-表示,称为电子的自旋磁量子数。对于基态C原子,其价电子自旋磁量子数的代数和为。(3)、氨基乙酸铜可由碳酸铜、氨乙酸、乙二胺等制得,碳酸铜中的空间结构为 , 氨基(-NH2)的电子式为。(4)、C、N、O三种元素最简单氢化物的键角由大到小的顺序为(用分子式表示)。(5)、基态N原子电子占据最高能级的电子云在空间有个伸展方向。(6)、一价铜及其化合物能催化以“Huisgen叠氮化物—环加成反应”为代表的许多反应。如图所示为CuCl结构的一部分,其余结构中各微粒相对位置与该部分类似。以下描述中正确的是____(填字母)。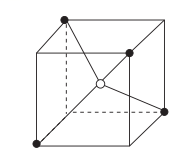 A、上图表示的是CuCl的晶胞 B、若图中正方体的边长为a pm,则CuCl的密度为g/cm3 C、在CuCl晶胞中,Cu+的配位数是4
A、上图表示的是CuCl的晶胞 B、若图中正方体的边长为a pm,则CuCl的密度为g/cm3 C、在CuCl晶胞中,Cu+的配位数是4