相关试卷
-
1、化学反应速率在生产、生活和科学研究中有重要意义。
Ⅰ.构成原电池能增大化学反应速率,甲、乙两个原电池装置如图所示:

回答下列问题:
(1)、若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。①电极X的电极反应式为。
②该电池的正极是(填“镁棒”或“铝棒”),该电极产物W是(填化学式)。
(2)、若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为(填化学式)溶液,电极X为(填字母)
a.Fe电极 b.Mg电极 c.Cu电极 d.Al电极
(3)、Ⅱ.一定温度下,在4 L密闭容器内进行的某一反应(该反应仅涉及两种物质),气体M、气体N的物质的量随时间变化的曲线如图所示。
t2 min时,v(正)(填“>”“<”或“=”)v(逆)。
(4)、若t1=2,则0~2 min内,M的平均反应速率v(M)=。(5)、t3 min时,反应物的转化率为。 -
2、物质的类别和核心元素化合价是研究物质性质的两个重要维度。硫及其部分化合物的“价-类”二维图如图所示,回答下列问题:
 (1)、甲的化学式为;其水溶液在空气中放置容易变浑浊,该反应的化学方程式为。(2)、通入气体乙可使酸性高锰酸钾溶液褪色,说明乙具有性;实验中可用足量的NaOH溶液吸收气体乙,防止污染空气,该反应的离子方程式为。(3)、某同学在用锌与丙的稀溶液反应制H2时,为了加快反应速度,将丙的稀溶液换成浓溶液,该同学的方案(填“合理”或“不合理”),理由是。(4)、丁的钠盐在空气中容易变质,检验其是否变质的方法是。(5)、已知酸性条件下K2Cr2O7能被丁还原为Cr3+ , 24 mL 0.05 mol•L-1 的丁溶液与0.02 mol•L-1的K2Cr2O7溶液恰好反应,则消耗K2Cr2O7溶液的体积为mL。
(1)、甲的化学式为;其水溶液在空气中放置容易变浑浊,该反应的化学方程式为。(2)、通入气体乙可使酸性高锰酸钾溶液褪色,说明乙具有性;实验中可用足量的NaOH溶液吸收气体乙,防止污染空气,该反应的离子方程式为。(3)、某同学在用锌与丙的稀溶液反应制H2时,为了加快反应速度,将丙的稀溶液换成浓溶液,该同学的方案(填“合理”或“不合理”),理由是。(4)、丁的钠盐在空气中容易变质,检验其是否变质的方法是。(5)、已知酸性条件下K2Cr2O7能被丁还原为Cr3+ , 24 mL 0.05 mol•L-1 的丁溶液与0.02 mol•L-1的K2Cr2O7溶液恰好反应,则消耗K2Cr2O7溶液的体积为mL。 -
3、高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
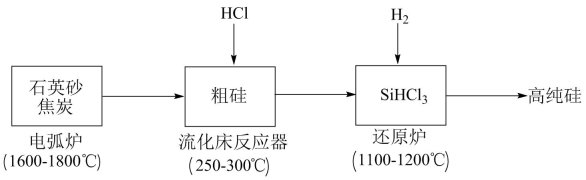 (1)、工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为。当有 1molC参与反应时,该反应转移的电子数是。(2)、有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和。
(1)、工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为。当有 1molC参与反应时,该反应转移的电子数是。(2)、有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和。物质
Si
SiCl4
SiHCl3
SiH2Cl2
SiH3Cl
HCl
SiH4
熔点/℃
1410
-70.4
-126.5
-122
-118
-114.2
-185
沸点/℃
2355
57.6
31.8
8.2
-30.4
-84.9
-111.9
(3)、还原炉中发生的化学反应方程式为:。(4)、上述工艺生产中循环使用的物质除Si、SiHCl3外,还有。(5)、工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为。(6)、若还原炉中有氧气混入,会造成的不良后果有(答一点即可)。 -
4、某小组模拟工业制备NH4SCN,其原理是: , 其中不合理的是( )




A.制备氨气
B.观察氨气流速
C.制备
D.尾气处理
A、A B、B C、C D、D -
5、下列关于硅元素及其化合物的说法正确的是( )A、陶瓷是以黏土和石灰石作为原料,经高温烧结而成的 B、因SiO2能导电,故SiO2可用来生产光导纤维 C、碳化硅可用作耐高温结构材料、耐高温半导体材料 D、瓷坩埚及石英坩埚能与氢氟酸接触,也能对苛性碱和碳酸钠进行熔融操作
-
6、CF1107是一种离子液体,有良好的光学性能,是电子、半导体、显示行业的理想材料。其阴离子(结构如图所示)由X、Y、Z、W、M五种原子序数依次增大的短周期元素构成,其中X、Y、Z、W同周期,Z与M同主族,下列有关说法正确的是( )
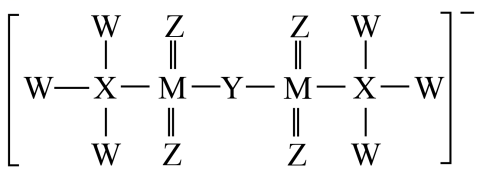 A、最高正价:W>M>Y>X B、简单氢化物稳定性:W>M C、含氧酸的酸性:M>Y>X D、Z与M组成的常见化合物均能使品红溶液褪色
A、最高正价:W>M>Y>X B、简单氢化物稳定性:W>M C、含氧酸的酸性:M>Y>X D、Z与M组成的常见化合物均能使品红溶液褪色 -
7、实验室探究SO2和Fe(NO3)3溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是( )
 A、滴加浓硫酸之前应进行的操作是打开弹簧夹,通入N2一段时间 B、Y中产生的白色沉淀是BaSO4 C、在X装置中浓硫酸体现氧化性和酸性 D、若将Fe(NO3)3换成氨水,Y中能产生白色沉淀
A、滴加浓硫酸之前应进行的操作是打开弹簧夹,通入N2一段时间 B、Y中产生的白色沉淀是BaSO4 C、在X装置中浓硫酸体现氧化性和酸性 D、若将Fe(NO3)3换成氨水,Y中能产生白色沉淀 -
8、硫化氢与甲醇合成甲硫醇(CH3SH)的催化过程如图。下列说法中错误的是( )
 A、过程①、②均需吸收能量 B、总反应可表示为 C、过程④中只形成了O-H键 D、反应前后催化剂的质量和化学性质没有改变
A、过程①、②均需吸收能量 B、总反应可表示为 C、过程④中只形成了O-H键 D、反应前后催化剂的质量和化学性质没有改变 -
9、“纸电池”工作原理如图所示。下列说法错误的是( )
 A、若电解液为食盐水,则该电池中电子从铁电极流出 B、该装置内铁电极发生氧化反应 C、若电解液为稀盐酸,则铜片上有气泡产生 D、若电解液为稀盐酸,电池工作时H+向铁电极定向移动
A、若电解液为食盐水,则该电池中电子从铁电极流出 B、该装置内铁电极发生氧化反应 C、若电解液为稀盐酸,则铜片上有气泡产生 D、若电解液为稀盐酸,电池工作时H+向铁电极定向移动 -
10、U、V、W、Z是原子序数依次增大的四种短周期元素。盐X由U、V、Z三种元素组成,y为元素W的单质,物质a、b、c、d、e、f均为中学常见二元化合物。各物质间能发生如图所示的转化关系(部分反应的产物及反应条件已略),相对分子质量:c比b大16,f比e大16。下列推断错误的是( )
 A、原子半径:Z>W>V B、物质沸点:a<d C、X为正盐或酸式盐 D、最简单氢化物稳定性:W>Z
A、原子半径:Z>W>V B、物质沸点:a<d C、X为正盐或酸式盐 D、最简单氢化物稳定性:W>Z -
11、如图所示为“双色双喷泉”实验装置,图中烧瓶Ⅰ、Ⅱ中分别充满氨气和氯化氢,烧杯内盛装滴有紫色石蕊试液的蒸馏水。下列说法错误的是( )
 A、在实验室中,可用浓氨水和生石灰制备氨气,用浓盐酸和浓硫酸制备氯化氢 B、在实验室中制备干燥的氨气时,可以选用碱石灰作干燥剂 C、实验中同时打开止水夹a、c、d,即可在烧瓶Ⅰ、Ⅱ中分别形成蓝色和红色喷泉 D、喷泉结束后,将烧瓶内溶液混合后转移至蒸发皿中蒸干,可得氯化铵固体
A、在实验室中,可用浓氨水和生石灰制备氨气,用浓盐酸和浓硫酸制备氯化氢 B、在实验室中制备干燥的氨气时,可以选用碱石灰作干燥剂 C、实验中同时打开止水夹a、c、d,即可在烧瓶Ⅰ、Ⅱ中分别形成蓝色和红色喷泉 D、喷泉结束后,将烧瓶内溶液混合后转移至蒸发皿中蒸干,可得氯化铵固体 -
12、工业上制硫酸涉及的三个装置如图,下列有关说法错误的是( )
 A、沸腾炉的进料口a通空气,进料口b加黄铁矿 B、接触室中的反应主要为2SO2 + O22SO3 C、吸收塔中不用水吸收SO3是因为SO3溶于水放出大量的热而形成酸雾,降低吸收效率 D、常温下,铁粒与足量浓硫酸混合会发生化学反应,但最终铁粒仍有剩余
A、沸腾炉的进料口a通空气,进料口b加黄铁矿 B、接触室中的反应主要为2SO2 + O22SO3 C、吸收塔中不用水吸收SO3是因为SO3溶于水放出大量的热而形成酸雾,降低吸收效率 D、常温下,铁粒与足量浓硫酸混合会发生化学反应,但最终铁粒仍有剩余 -
13、在日常的生活和实验中下列调控反应的措施,不能加快反应速率的是( )A、向炉膛内鼓风,用煤粉代替煤块 B、在糕点包装内放置除氧剂 C、在5% H2O2溶液中滴入两滴1 mol•L-1FeCl3溶液 D、CaCO3与稀盐酸反应生成CO2时,适当升高温度
-
14、下列有关硫及其化合物的说法错误的是( )A、浓硫酸用作干燥剂利用了其脱水性 B、常温下,浓硫酸可以用铁制容器盛放 C、硫黄可以用于处理破碎的水银温度计 D、少量的SO2可作为葡萄酒的抗氧化剂
-
15、在一定条件下的密闭容器中,发生可逆反应N2(g)+3H2(g) 2NH3(g)。下列情况下不能说明该反应一定达到化学平衡的是( )A、NH3的质量分数保持不变 B、H2的含量保持不变 C、正反应和逆反应的速率相等 D、N2、H2和NH3的物质的量之比为1:3:2
-
16、《物理小识》中记载:“青矾(主要成分为FeSO4·7H2O)厂气熏人,衣服当之易烂,栽木不茂。”下列叙述错误的是( )A、常温下,FeSO4·7H2O为绿色固体 B、青矾厂气有臭鸡蛋气味 C、青矾厂气中含有硫元素 D、青矾厂气的大量排放会导致形成酸雨
-
17、下列关于能量转换的认识中不正确的是( )A、氢氧燃料电池反应时,化学能转化为电能 B、绿色植物进行光合作用时,太阳能转化为化学能 C、煤燃烧时,化学能主要转化为热能 D、白炽灯工作时,电能全部转化为光能
-
18、农谚:“雷雨发庄稼”、“雨生百谷”主要涉及的元素是( )A、氮 B、磷 C、碳 D、钾
-
19、苯甲酸是一种化工原料,常用作制药和染料的中间体,也用于制取增塑剂和香料等。实验室合成苯甲酸的原理、相关数据、实验步骤及装置图如下:
反应原理



名称
性状
相对分子质量
熔点(℃)
沸点(℃)
密度(g/mL)
溶解度(g)
水
乙醇
甲苯
无色液体易燃易挥发
92
-95
l10.6
0.8669
不溶
互溶
苯甲酸
白色片状或针状晶体
122
122.4
248
1.2659
微溶
易溶
苯甲酸在水中的溶解度:0.34g(25℃);0.85g(50℃);2.2g(75℃)。
根据下列实验步骤,回答相关问题:
(1)、Ⅰ.制备苯甲酸:在如图所示的三颈烧瓶中放入2.7mL.甲苯和100mL水,控制100℃机械搅拌溶液,加热回流。分批加入8.5g高电动搅拌器锰酸钾,继续搅拌4~5h。
三颈烧瓶的最适宜规格为____。 A、100mL B、250mL C、500mL D、1000mL(2)、反应4~5h后﹐静置发现现象时,停止反应。仪器a的作用是。(3)、完成并配平该化学方程式:
A、100mL B、250mL C、500mL D、1000mL(2)、反应4~5h后﹐静置发现现象时,停止反应。仪器a的作用是。(3)、完成并配平该化学方程式: +KMnO4
+KMnO4 +MnO2↓+H2O+(4)、Ⅱ.分离提纯:
+MnO2↓+H2O+(4)、Ⅱ.分离提纯:
向反应后的混合液中加NaHSO3溶液的目的是。
(5)、上述“一系列操作”的顺序是____(用字母表示)。A、重结晶 B、过滤 C、洗涤(6)、Ⅲ.产品纯度测定:称取1.220g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶中,滴加2~3滴酚酞,用KOH标准溶液滴定,消耗KOH溶质的物质的量为2.40×10-3mol。产品中苯甲酸的质量分数为(保留两位有效数字)。若滴定终点俯视读数,所测结果(选填“偏高”、“偏低”、“无影响”)。
-
20、CH4还原CO2是实现“碳达峰”"碳中和”的有效途径之一,相关的主要反应有:
Ⅰ:CH4(g)+CO2(g)2CO(g)+2H2(g) △H1=+247k/mol K1△S1=+200J/(K·mol)
Ⅱ:H2(g)+CO2(g)CO(g)+H2O(g) △H2=+41kJ/mol K2△S2=+42J/(K·mol)。
回答下列问题:
(1)、反应Ⅰ在常温下(填“能”或“不能”)自发进行。(2)、有利于提高CO2平衡转化率的条件是____。A、低温低压 B、低温高压 C、高温低压 D、高温高压(3)、计算反应CH4(g)+3CO2(g)4CO(g)+2H2O(g)的△H=kJ/mol,K=(用含K1、K2的式子表示)。(4)、恒温恒容条件下,向密闭容器中充入一定量CH4和CO2 , 下列条件不能判断反应达到平衡状态的是____。A、n(CH4):n(CO2)=1:2 B、CH4体积分数保持不变 C、混合气体的密度保持不变 D、反应体系的热效应为0(5)、恒温恒容条件下,向密闭容器中加入等物质的量的CH4和CO2 , 发生反应Ⅰ和反应Ⅱ,起始压强为0.2MPa。平衡时总压强为0.3MPa,CO2的转化率为70%。反应Ⅱ的平衡常数Kp=(用分压表示,分压=总压×物质的量分数)。(6)、恒温恒压条件下,CH4和CO2按一定的比例投料,反应经如下流程(主要产物已标出)可实现CO2的高效转化:
过程ⅱ平衡后通入氦气,一段时间后测得CO的物质的量上升。过程ⅲ发生的反应有CaCO3(s)CaO(s)+CO2(g),3Fe(s)+4CO2(g)Fe3O4(s)+4CO(g),结合平衡移动原理,解释CO物质的量上升的原因:。