相关试卷
-
1、过度排放会造成气候、环境问题,在特定催化剂下,和可发生反应生成和 , 热化学方程式如下:
反应I:
反应II:
(1)、已知:写出表示燃烧热的热化学方程式:。
(2)、在一定温度下,将和充入体积为1L的恒容密闭容器中,容器起始压强为p,仅发生反应I,回答下列问题:①反应I在低温下可自发进行的原因是。
②已知平衡常数可用反应体系中的气体分压代替浓度表示,分压=总压×物质的量分数。若该反应平衡后混合气体的压强变为0.75p,则该温度下反应的化学平衡常数Kp为。(用含p的计算式化简后表示)
③一定温度下和的物质的量之比为n:1,相应平衡体系中的物质的量分数为y,请在下图中绘制y随n变化的示意图。
 (3)、有研究表明,5MPa气压下经催化,的含水蒸气量与平衡转化率、甲醇平衡产率的关系如图1、图2所示:
(3)、有研究表明,5MPa气压下经催化,的含水蒸气量与平衡转化率、甲醇平衡产率的关系如图1、图2所示:
①下列说法不正确的是。
A.其他条件不变,增大含水蒸气的量一定可以使反应I的平衡逆移,平衡浓度增大
B.中的水蒸气在高温下可以作为反应的热源,有利于反应I的速率加快
C.图1中450℃下的图像变化说明高温下含水蒸气量增大不利于甲醇生成
D.改用活性更好的催化剂能使图2中各温度下的甲醇产率都增大
②图2中260℃时甲醇产率变化趋势与220、240℃时相反,请从温度与水蒸气含量的角度对此作出合理的解释。
-
2、氮气是一种重要的工业基础原料,可按如下流程进行转化利用。反应Ⅱ的原子利用率100%,硝酸氯可溶于水,Y是硝酸氯的同分异构体,结构中有一个三元环,氮原子的杂化方式为 , 盐A是84消毒液的主要成分,流程图中的水已省略。
 (1)、化合物X的化学式。(2)、写出反应Ⅲ的化学方程式。(3)、下列说法正确的是____。A、薯片的包装袋中、灯泡中、工业制镁的电解槽中都充入氮气做保护气 B、硝酸氯分子中的所有原子可能处于同一平面 C、为了加快反应速率,可以加热反应I D、反应Ⅳ属于氧化还原反应(4)、通常情况下硝酸氯与均为液体,但硝酸氯的沸点明显低于 , 且比更易发生分解,试分析原因。(5)、设计实验验证硝酸氯中的氯元素。
(1)、化合物X的化学式。(2)、写出反应Ⅲ的化学方程式。(3)、下列说法正确的是____。A、薯片的包装袋中、灯泡中、工业制镁的电解槽中都充入氮气做保护气 B、硝酸氯分子中的所有原子可能处于同一平面 C、为了加快反应速率,可以加热反应I D、反应Ⅳ属于氧化还原反应(4)、通常情况下硝酸氯与均为液体,但硝酸氯的沸点明显低于 , 且比更易发生分解,试分析原因。(5)、设计实验验证硝酸氯中的氯元素。 -
3、锗是一种战略性金属,广泛应用于光学及电子工业领域,工业上可由提取 , 并制造晶体,生产一种用于制作太阳能电池的材料。(1)、的价层电子排布式为 , 基态原子有种空间运动状态。(2)、比较与的金属性强弱的实验方法:。(3)、固态时,以环状和链状(SO3)n两种形式存在,下列说法不正确的是____。
 A、单分子中心原子为杂化,空间结构为平面三角形 B、环状(SO3)n中硫原子的杂化轨道类型为 C、单分子和链状(SO3)n均是分子晶体 D、链状(SO3)3中最多可能有6个原子在同一平面上(4)、硫酸可以和硝酸反应生成 , 比较键角 , (填“>”、“<”或“=”),理由是。(5)、的晶胞如图所示。与的最短距离比与的最短距离大,则在晶胞中的位置为(填“A”、“B”或“C”)所处的位置,晶体中一个周围与其距离最近的的个数为。
A、单分子中心原子为杂化,空间结构为平面三角形 B、环状(SO3)n中硫原子的杂化轨道类型为 C、单分子和链状(SO3)n均是分子晶体 D、链状(SO3)3中最多可能有6个原子在同一平面上(4)、硫酸可以和硝酸反应生成 , 比较键角 , (填“>”、“<”或“=”),理由是。(5)、的晶胞如图所示。与的最短距离比与的最短距离大,则在晶胞中的位置为(填“A”、“B”或“C”)所处的位置,晶体中一个周围与其距离最近的的个数为。
-
4、下列方案设计、现象和结论都正确的是( )
选项
目的
方案设计
现象和结论
A
探究和的氧化性强弱
将稀硫酸酸化的加入溶液中
若溶液出现黄色,则说明的氧化性比强
B
比较、结合的能力强弱
分别配得相同的溶液与溶液,稀释10倍后,用计测定溶液
, 说明结合的能力强于
C
探究浓度对平衡的影响
向溶液中加入溶液,溶液呈红色,再三等分于a、b、c三支试管中,向b中加入铁粉、向c中滴加4滴溶液
若b中颜色比a浅,c中颜色比a深,则说明浓度对平衡产生影响
D
探究蔗糖在酸性水溶液中的稳定性
取2mL20%的蔗糖溶液于试管中,加入适量稀后水浴加热5min;再加入适量新制悬浊液并加热
若没有生成砖红色沉淀,则蔗糖在酸性水溶液中稳定
A、A B、B C、C D、D -
5、常温下,往溶液中通入形成饱和溶液X,有微量生成。溶液X中(溶液体积和浓度的变化忽略不计)。已知:电离常数、 , 。下列说法不正确的是( )A、溶液X中, B、反应的 C、溶液X中, D、溶液X中存在
-
6、某电解质溶液中部分微观粒子的结构如图,“---”表示微粒间存在较强静电作用。A、B、C、D、E、F为原子序数依次增大的短周期元素。下列说法不正确的是( )
 A、工业上采用电解的方法冶炼D单质 B、同周期元素中,有一种元素的第一电离能介于B和C之间 C、最简单氢化物的沸点:C>F D、未成对电子数:A>E
A、工业上采用电解的方法冶炼D单质 B、同周期元素中,有一种元素的第一电离能介于B和C之间 C、最简单氢化物的沸点:C>F D、未成对电子数:A>E -
7、叔丁基溴在乙醇中反应的能量变化如图所示。

反应1:
反应2:
下列说法不正确的是( )
A、在乙醇中反应生成时,反应的催化剂是 B、在乙醇中反应生成时,增加催化剂的用量,可以提高转化为的选择性,减少副反应 C、在乙醇中反应生成时,决速步反应活化能为 D、升高温度,与乙醇反应转化率下降,与反应转化率升高 -
8、太阳能驱动和制备的装置如图。下列说法不正确的是( )
 A、阳极区电极反应式为 B、溶液中电流从a极流向b极 C、阳极区中补充可提高制备效率 D、理论上,每生成标况下时,阴极区溶液质量增加22g
A、阳极区电极反应式为 B、溶液中电流从a极流向b极 C、阳极区中补充可提高制备效率 D、理论上,每生成标况下时,阴极区溶液质量增加22g -
9、苯氧乙酸是制备某种香料的中间体,其制备原理如下图所示:

下列说法正确的是( )
A、环氧乙烷只能由乙烯氧化法制得 B、苯氧乙酸含有3种含氧官能团 C、苯氧乙醇的结构简式可能为 D、步骤2可以选用或作为氧化剂
D、步骤2可以选用或作为氧化剂
-
10、下列方程式与所给事实相符的是( )A、将少量通入溶液中: B、银氨溶液中加入足量盐酸产生沉淀: C、利用与制备沉淀: D、加热氯化铜溶液,溶液由绿色变为黄绿色:
-
11、有关有机物检测,下列说法正确的是( )A、酸性高锰酸钾溶液可以用于鉴别苯、己烷与苯乙烯 B、咖啡因的分子结构可以通过X射线衍射技术最终测定 C、质谱仪可用于确定丙醇中有几种化学环境的氢原子 D、光照条件下可以与发生取代反应的烃一定是烷烃
-
12、下列实验装置使用正确的是( )A、装置①可用于硫酸钠的焰色试验
 B、装置②可产生喷泉现象
B、装置②可产生喷泉现象 C、装置③可用于在铁制镀件表面镀铜
C、装置③可用于在铁制镀件表面镀铜 D、装置④可验证氨气能与酸反应
D、装置④可验证氨气能与酸反应
-
13、为阿伏加德罗常数的值,下列说法正确的是( )A、和固体混合物中,阳离子总数大于 B、足量的浓盐酸与反应,转移电子的数目为 C、50g46%的乙醇水溶液中含有的氢原子数为 D、的溶液中离子数为
-
14、实验室制取(一水合碘酸钙)的实验流程如图所示:

已知:常温下微溶于水,难溶于乙醇。下列说法不正确的是( )
A、四氯化碳的作用增大的溶解度,以提高利用率 B、操作1的名称为分液 C、加入后水层中的杂质为 D、操作2可以在冷却后加入乙醇促进产品析出 -
15、常温下,下列各组离子在指定条件下能大量共存的是( )A、溶液中:、、、 B、水溶液中:、、、 C、使紫色石蕊变红的溶液:、、、 D、使酚酞变红的溶液:、、、
-
16、三氟化溴遇水立即发生反应。下列有关该反应的说法正确的是( )A、氧化剂与还原剂的物质的量之比为2∶3 B、反应中每转移生成 C、反应中生成的两种酸都是强酸 D、中心原子价层电子对数为4
-
17、下列表述不正确的是( )A、富勒烯与金刚石互为同素异形体 B、乙炔中碳原子杂化轨道电子云轮廓图:
 C、五氯化磷的电子式中每个原子都满足最外层8电子结构
D、的名称:3-甲基-5-乙基庚烷
C、五氯化磷的电子式中每个原子都满足最外层8电子结构
D、的名称:3-甲基-5-乙基庚烷
-
18、下列关于铁及其化合物的叙述不正确的是( )A、红热的铁与水蒸气反应生成氢氧化铁和氢气 B、在空气里受热,能迅速被氧化成 C、隔绝空气的条件下,向溶液中加入后得到红褐色沉淀 D、溶液可用于有机物中酚羟基的检验
-
19、下列物质属于强电解质的是( )A、氨气 B、硬脂酸钠 C、醋酸 D、石灰水
-
20、苯乙烯是生产塑料与合成橡胶的重要原料。氧化乙苯脱氢的反应为:(1)、已知:

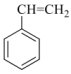
反应I:


反应II:
则。
(2)、下列关于氧化乙苯脱氢反应说法正确的是____(填标号)。A、恒温恒容下,若体系气体的平均相对分子质量不变,则反应达到平衡状态 B、及时分离出水蒸气,有利于提高平衡混合物中苯乙烯含量 C、恒温恒容下,反应达平衡后,再充入少量 , 平衡将向左移动 D、升高温度,正反应速率增大,逆反应速率减小(3)、常压下,乙苯和吸附在催化剂表面的活性中心,并发生反应。控制投料比[(乙苯)]分别为1:1、5:1和10:1,乙苯平衡转化率与反应温度的关系如图所示。
①乙苯平衡转化率相同时,投料比越高,对应的反应温度越(填“高”或“低”)。
②实验发现,相同温度下,当投料比远大于10:1时,乙苯的消耗速率明显下降,可能的原因是(答出一条即可)。
(4)、700K时,向恒容密闭容器中加入过量和一定量乙苯,此时反应I和II不发生。初始容器内压强为(此时未分解),平衡时容器内压强 , 则平衡时苯乙烯的分压为(以含有的代数式表示)。[已知:①为以分压表示的平衡常数,分压=总压物质的量分数。②时,(5)、催化氧化乙苯脱氢制苯乙烯可能存在两种机理:
①机理一可表示为下列两个基元反应(表示催化剂),请补全反应ii:
i:


ii:。
机理二认为乙苯在催化剂表面先发生反应I,再发生反应II。
②用代替乙苯,分别在催化剂A和B表面进行模拟实验,以验证催化剂的作用机理。实验前,两催化剂均吸附有少量;实验中,两催化剂表面依次通过。用质谱仪对气相体系中各物质进行实时检测结果如下表。其中“+”和“-”分别表示检测到和未检测到相应产物。实验检测结果如下表所示。
催化剂种类
A
B
通入的气体
CO检验结果
+(结果a)
−
+(结果c)
+
检验结果
+(结果b)
−
+(结果d)
−
已知:i.Ar不参与反应,且不与催化剂作用;
ii.质谱仪工作时,有少量产生于质谱仪中的分子碎片。
实验中检测到各物质的物质的量:结果结果 , 结果结果 , 结果结果。由此可推测,在催化剂B的作用下,主要存在机理(填“一”或“二”);通入后,气体检测结果进一步佐证了在催化剂B作用下上述机理的存在,同时进一步排除了另一种机理,试加以说明。