相关试卷
-
1、某兴趣小组的同学向一定体积的溶液中逐滴加入稀硫酸,并测得混合溶液的到点能力随时间变化的曲线如图所示。
 (1)、写出溶液与稀硫酸反应的离子方程式。(2)、该小组的同学关于如图的下列说法中,正确的是(填序号)。
(1)、写出溶液与稀硫酸反应的离子方程式。(2)、该小组的同学关于如图的下列说法中,正确的是(填序号)。①AB段溶液的导电能力不断减弱,说明电解质逐渐转变为非电解质
②B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子
③BC段溶液的导电能力不断增大,主要是由于过量的电离出的离子导电
④a时刻溶液与稀硫酸恰好完全中和
-
2、嫦娥五号将月壤等样本成功带回地球,科学家用充满氮气的人造水晶容器进行了保存。深入研究表明月壤富含Fe、He、SiO2、Al2O3、FeO、CaO等物质,下列说法不正确的是A、氮气可保护月壤样品中低化合价的成分 B、CaO属于碱性氧化物 C、通过月壤样品组分推测,该样品中Si元素的含量最高 D、科学家在分析月壤时,对物质进行分类,有利于更深入地研究
-
3、2022年4月16日,神舟十三号载人飞船返回舱成功着陆,中国航天又站在了一个新的起点。火箭和飞船升空所需的巨大能量可由下列化学反应提供:。有关该反应的说法正确的是A、该反应是分解反应 B、反应中碳元素的化合价降低 C、反应中作氧化剂 D、属于烃
-
4、某溶液中大量含有、、、、、、、。将足量固体加入其中后,离子浓度基本不变的一组是(忽略溶液体积变化)A、、 B、、 C、、 D、、
-
5、在无色透明的碱溶液中,能大量共存的离子组A、Fe3+、Na+、、Cl- B、Mg2+、、、Cl- C、Na+、K+、、Cl- D、Cu2+、Na+、、
-
6、分类是学习和研究化学的一种重要思想方法,下列关于物质分类的说法中正确的是A、漂白粉、胆矾都是混合物 B、烧碱、氯化钠都是离子化合物 C、二氧化碳、一氧化碳都是酸性氧化物 D、水、氨水都是弱电解质
-
7、下列离子方程式中正确的是A、氯气与碘化钾溶液反应:Cl2+I-=Cl-+I2 B、氯化铝溶液与氨水反应:Al3++3OH-=Al(OH)3↓ C、碳酸钠溶液与足量稀盐酸反应:+2H+=H2O+CO2↑ D、钠与水反应:Na+2H2O=Na++2OH-+H2↑
-
8、下列各组反应,最终一定能得到白色沉淀的是A、向Na2CO3溶液中加入CaCl2溶液 B、向CuSO4溶液中加入NaOH溶液 C、向FeCl2溶液中加入过量NaOH溶液 D、向Al2O3固体中加入过量NaOH溶液
-
9、下列离子方程式书写正确的是A、石灰乳中通入少量: B、往溶液中通入少量: C、碳酸氢钾溶液中滴少量氢氧化钡溶液: D、向溶液中滴加溶液至中性:
-
10、下列电离方程式书写不正确的是A、HNO3=H++ B、Ba(OH)2=Ba2++OH- C、NH4NO3=+NO D、NaHCO3=Na++
-
11、中华民族有着光辉灿烂的发明史,下列发明创造的主要原理不涉及化学变化的是A、黑火药的使用 B、用铁矿石炼铁 C、打磨磁石制备指南针 D、粮食酿酒
-
12、中国传统文化对人类文明贡献巨大,很早就把化学技术应用到生产生活中。下列与化学有关的说法不正确的是A、《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以烽燧铳极”这是利用了“KNO3 的氧化性” B、《本草经集注》中记载了区分硝石(KNO3) 和朴消(Na2SO4)的方法:“以火烧之, 烟起,乃真硝石也”,二者也可以利用“焰色试验”区分 C、古人很早就掌握了用孔雀石和木炭一起加热进行火法炼铜的工艺,孔雀石的主要成分Cu2(OH)2CO3物质类别属于碱 D、夏天晒盐,冬天捞碱,是古人巧妙运用温度变化和溶解度差异获得资源的方法
-
13、某同学对胶体的有关认识正确的是( )A、氯化钠注射液能产生丁达尔效应,属于胶体 B、通电时溶液中的溶质粒子向两极移动,而胶体分散质粒子向某一极移动 C、Fe(OH)3胶体具有吸附性,可用于净水 D、向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
-
14、过氧乙酸(CH3CO3H)是一种广谱高效消毒剂,不稳定、易分解,高浓度易爆炸。常用于空气、器材的消毒,可由乙酸与H2O2在硫酸催化下反应制得,热化学方程式为:CH3COOH(aq)+H2O2(aq)⇌CH3CO3H(aq)+H2O(l) △H=-13.7KJ/mol
(1)市售过氧乙酸的浓度一般不超过21%,原因是 。
(2)利用上述反应制备760 g CH3CO3H,放出的热量为kJ。
(3)取质量相等的冰醋酸和50% H2O2溶液混合均匀,在一定量硫酸催化下进行如下实验。
实验1:在25 ℃下,测定不同时间所得溶液中过氧乙酸的质量分数。数据如图1所示。
实验2:在不同温度下反应,测定24小时所得溶液中过氧乙酸的质量分数,数据如图2所示。

①实验1中,若反应混合液的总质量为mg,依据图1数据计算,在0—6h间,v(CH3CO3H)= g/h(用含m的代数式表示)。
②综合图1、图2分析,与20 ℃相比,25 ℃时过氧乙酸产率降低的可能原因是。(写出2条)。
(4) SV-1、SV-2是两种常用于实验研究的病毒,粒径分别为40 nm和70 nm。病毒在水中可能会聚集成团簇。不同pH下,病毒团簇粒径及过氧乙酸对两种病毒的相对杀灭速率分别如图3、图4所示。

依据图3、图4分析,过氧乙酸对SV-1的杀灭速率随pH增大而增大的原因可能是
-
15、表示阿伏加德罗常数的值。下列说法正确的是A、溶液中含有的数目小于(忽略水的电离) B、标准状况下,与充分反应,生成的分子数目为 C、标准状况下,22.4L HF中含有氟原子的数目为 D、完全分解,得到的分子数目为
-
16、在一定温度下,某反应达到了化学平衡,其反应过程对应的能量变化如图。下列说法正确的是
 A、Ea为逆反应活化能,E
A、Ea为逆反应活化能,E 为正反应活化能
B、该反应为放热反应,ΔH=Ea’-Ea
C、所有活化分子的平均能量高于或等于所有分子的平均能量
D、温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
为正反应活化能
B、该反应为放热反应,ΔH=Ea’-Ea
C、所有活化分子的平均能量高于或等于所有分子的平均能量
D、温度升高,逆反应速率加快幅度大于正反应加快幅度,使平衡逆移
-
17、某研究小组探究Fe3+盐溶液与Cu的反应,进行了如下实验。
实验装置
序号
试剂a
实验现象

I
0.25 mol·L-1Fe2(SO4)3溶液
溶液逐渐变为蓝色。2天后,Cu片有较大量剩余,溶液仍为蓝色
Ⅱ
0.5 mol·L-1FeCl3溶液
溶液逐渐变为蓝绿色,铜片表面覆盖有白色固体(经检验为CuCl)。2天后,白色固体消失,Cu片无剩余,溶液中产生大量红褐色沉淀
Ⅲ
0.5 mol·L-1 Fe(NO3)3溶液
溶液逐渐变为绿色,实验过程中未见气泡产生。 2天后,Cu片少量剩余,溶液中产生大量红褐色沉淀
资料:i.CuCl、CuSCN是难溶于水的白色固体;
ii.Fe2+ + NO⇌[Fe(NO)]2+ (棕色)。
(1)、用化学用语解释Fe3+盐溶液显酸性的原因。(2)、实验I中发生反应的离子方程式为。(3)、小组同学取2 mL实验I中反应2天后的溶液于试管中,加入2滴1 mol·L-1 KSCN溶液,观察到溶液迅速变红,产生大量白色沉淀。甲同学猜想Fe2+可能在该条件下被Cu2+氧化了。
①用离子方程式表示甲同学的猜想。
②甲同学通过实验证实了其猜想,实验方案是。
(4)、对比实验I和实验Ⅱ,小组同学推测Cl-可以催化Fe3+与Cu反应。其理由是。(5)、实验Ⅱ中产生大量红褐色沉淀的原因是。(6)、实验Ⅲ所得溶液的颜色不是蓝色,小组同学猜测反应中生成了[Fe(NO)]2+ , 设计并实施了以下实验,验证了其猜想。步骤
实验操作
实验现象
①
向盛有2 g金属Cu片的烧杯中加入试剂X
2天后溶液颜色无明显变化,铜片表面有细小气泡附着
②
继续加入少量FeSO4固体
溶液迅速变为浅棕色
试剂X是。
综合以上实验,Fe3+盐溶液与Cu反应的多样性与阴离子种类、生成物存在形式等有关。
-
18、有关Na2O2性质实验如下:
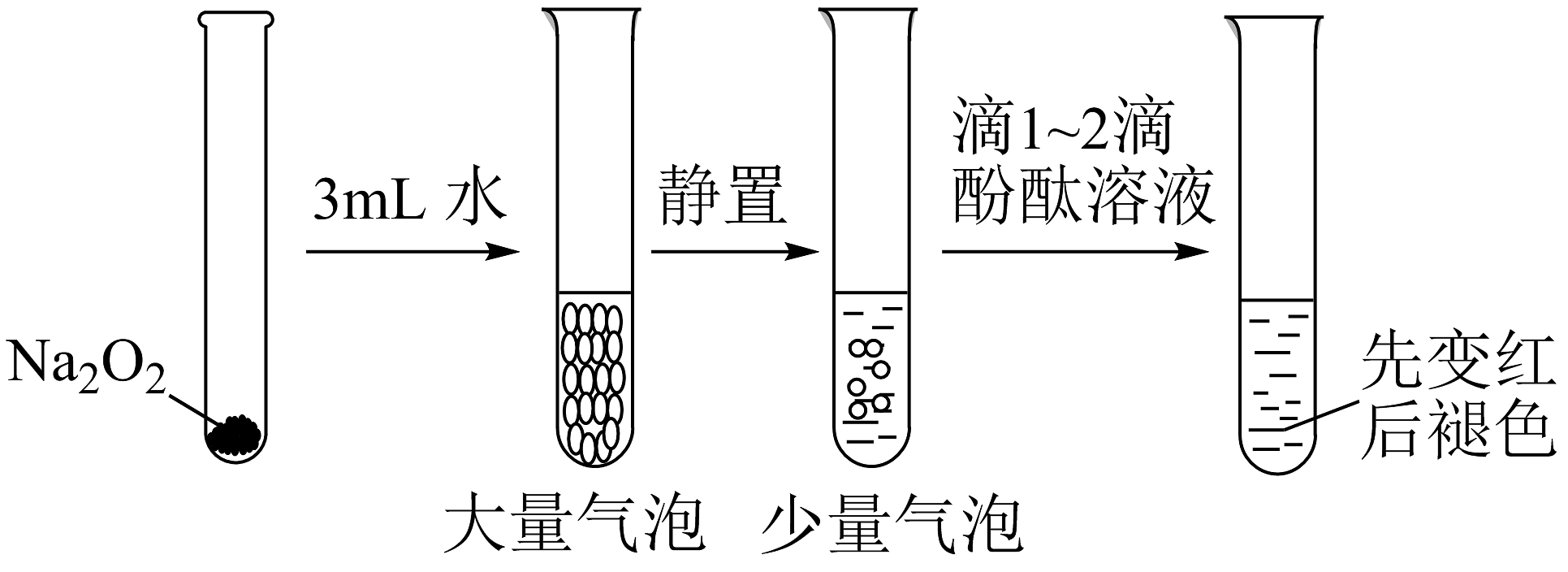
已知:①Na2O2与水反应经历了Na2O2+2H2O =2NaOH+H2O2;
②酚酞褪色原因与溶液的强碱性或强氧化性有关。
根据上述实验可以得出的结论是
A、双氧水能使酚酞褪色 B、浓氢氧化钠能使酚酞褪色 C、双氧水和浓氢氧化钠都能使酚酞褪色 D、可利用二氧化锰和水来完善实验方案 -
19、化学小组研究金属的电化学腐蚀,实验如下:
序号
实验Ⅰ
实验Ⅱ
实验


现象
铁钉周边出现_________色
锌片周边未见明显变化
铁钉周边出现蓝色
铜片周边略显红色
下列说法不正确的是
A、实验Ⅰ中铁钉周边出现红色 B、实验I中负极的电极反应式: C、实验Ⅱ中正极的电极反应式: D、对比实验I、Ⅱ可知,生活中镀锌铁板比镀铜铁板在镀层破损后更耐腐蚀 -
20、利用超分子可分离和 , 将、混合物加入一种空腔大小适配的“杯酚”中进行分离的流程如图。下列说法正确的是
 A、一个分子中含有90个键 B、“杯酚”与形成氢键 C、一个晶胞中含有8个分子 D、该分离过程利用的是超分子的自组装特征
A、一个分子中含有90个键 B、“杯酚”与形成氢键 C、一个晶胞中含有8个分子 D、该分离过程利用的是超分子的自组装特征