相关试卷
-
1、某学者绘制了一种八角星元素周期表,每个八角星代表一个周期(第1周期除外),每个“●”代表一种元素,“------”相连代表同族元素。X、Y、Z、R、M为原子半径依次减小的五种短周期主族元素,Y的最外层电子数比最内层电子数多1.下列说法错误的是
 A、简单氢化物稳定性:Z >R B、离子半径:Z >R>X C、X、Y、Z的最高价氧化物对应的水化物之间均能两两反应 D、X、R形成的化合物中一定含有离子键,可能含有共价键
A、简单氢化物稳定性:Z >R B、离子半径:Z >R>X C、X、Y、Z的最高价氧化物对应的水化物之间均能两两反应 D、X、R形成的化合物中一定含有离子键,可能含有共价键 -
2、化学与化工生产密切相关。下列工业生产中的反应式错误的是
选项
工业生产
反应式
A
氯碱工业
2Cl-+2H2OCl2↑+H2↑+2OH-
B
制备粗硅
2CO+SiO2Si+2CO2
C
侯氏制碱
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
D
合成导电高分子材料
 A、A B、B C、C D、D
A、A B、B C、C D、D -
3、实验操作是进行科学实验的基础。如图实验操作科学合理的是
 A、装置①:滴定终点前蒸馏水冲洗锥形瓶内壁 B、装置②:实验室制备乙炔气体 C、装置③:验证 水溶液的酸性和漂白性 D、装置④:制备氨水
A、装置①:滴定终点前蒸馏水冲洗锥形瓶内壁 B、装置②:实验室制备乙炔气体 C、装置③:验证 水溶液的酸性和漂白性 D、装置④:制备氨水 -
4、蒙顶山茶是中国历史名茶,自古便有“扬子江中水,蒙顶山上茶”。茶多酚是茶叶的活性成分,具有抗菌、抗炎和抗癌功效,其结构如图所示。下列关于茶多酚的叙述正确的是
 A、能与Na2CO3溶液反应产生CO2 B、1个分子中含1个手性碳原子 C、具较好水溶性的主要原因是能与水形成分子间氢键 D、在空气中能稳定存在
A、能与Na2CO3溶液反应产生CO2 B、1个分子中含1个手性碳原子 C、具较好水溶性的主要原因是能与水形成分子间氢键 D、在空气中能稳定存在 -
5、可利用反应 NaCN+2NaOH+Cl2=NaCNO+2NaCl+H2O处理含剧毒物质氰化钠的废水。设阿伏加德罗常数的值为NA , 下列说法错误是A、NaCN中σ键和π键个数比为1:2 B、25℃和101 kPa,22.4 L Cl2所含分子个数大于NA C、NaOH的电子式为
 D、CNO-的空间结构为直线形
D、CNO-的空间结构为直线形
-
6、在日常生活中,我们会接触到各种各样的“剂”,它们有着不同的成分和用途。下列关于常见“剂”的主要成分、功能的说法正确的是
选项
常见“剂”
主要成分
主要功能
A
汽车“防冻液”
乙二醇
降低水的凝固点
B
厨房“洗洁精”
含NaOH的表面活性剂
乳化溶解油脂等物质
C
医用“酒精消毒剂”
95%的乙醇
使病毒细菌的蛋白质变性
D
面团“膨松剂”
碳酸钠
产生CO2使面团蓬松
A、A B、B C、C D、D -
7、2025年2月12日,中国载人月球探测任务登月服被命名为“望宇”,载人月球车被命名为“探索”。下列叙述错误的是A、“望宇”采用的聚酯纤维,属于人工合成高分子材料 B、“望宇”保温层使用的气凝胶,具有极低导热性和优异轻质特性 C、“探索”车轮可以采用天然橡胶,其主要成分为聚1,3-丁二烯 D、“探索”车身采用碳纤维复合材料,具有高强度、轻质和耐腐蚀等性质
-
8、酸性溶液主要组成为与(与会络合为),其具有溶铜速率快、稳定、易控制及易再生等优点,常应用于印刷线路板(PCB)的刻蚀。刻蚀原理为 ,(1)、CuCl中基态亚铜离子的价层电子轨道表示式为。(2)、溶液中存在平衡: , 下列说法不正确的是_______(填序号)。A、加入几滴溶液,平衡逆向移动 B、加热溶液,溶液由蓝绿色变为黄绿色,平衡常数增大 C、加水稀释,的比值会减小 D、加入少量固体,平衡正向移动,转化率增大(3)、盐酸的浓度会影响刻蚀速率,浓度相同,盐酸浓度分别为、、时,随时间的变化曲线如图所示,中间速率变缓慢的可能原因是。
时,在内,的平均生成速率为。
 (4)、能形成多种配合物。铜氨溶液具有显著的抗菌作用。往溶液中通入氨气,测得和铜氨各级配合物的物质的量分数与平衡体系的浓度的负对数)的关系如图所示。
(4)、能形成多种配合物。铜氨溶液具有显著的抗菌作用。往溶液中通入氨气,测得和铜氨各级配合物的物质的量分数与平衡体系的浓度的负对数)的关系如图所示。
①曲线5代表的含铜微粒为。
②b点的纵坐标为。
③结合图像信息,计算反应的平衡常数。(已知的 , 写出计算过程)
-
9、锗单质在光纤通信、国防科技、航空航天技术和半导体材料等领域的应用日趋广泛。工业上一种以冶锌废渣(主要为Zn、Fe、Ge等的氧化物)为原料制备锗的流程如图所示。

已知:①25℃时, , ;
②当离子浓度小于等于时认为该离子已沉淀完全。
③溶浸中元素形式存在回答下列问题:
(1)、“溶浸”时要先把废渣粉碎过筛,目的是;加入的作用是。(2)、在实验室进行“沉锗”后分离得到操作所需的玻璃仪器有。(3)、“氧化”时反应(氧化产物标准状况下为气态)的氧化剂和还原剂的物质的量之比为。(4)、选择氢气还原氧化锗,而不是焦炭,原因可能是(答出一条即可);写出该步骤反应的化学方程式:。(5)、若采用加入氨水沉淀法获得 , 当溶液中恰好完全沉淀时,此时沉淀后溶液中(填“>”“<”或“=”)。(6)、通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,某种硅锗合金的立方晶胞结构如图所示。图中①指示的锗原子的分数坐标为;若该合金的密度为 , 则阿伏加德罗常数(用含、的代数式表示)。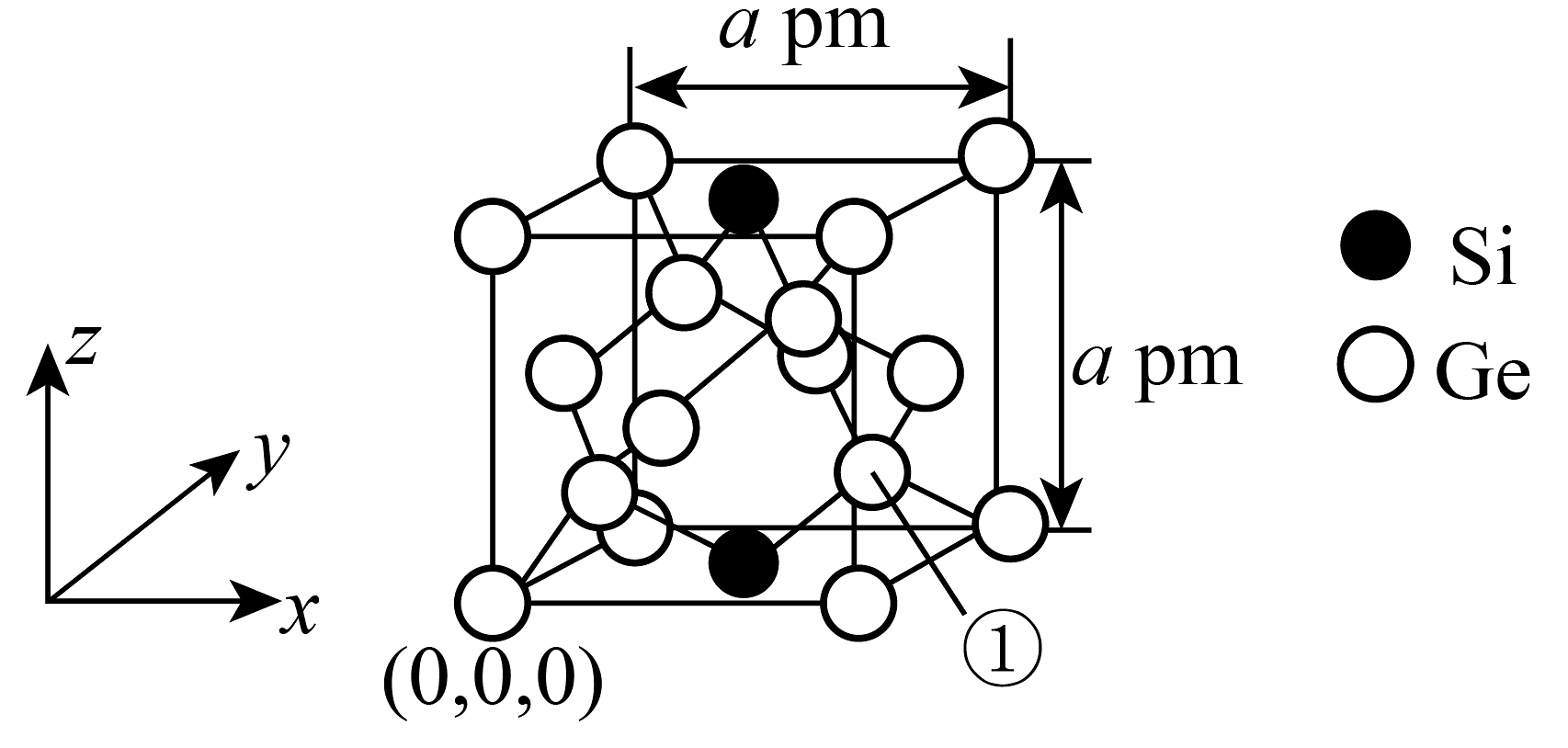
-
10、
I.关于氨的研究学习
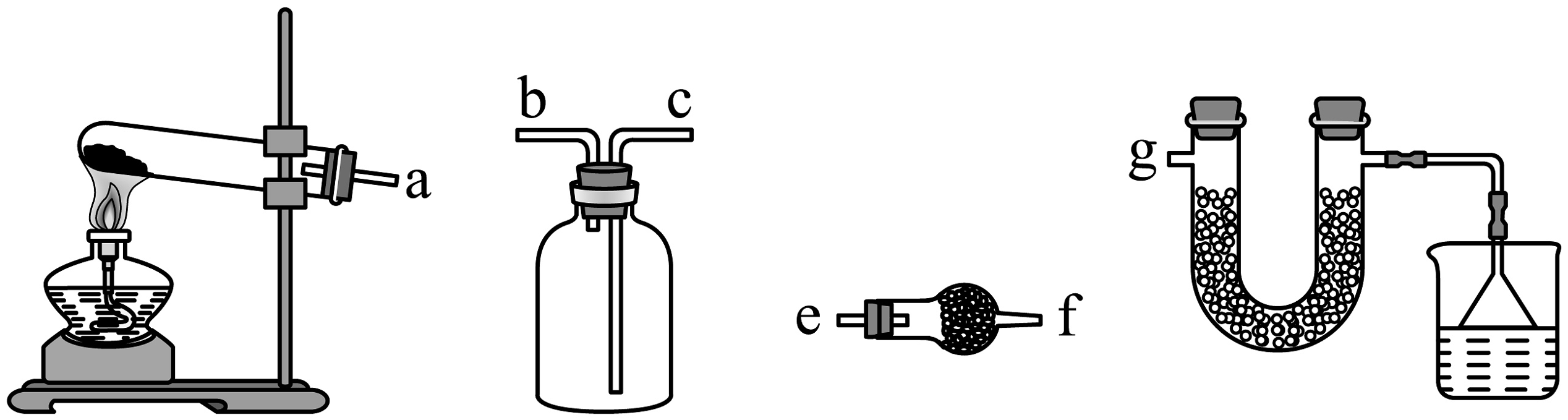
(1)氨气制备装置如下图
①利用上图装置进行实验室制备NH3 , 反应的化学方程式为。
②制取并收集纯净干燥NH3 , 连接装置:ag(填接口字母)。
③球形干燥管和U形管中装干燥剂,下列干燥剂可以选择的是。
A.P2O5 B.碱石灰 C.无水CaCl2
(2)检验某盐溶液中是否含有 , 实验操作和现象:取少量该溶液于试管中,(完成该实验操作、现象和结论)。
(3)用氨水洗涤离心试管中残留的AgCl固体,离子方程式:。
Ⅱ.探究银氨溶液与醛基的反应
实验1:往20mL0.1mol/LAgNO3溶液中滴加3滴乙醛,水浴加热。无明显现象。
实验2:往20mL0.1mol/L银氨溶液中滴加3滴乙醛,水浴加热。出现光亮的银镜。
针对上述实验甲同学基于氧化还原的知识提出以下假设:
假设1:乙醛在碱性条件下还原性增强。假设2:……
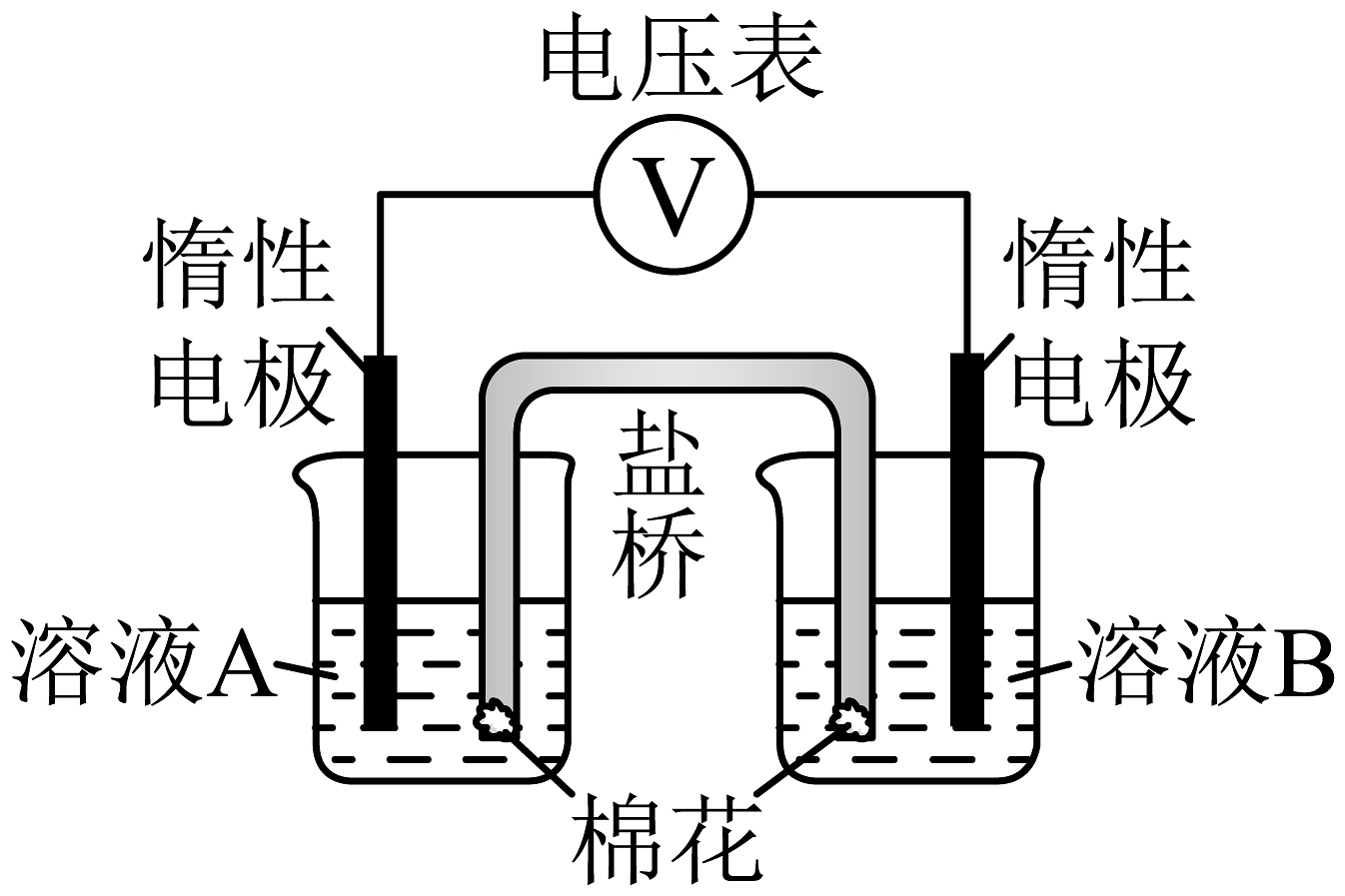
为验证以上假设,甲同学设计了如图所示的电化学装置,并进行了以下四组实验。每组实验中,溶液A和溶液B体积均为20mL,浓度均为0.1mol/L,向溶液B中滴加3滴乙醛后,测得电压表读数如表所示。
已知:参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,检测到的电压越大。
编号
溶液A
溶液B
电压表读数
ⅰ
AgNO3溶液
NaCl溶液
U1
ⅱ
AgNO3溶液
NaOH溶液
U2
ⅲ
银氨溶液
NaCl溶液
U3
ⅳ
银氨溶液
溶液
U4
(4)实验ⅰ和实验ⅲ中,溶液B选用NaCl溶液,而不使用蒸馏水的原因是。
(5)①由实验数据可知假设1成立。假设1成立的判断依据是:。
②碱性条件下,乙醛发生氧化反应的电极方程式为:。
(6)甲同学分别对比了实验ⅰ和实验ⅲ、实验ⅱ和实验ⅳ数据,你认为甲同学想研究的问题是:
(7)乙同学使用pH计测得0.1mol/LAgNO3溶液的pH=6,并指出:在酸性环境,也可能氧化乙醛;这会影响数据的测定和实验结果的判断。
针对该质疑,甲同学在实验ⅰ的基础上进行改进和优化,增设了一组实验v,测得电压表读数远小于U1,因此实验中的影响可忽略。请你简述该改进和优化的方案:。
-
11、某实验小组尝试设计如下装置,利用光伏发电,以甲苯为原料通过间接氧化法制取苯甲酸并实现储能,反应原理如下图所示。下列有关说法错误的是
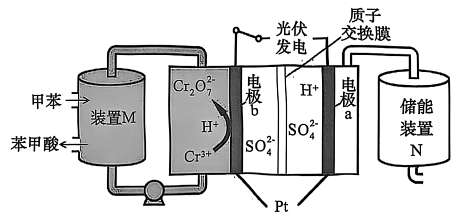 A、电极a为阴极,通过质子交换膜移向a极 B、装置中发生反应:
A、电极a为阴极,通过质子交换膜移向a极 B、装置中发生反应: C、每生成 , 理论上装置中可获得苯甲酸
D、电极发生电极反应为
C、每生成 , 理论上装置中可获得苯甲酸
D、电极发生电极反应为
-
12、部分含硫元素或氮元素物质的类别与相应化合价关系如图所示。

下列描述不合理的是
A、在自然界中存在c,说明该元素非金属性较弱 B、一定条件下,b与e可发生反应转化为c C、f、g为常见的强酸,常温下其浓溶液可用铁制容器储运 D、a、b分子中中心原子的VSEPR模型相同 -
13、已知:甲酸可以分解制取;某学习小组设计实验制取并验证其性质的装置如图所示(部分夹持装置略),下列说法不正确的是
 A、浓硫酸的作用为催化剂、脱水剂 B、碱石灰可吸收水蒸气和甲酸蒸气以及可能产生的和 C、该装置可验证具有还原性 D、可用NaOH溶液吸收尾气,防止污染空气
A、浓硫酸的作用为催化剂、脱水剂 B、碱石灰可吸收水蒸气和甲酸蒸气以及可能产生的和 C、该装置可验证具有还原性 D、可用NaOH溶液吸收尾气,防止污染空气 -
14、酸性锌锰干电池的构造示意图如下。关于该电池及其工作原理,下列说法错误的是
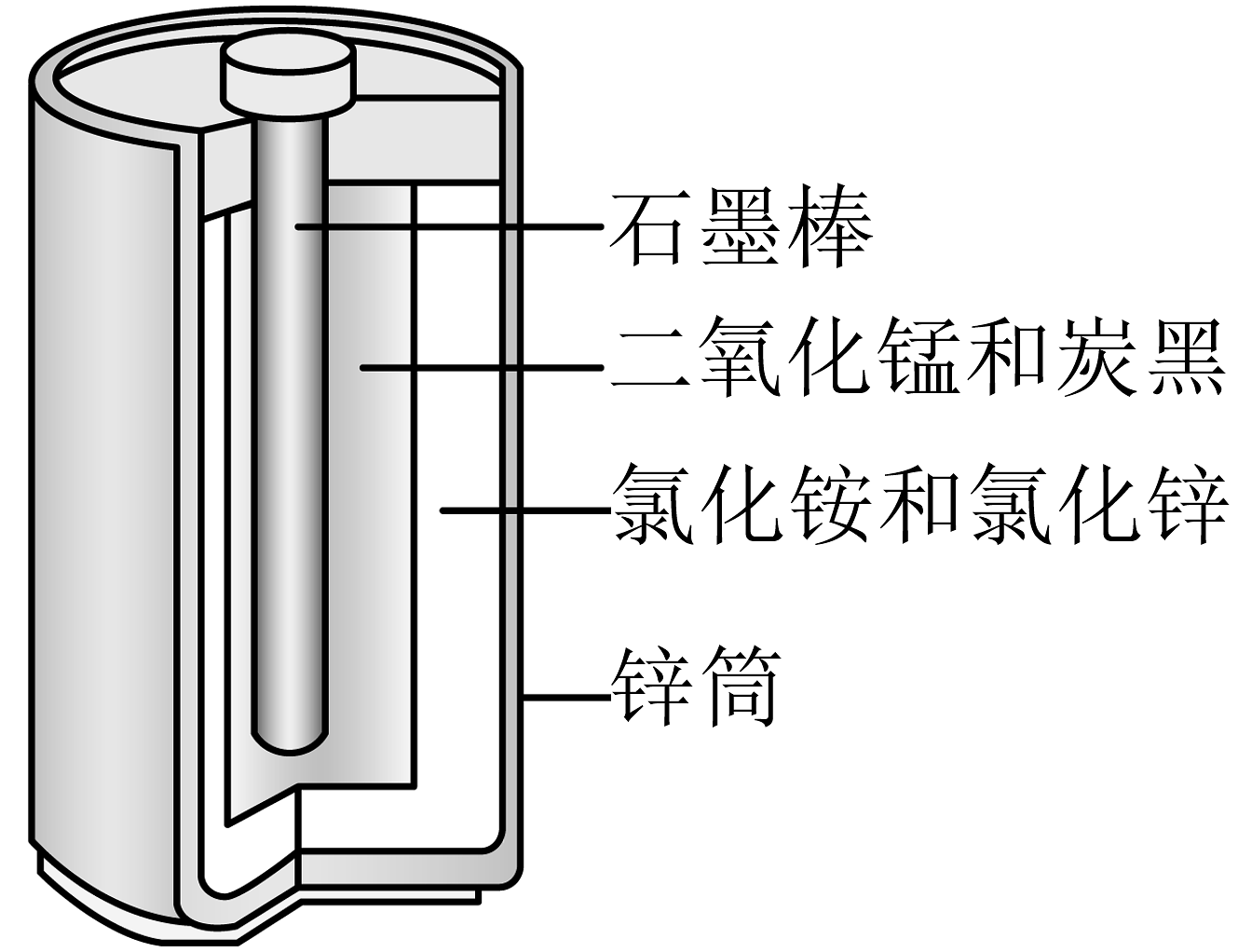 A、石墨作电池的正极材料 B、电池工作时,向正极方向移动 C、发生氧化反应 D、锌筒发生的电极反应为
A、石墨作电池的正极材料 B、电池工作时,向正极方向移动 C、发生氧化反应 D、锌筒发生的电极反应为 -
15、提纯混有少量苯甲酸的苯甲醇(常温为液态,微溶于水)过程如图所示,其中操作为
 A、冷却结晶 B、蒸发结晶 C、蒸馏 D、萃取分液
A、冷却结晶 B、蒸发结晶 C、蒸馏 D、萃取分液 -
16、劳动开创未来,下列劳动项目与所述的化学知识有关联的是
选项
劳动项目
化学知识
A
做水果罐头时加入维生素C
维生素C受热易分解
B
用固体疏通剂处理管道堵塞
C
用除去废水中的
具有很强的还原性
D
用氢氟酸雕刻玻璃花纹
氢氟酸具有弱酸性
A、A B、B C、C D、D -
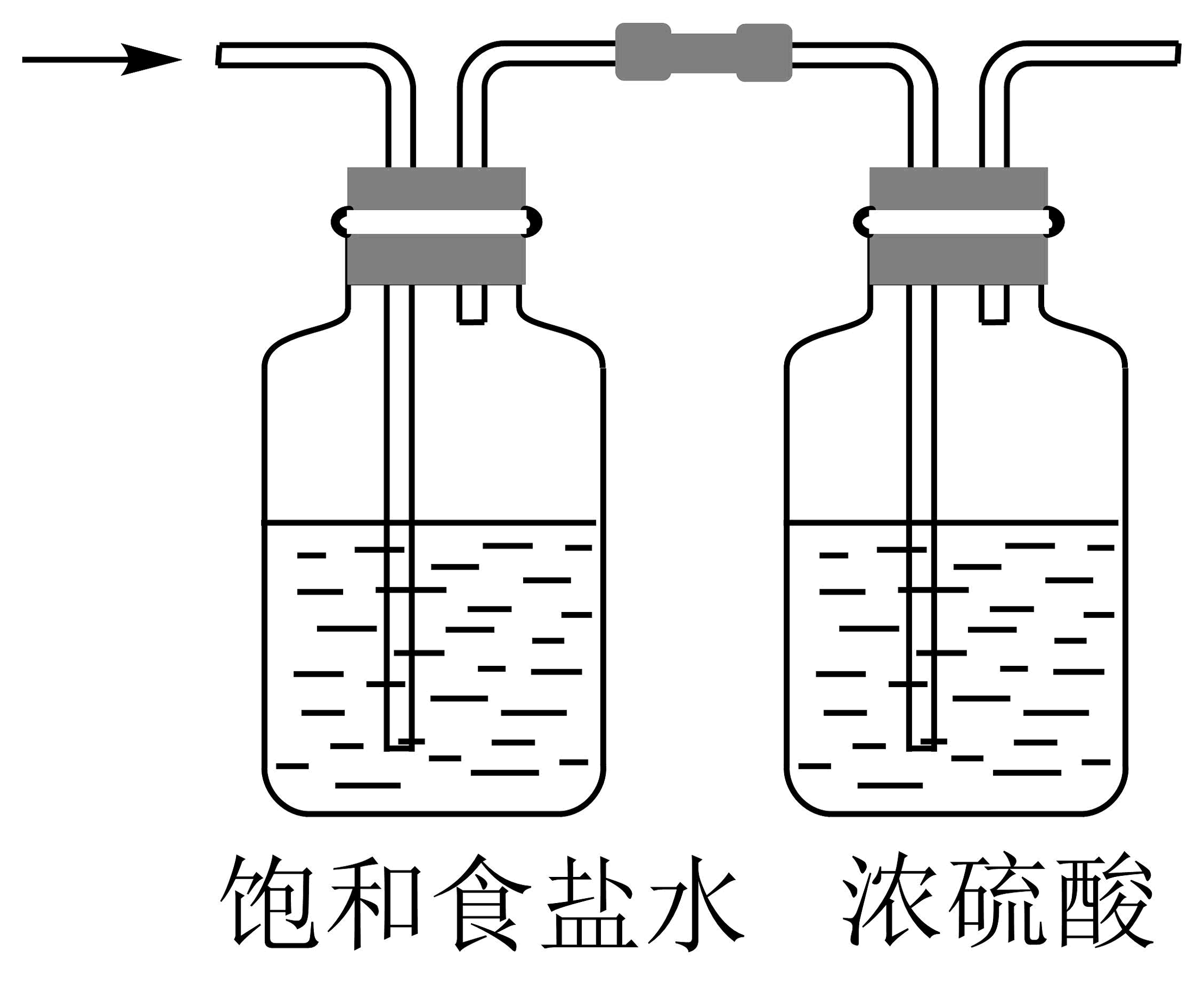
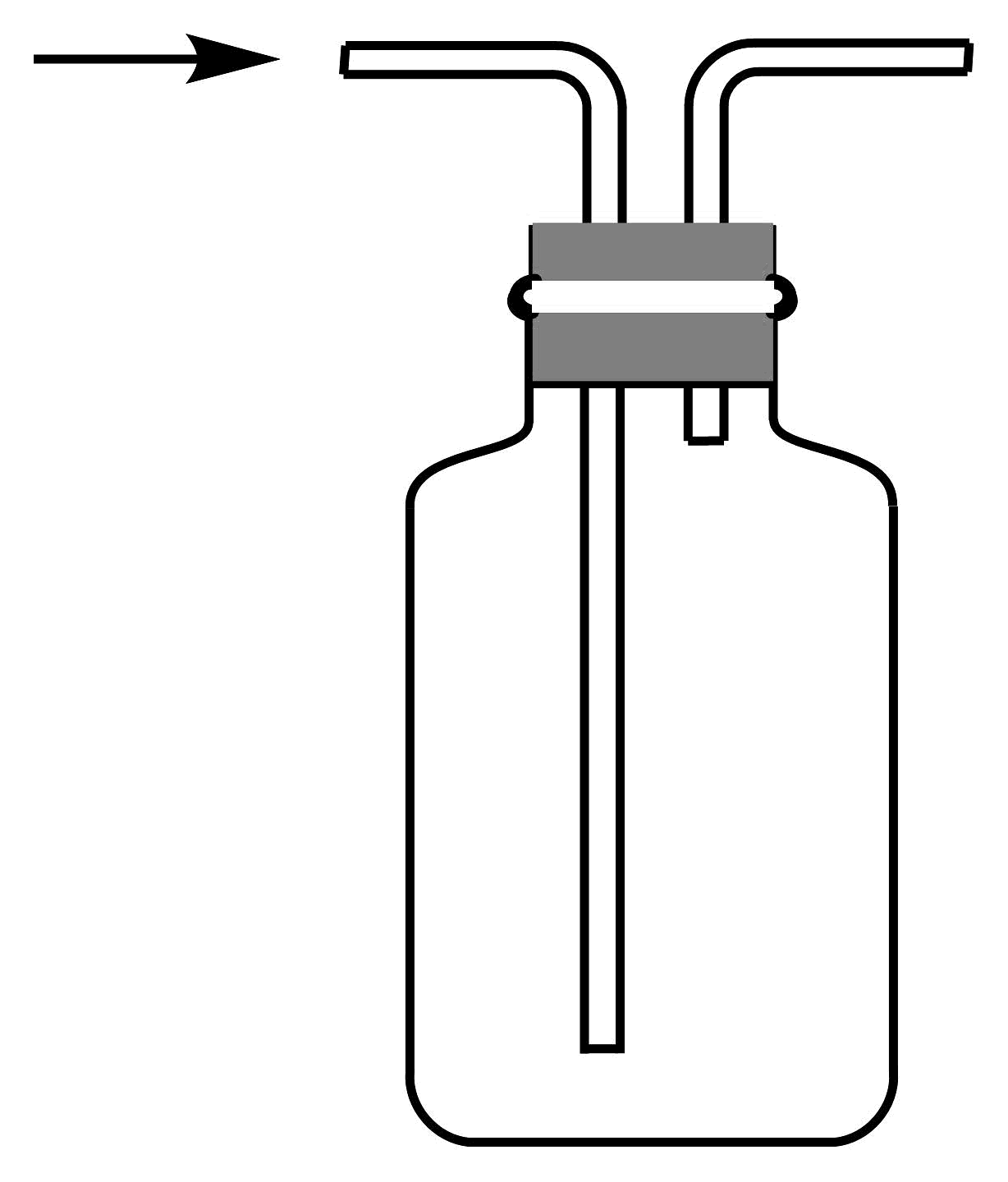
17、1774年舍勒发现了氯气。下列有关氯气制备的实验装置不正确的是


A.制备氯气
B.净化氯气
C.收集氯气
D.尾气处理
A、A B、B C、C D、D -
18、化学助力于人类创造美好生活,下列说法正确的是A、节日里燃放五颜六色的烟花,电子从基态跃迁到激发态以光的形式释放能量 B、传感器测土壤酸碱性,用改善酸性土壤 C、乘氢能源电池公交车出行,沸点低、极易液化 D、锂电池无人机助力现代农业,锂电池放电时化学能转化为电能
-
19、最近,我国在战斗机技术和预警机技术上实现重大跨越,第六代战机歼36试飞成功以及空警3000预警机首次亮相,标志着中国军事力量的全面提升。下列说法正确的是A、钛合金是一种高强度、耐腐蚀的复合材料,钛元素在元素周期表中位于第ⅡB族 B、碳化硅(SiC)是一种耐高温陶瓷材料,属于分子晶体 C、发动机用到的超高温合金含有铌、铁、镍等元素,的中子数为30 D、氢气是战斗机的主要燃料之一,H和D互为同素异形体
-
20、岭南文化源远流长,对社会的发展起着积极的推动作用。下列地方文化涉及的材料不属于有机高分子化合物的是
选项
A
B
C
D
地方文化

顺德木制龙舟

石湾陶塑

广东剪纸

粤剧现代戏服
A、A B、B C、C D、D