-
1、下列有机物命名正确的是A、3,3-二甲基-2-乙基戊烷 B、3,3-二甲基戊烷 C、2-甲基-3-丁烯 D、1,5-二甲苯
-
2、吸湿性强,常被用作气体和液体的干燥剂,它甚至可以使硝酸脱水:。下列说法正确的是A、第一电离能:N<P B、电负性:N<P C、离子半径: D、沸点:
-
3、我国力争2030年前实现碳达峰,2060年前实现碳中和,这体现了中国对解决气候问题的大国担当。在实际生产中,可利用反应来捕捉废气中的 , 下列有关化学用语表示正确的是A、的分子结构模型:
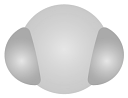 B、键电子云轮廓图
B、键电子云轮廓图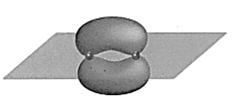 C、的电子式:
C、的电子式: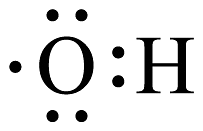 D、的电子排布式:
D、的电子排布式:
-
4、文物凝结了人类智慧的结晶,是历史进步的标志。下列文物所用主要材料属于有机物的是A、
 黄金面具
B、
黄金面具
B、 战国初期竹木简牍
C、
战国初期竹木简牍
C、 曲阳石雕
D、
曲阳石雕
D、 葫芦纹彩陶壶
葫芦纹彩陶壶
-
5、浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验装置。据此回答下列问题:

已知:。
(1)、A中观察到的现象是无水硫酸铜变(填“红色”或“蓝色”)。(2)、B中观察到品红溶液红色褪去,可以证明产物中含有(填“SO2”或“CO2”)。(3)、C中酸性KMnO4的作用是。(4)、D中澄清石灰水变浑浊,发生反应的离子方程式为。(5)、若反应消耗了2mol H2SO4 , 产生气体的体积为(标准状况下)。 -
6、金属镁及其合金在生产生活中应用非常广泛。大量的镁是从海水中提取的,其中的主要步骤如下:
 (1)、提取镁的工厂一般都修建在海边。试剂①适宜选取[填“NaOH”或“Ca(OH)2”]。(2)、试剂②用于溶解Mg(OH)2沉淀,应该选择(填“盐酸”或“硫酸”)。(3)、无水MgCl2在熔融状态下通电后会产生Mg和Cl2 , 写出反应的化学方程式:。(4)、一定温度下,向2L恒容密闭容器中充入4mol M发生反应,其物质的量随着时间的变化关系如图所示,据此回答:
(1)、提取镁的工厂一般都修建在海边。试剂①适宜选取[填“NaOH”或“Ca(OH)2”]。(2)、试剂②用于溶解Mg(OH)2沉淀,应该选择(填“盐酸”或“硫酸”)。(3)、无水MgCl2在熔融状态下通电后会产生Mg和Cl2 , 写出反应的化学方程式:。(4)、一定温度下,向2L恒容密闭容器中充入4mol M发生反应,其物质的量随着时间的变化关系如图所示,据此回答:
①该反应的化学方程式为[填“”或“”]。
②0~3min,用M表示的化学反应速率为(填“0.5”或“1.0”)mol·L-1·min-1。
-
7、如图为元素周期表的一部分,据此回答:
 (1)、元素③的名称是。(2)、①和②形成的常见化合物是(填“CO2”或“NO”)。(3)、元素④的原子,电子式可以表示为。(4)、元素⑤和Na元素形成的化合物中,存在的化学键类型是(填“共价键”或“离子键”)。
(1)、元素③的名称是。(2)、①和②形成的常见化合物是(填“CO2”或“NO”)。(3)、元素④的原子,电子式可以表示为。(4)、元素⑤和Na元素形成的化合物中,存在的化学键类型是(填“共价键”或“离子键”)。 -
8、乙烯的年产量可以衡量一个国家石油化工的发展水平。乙烯在一定条件下能发生如下转化,根据题意回答:
 (1)、CH3CH2OH的化学名称是(填“乙醇”或“乙酸”)。(2)、CH3COOH中的官能团是(填“羧基”或“羟基”)(3)、C2H4和H2O在催化剂存在时反应生成CH3CH2OH的反应类型是(填“化合反应”或“加成反应”)。
(1)、CH3CH2OH的化学名称是(填“乙醇”或“乙酸”)。(2)、CH3COOH中的官能团是(填“羧基”或“羟基”)(3)、C2H4和H2O在催化剂存在时反应生成CH3CH2OH的反应类型是(填“化合反应”或“加成反应”)。 -
9、非金属及其化合物在生产生活中应用广泛,根据题意回答:(1)、SO2能使品红溶液褪色,说明SO2具有(填“强氧化性”或“漂白性”)。(2)、太阳能电池板的使用,极大促进了人们对太阳能的开发利用,太阳能电池板的主要成分是(填“硅”或“二氧化硅”)。(3)、为了延长食品的保存时间,熟食包装袋中通常都要充入气体对食品进行抗氧化保护。适宜作为食品保护气的是(填“N2”或“NH3”)。
-
10、金属化合物应用广泛,回答下列问题:(1)、丹霞地貌的岩层因含有(填“Fe2O3”或“Fe3O4”)而呈红色。(2)、Cs位于元素周期表的第六周期第ⅠA族,Cs的金属性比Na(填“强”或“弱”)。(3)、铝是地壳中含量最多的金属元素。具有两性的含铝化合物是(填“Al2O3”或“AlCl3”)。
-
11、二氯二乙硫醚俗称芥子气,化学式为C4H8Cl2S,熔点为14.4℃,沸点为216℃。因具有挥发性,有像芥末的味道而得名,主要用于有机合成、制作药物等。下列关于芥子气的叙述正确的是A、芥子气的摩尔质量为159g B、标准状况下,1mol芥子气的体积为22.4L C、1mol芥子气中含有2NA个氯原子 D、芥子气属于氢化物
-
12、是工业制硫酸过程中的关键步骤。在一定温度下,向一密闭容器中投入2mol SO2和1mol O2充分反应,反应达到平衡时,下列相关说法正确的是A、SO2和O2完全转化成SO3 B、SO2、O2浓度相等 C、SO2和O2不再反应 D、生成SO3的量不再变化
-
13、化学是一门以实验为基础的自然科学,下列关于实验的叙述正确的是A、过滤时需要用到的玻璃仪器有烧杯、玻璃棒和普通漏斗 B、采用蒸馏的方法可以从NaCl溶液中获取NaCl固体 C、在容量瓶中溶解NaCl并定容,配制一定物质的量浓度的NaCl溶液 D、用加热NH4Cl分解的方法制取氨气
-
14、对于如图所示的铜锌电池,下列相关说法错误的是
 A、Zn电极失去电子 B、移向Cu电极 C、Cu电极为正极 D、装置将化学能转化成电能
A、Zn电极失去电子 B、移向Cu电极 C、Cu电极为正极 D、装置将化学能转化成电能 -
15、氯化亚铁是实验室常见的溶液,在配制时需要加入少量铁粉,加入铁粉的目的是A、防止Fe2+被氧化 B、防止Fe2+被还原 C、防止Fe2+水解 D、防止Fe2+与酸反应
-
16、采用下列措施,可以使化学反应速率减小的是A、升高温度 B、移出反应物 C、使用催化剂 D、增加原料
-
17、下列物质不可用作食品添加剂的是A、砒霜 B、苯甲酸钠 C、维生素C D、谷氨酸钠
-
18、下列化学用语的表述,不正确的是A、钠的原子结构:
 B、水的电子式:
B、水的电子式: C、乙烯的空间填充模型:
C、乙烯的空间填充模型: D、乙酸的分子式:C2H4O2
D、乙酸的分子式:C2H4O2
-
19、将一小块黄豆粒大小的金属钠投入滴有酚酞的冷水中,下列现象不会出现的是A、钠球四处游动,并发出“嘶嘶”的响声 B、钠球沉在水底,和水剧烈反应 C、滴有酚酞的溶液变成红色 D、金属钠熔化成一个闪亮的小球
-
20、“酒是陈年香”是因为酒在长期放置的过程中氧化生成的乙酸与乙醇发生反应生成了具有香味的乙酸乙酯,反应的化学方程式为 , 从反应类型上看,上述反应属于A、置换反应 B、取代反应 C、加成反应 D、加聚反应