相关试卷
- 江苏省扬州市江都区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市高新区2016-2017学年九年级上学期化学期末考试试卷
- 江苏省常州市2016-2017学年九年级上学期化学期末考试试卷
- 江苏省苏州市工业园区2017-2018学年九年级上学期化学12月调研考试试卷
- 江苏省扬州市江都区五校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省扬州市邗江区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省泰州市医药高新区2017-2018学年九年级上学期化学期中考试试卷
- 江苏省常州市金坛区2017-2018学年九年级上学期化学期中质量调研考试试卷
- 江苏省扬州实验学校2017-2018学年九年级上学期化学期中考试试卷
- 江苏省苏州市相城区2015-2016学年九年级化学一模考试试卷(4月)
-
1、金属蚀刻画是我国一项高超的艺术制作技艺,化学探究学习兴趣小组想利用废弃的金属片亲手制作简单的金属蚀刻画,请你参与进来一起完成本次探究活动。(1)、任务一:筛选金属底板
【提出问题】
I.选择金属考虑哪些问题?
II.金属的选择和蚀刻反应液之间存在什么关系?
【讨论】
I.要考虑金属活动性,选择容易反应的金属片,不能选择铜等活动性较稳定的金属。
II.反应在常温下进行,考虑金属与酸反应、金属与盐溶液发生反应等易于进行操作。
【实验操作】
I.同学们利用化学知识,选择金属活动性较强的金属用于实验。
II.最后,选择了铝片和铁片。区分铝片和铁片的物理方法是________(写一种)。
(2)、任务二:预处理金属底板和选择蚀刻液进行蚀刻【提出问题】
I.如何让金属只与反应液反应,而其他部分不参与反应?
II.选择什么蚀刻液进行实验?
【讨论】
I.通过课外知识,同学们讨论使用石蜡作为保护金属片的物质,因为石蜡在常温下难与酸和盐溶液发生化学反应。
II.同学们经过讨论,决定选择酸和盐溶液进行蚀刻反应。
【实验操作及现象】
I.用砂纸打磨铝片和铁片表面,去除氧化膜。这样处理的目的是。
II.用融化的石蜡均匀地覆盖在铝片和铁片上,待石蜡固化后用尖利的刀子划破石蜡,在铝片上画刻出“中国梦”的字样,在铁片上刻画出一朵小花。
III.随后将铝片浸入足量的甲蚀刻液中,将铁片浸入足量的乙蚀刻液中,一段时间后取出,小心去除金属表面的石蜡。
IV.铝片上“中国梦”字迹凹陷,没有附着物;铁片上的小花图案呈突起的红色。则他们选择的甲蚀刻液、乙蚀刻液分别是下列中的、(填序号)。
①硫酸铜溶液 ②硝酸银溶液 ③稀盐酸 ④氯化亚铁溶液 ⑤氯化钠溶液
其中,铁片上发生反应的化学方程式为。
(3)、任务三:讨论如何进行废液回收利用【讨论及分析】
铝片蚀刻废液处理,可加入足量铝片,得到的溶液中的溶质为________,回收保存。
【结果】通过大家分析,一直通过讨论分析的可行性评价,可以实施。
【反思】化学学习不但激发我们对物质世界的好奇心,还能发展科学思维、创新精神与实践能力,促进我们对物质世界深层次认识,培养我们科学态度和社会责任。
-
2、化学是一门以实验为基础的学科,某小组利用如图装置制备气体。回答下列问题。
 (1)、检查B装置气密性的方法是________。(2)、实验室用A装置制取氧气,发生反应的化学方程式为 , 若用C装置收集氧气,氧气应从(填“m”或“n”)端通入。(3)、若用D装置收集氧气,集气瓶内装35%的水(其余部分为空气),收集的气体恰好能使带火星的木条复燃,则能使带火星木条复燃的氧气最低含量为________%(用体积分数表示)。
(1)、检查B装置气密性的方法是________。(2)、实验室用A装置制取氧气,发生反应的化学方程式为 , 若用C装置收集氧气,氧气应从(填“m”或“n”)端通入。(3)、若用D装置收集氧气,集气瓶内装35%的水(其余部分为空气),收集的气体恰好能使带火星的木条复燃,则能使带火星木条复燃的氧气最低含量为________%(用体积分数表示)。 -
3、中国芯,湖南造。现代科技的发展离不开芯片,硅是芯片的重要基材。如图是工业上以四氯硅烷(SiCl4)为原料制取高纯硅的微观示意图。
 (1)、保持乙的化学性质的最小粒子是________。(2)、该反应的化学方程式为 , 该反应属于(填基本反应类型)。(3)、参加反应的乙与生成物丙的质量比是________。
(1)、保持乙的化学性质的最小粒子是________。(2)、该反应的化学方程式为 , 该反应属于(填基本反应类型)。(3)、参加反应的乙与生成物丙的质量比是________。 -
4、阅读下面文章。
随着全球能源危机、气候变暖等环境问题的日益突出,“低碳”已经成为世界关注的焦点。高能耗、高排放的钢铁行业降低成本、节能与环保愈加重要,将生物质这种可再生碳源合理应用于钢铁生产,必会带来巨大的经济效益、环境效益和社会效益。
生物质是一切生命体新陈代谢产生的有机物质,如秸秆、锯末、牛粪等。生物质能本质上是太阳能的一种表现形式,具有可再生性、清洁性、丰富性和可替代性等特点。
生物质能替代化石能源用于钢铁生产成为研究和关注的热点,生物质碳化技术工艺如图所示。

研究发现,利用生物炭部分替代煤炭炼焦进行炼铁时,可使高炉的温室气体排放量降低23.5%左右。制备出的生物炭具有管状结构,有较高的比表面积,其燃烧性能以及与CO2气化反应性能均优于煤炭。
目前,我国已将生物质能开发列入国家“十二五”能源发展规划,未来在钢铁生产中的潜力巨大。
(1)、生物质能理论上可达到碳的零排放,原因是________。(2)、生物炭与CO2气化反应的化学方程式为________。(3)、生物炭燃烧性能优于煤炭的原因是________。 -
5、宣纸是我国传统的古典书画用纸,其制作工艺被列入首批国家级非物质文化遗产。以檀树茎皮和稻草等为原料生产宣纸的部分流程如图所示,请分析思考,解答问题:
 (1)、抄纸是用多孔的竹帘将纸浆捞出,其原理与实验基本操作________相同。(2)、晒纸时,在阳光下比阴凉处干得快,其微观解释为________。(3)、博物馆里一般把贵重字画保存在充满氮气的圆桶中,以防止宣纸蛀虫和氧化变黄,原因是________(写一点)。
(1)、抄纸是用多孔的竹帘将纸浆捞出,其原理与实验基本操作________相同。(2)、晒纸时,在阳光下比阴凉处干得快,其微观解释为________。(3)、博物馆里一般把贵重字画保存在充满氮气的圆桶中,以防止宣纸蛀虫和氧化变黄,原因是________(写一点)。 -
6、天气瓶可用来预测天气变化,瓶内液体结晶的形态会随温度而发生改变。制作天气瓶需用到硝酸钾和氯化铵固体,下图是两种物质的溶解度曲线。
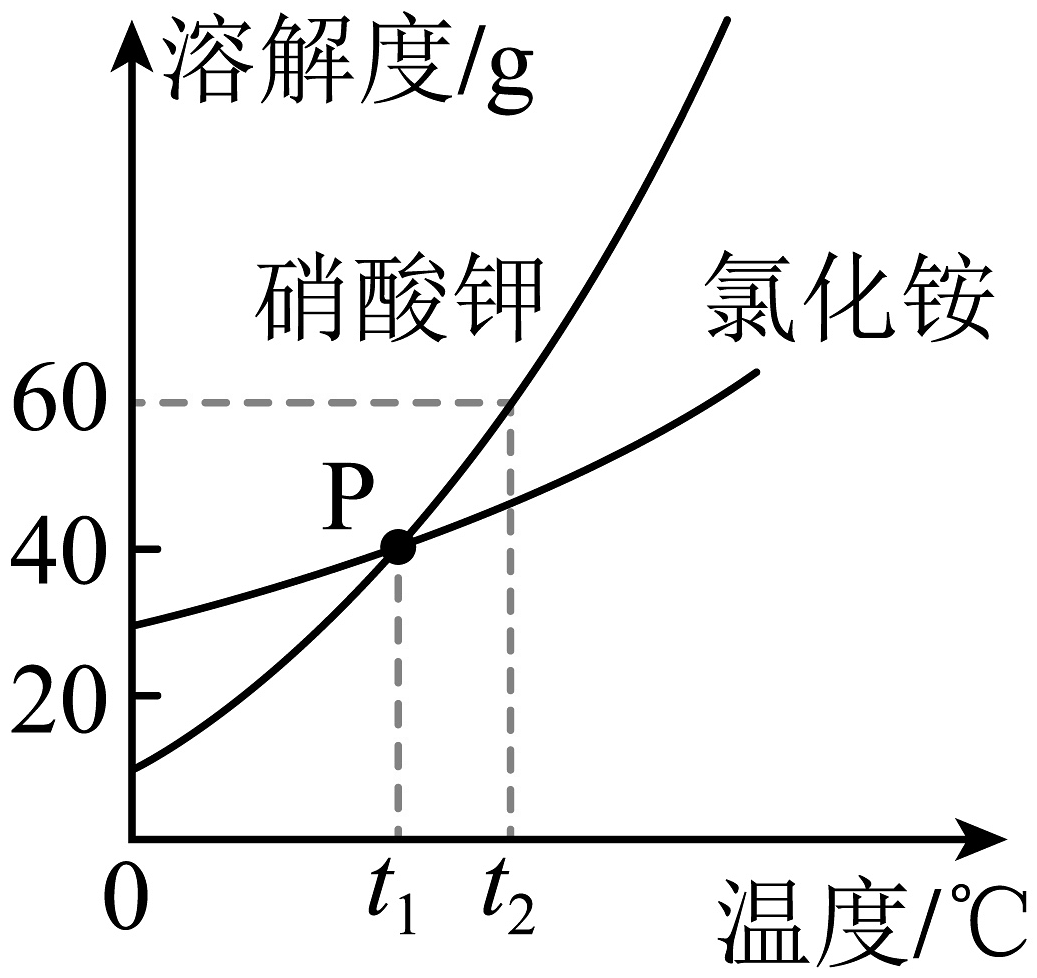 (1)、当温度小于________℃时,氯化铵的溶解度大于硝酸钾。(2)、时,50g硝酸钾加入到50g水中,充分溶解后所得溶液的质量为________g。(3)、时,分别将等质量的硝酸钾、氯化铵的饱和溶液升温到 , 硝酸钾溶液中溶质的质量________(填“大于”“等于”或“小于”)氯化铵溶液中溶质的质量。
(1)、当温度小于________℃时,氯化铵的溶解度大于硝酸钾。(2)、时,50g硝酸钾加入到50g水中,充分溶解后所得溶液的质量为________g。(3)、时,分别将等质量的硝酸钾、氯化铵的饱和溶液升温到 , 硝酸钾溶液中溶质的质量________(填“大于”“等于”或“小于”)氯化铵溶液中溶质的质量。 -
7、化学与生活、生产息息相关,请运用化学知识回答下列问题:(1)、小苏打不仅能用于焙制糕点,还能用于治疗胃酸过多症,其化学式为________。(2)、长沙臭豆腐起源于湘阴油炸豆腐,是皮酥内软口感极佳的小吃,臭豆腐可提供的主要营养素是________。
-
8、下列关于溶液的说法正确的是A、溶液都是无色透明的液体 B、气体、液体、固体都可以作为溶液的溶质 C、溶液由溶质和溶剂组成,所以溶液的质量和体积等于溶质和溶剂的质量和体积 D、溶液具有均一性、稳定性,所以具有均一性、稳定性的液体都是溶液
-
9、小组同学用如图装置探究可燃物燃烧的条件,向上提拉燃烧匙,直至a处白磷、b处红磷露出水面,观察到仅a处的白磷燃烧(已知白磷、红磷的着火点分别为40℃、60℃),下列说法正确的是
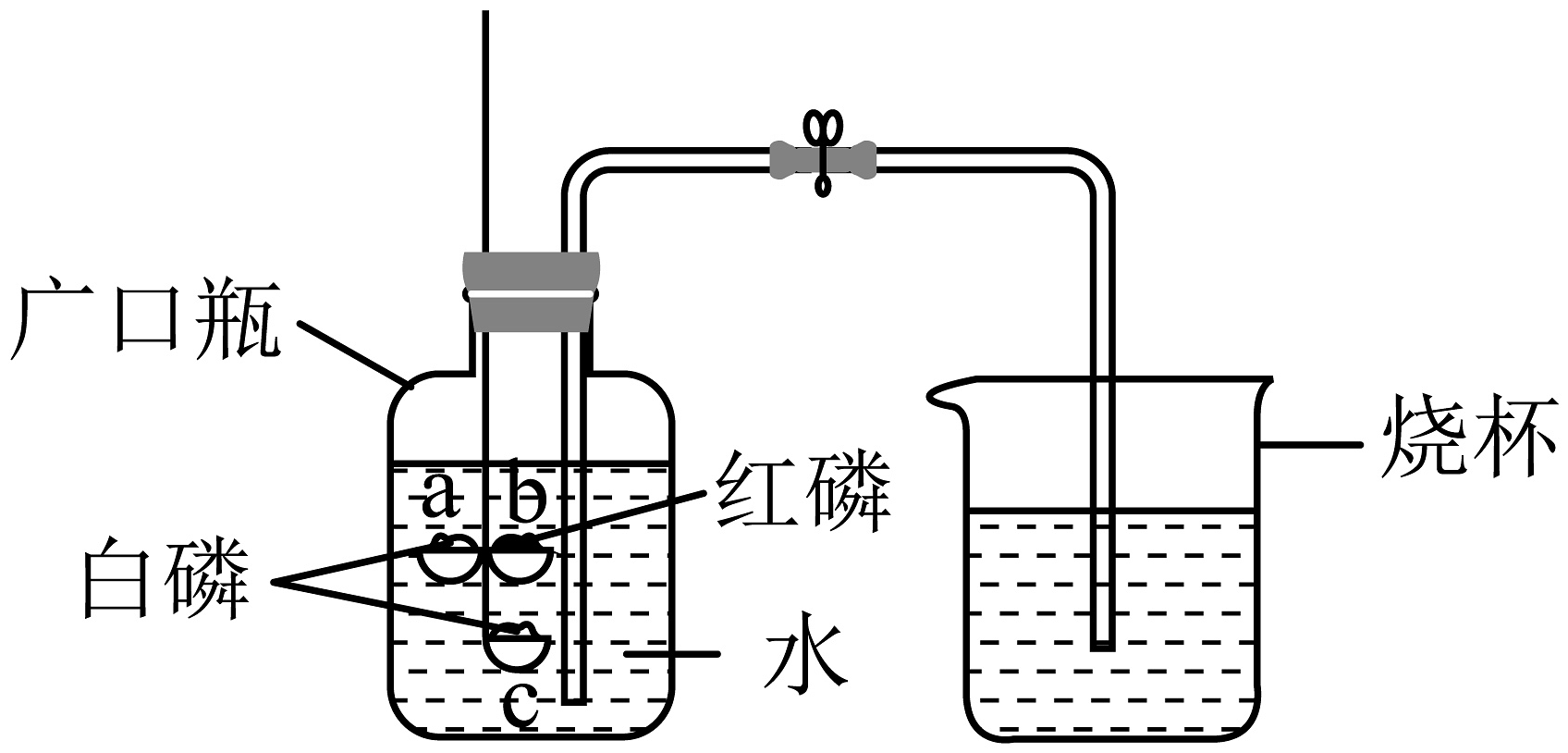 A、广口瓶内水的温度可能是30℃ B、实验中红磷不燃烧,说明红磷不是可燃物 C、对比a、c处的现象,证明燃烧需要与氧气接触 D、冷却至室温后打开弹簧夹,广口瓶内的水流至烧杯中
A、广口瓶内水的温度可能是30℃ B、实验中红磷不燃烧,说明红磷不是可燃物 C、对比a、c处的现象,证明燃烧需要与氧气接触 D、冷却至室温后打开弹簧夹,广口瓶内的水流至烧杯中 -
10、下列物质性质和用途对应关系不正确的是A、活性炭有吸附性,可用作除味剂 B、熟石灰有碱性,可用于治疗胃酸过多 C、油脂能溶于汽油,可用于除油污 D、铁粉能与氧气和水反应,可用作食品干燥剂
-
11、某中学考查通过实验检验生活中常见物质的酸碱性,下列物质中呈酸性的是A、食盐水 B、蒸馏水 C、肥皂水 D、白醋
-
12、合理使用化肥对“发展粮食产业,助力乡村振兴”具有重要意义。下列化肥属于复合肥的是A、KNO3 B、K2SO4 C、CO(NH2)2 D、NH4HCO3
-
13、打火机的燃料是丁烷(化学式为C4H10)。下列有关说法正确的是A、丁烷分子中含有氢气 B、丁烷由碳、氢原子构成 C、丁烷的燃烧产物只有二氧化碳和水 D、丁烷中碳、氢元素的质量比为24:5
-
14、我国近代科学家徐寿将西方化学知识系统引入中国,他所创造的许多元素的中文名称一直沿用至今。下列元素名称与符号均正确的是A、锰(Mn) B、碳(c) C、氯(Al) D、纳(Na)
-
15、凤凰古城着力顺应国家绿色发展号召,开发和使用新能源,打造低碳环保的绿色文明城市。下列属于新能源的是A、天然气 B、石油 C、煤 D、太阳能
-
16、下列用来制作苗族服饰的材料中,属于金属材料的是A、火麻 B、银器 C、黄蜡 D、彩线
-
17、下列凤凰古城中特色相关的情境中,主要发生化学变化的是A、凤凰姜糖的切割 B、苗族银饰的捶打 C、烧火熏制腊肉 D、酒鬼酒的装瓶
-
18、《天工开物》中记载了我国古代利用炉甘石冶炼金属锌的工艺,其反应原理为ZnCO3 + 2CZn + xCO↑下列有关说法正确的是A、CO中碳元素的化合价为+1价 B、ZnCO3属于氧化物 C、根据质量守恒定律可知x为3 D、该反应属于复分解反应
-
19、工业上吸收SO2的化学方程式为2NaOH+SO2=Na2SO3+H2O。(1)、工厂排出的SO2如果未经处理或未达标排放到空气中,可能导致降雨的酸性________(填“增强”或“减弱”)。(2)、若吸收6.4gSO2 , 需消耗10%的NaOH溶液的质量是多少?
-
20、
某化学实验小组受市售牙膏的启发,以乳酸为研究对象,制作一支使牙齿健康、清洁、亮白的牙膏。
任务一:认识口腔环境
【查阅资料】正常唾液的pH范围为6.6~7.1.
实验1:测定唾液的酸碱性
(1)将棉签放置舌下约1分钟,棉签湿润后取出,将紫色石蕊溶液滴至棉签上。石蕊溶液颜色并没有发生改变,你认为原因是________。实验2:用pH计测定唾液的酸碱度
用pH计检验收集的唾液样本,测得结果为6.7.
任务二:牙膏材料的选择
(2)牙膏的主体材料是摩擦剂,当前主流摩擦剂主要有水合硅石和碳酸钙两种。小组同学选择水合硅石作为摩擦剂,并在主体材料中添加________(填元素名称),可以预防龋齿。【查阅资料】
①若食物残渣浸润在牙齿周围,经口腔微生物发酵产生乳酸,会使原本接近中性的口腔环境变为酸性。当pH<5.5时,会对牙齿造成伤害,甚至引起疾病。为了清除口腔中的乳酸(C3H6O3),还需要添加能和其反应的物质。
②乳酸在水中会产生H+和乳酸根离子()。
实验3:氢氧化钠、碳酸氢钠分别与乳酸反应
分别取适量的氢氧化钠、碳酸氢钠于试管中,各加入2mL乳酸溶液,观察到如下实验现象。
物质
氢氧化钠
碳酸氢钠
实验现象
白色固体消失
有气泡冒出
(3)两种物质都能与乳酸反应,小组同学最终选择向牙膏中添加碳酸氢钠,原因是氢氧化钠有________性。(4)白色固体消失,不一定能说明氢氧化钠与乳酸反应。请说明原因并设计实验证明氢氧化钠能与乳酸反应:________。任务三:测定市售牙膏中碳酸氢钠含量、制作牙膏
实验4:测定市售牙膏中碳酸氢钠含量
(5)取一定量的牙膏于试管中,加入足量的稀盐酸。通过测量生成的CO2的质量来计算出牙膏中NaHCO3的含量。请写出稀盐酸与碳酸氢钠反应的化学方程式________。实验5:动手制作牙膏
实验小组通过反复查找资料,确定制作牙膏的配比:水合硅石50%、碳酸氢钠20%、甘油15%、草莓香料9.9%、水5%、氟化钠0.1%。
(6)牙膏制作好后,请帮他们设计产品的宣传口号________。【项目交流】产品的研发遵循物质的性质决定用途的规律。