相关试卷
-
1、
某社团小组对暖宝宝展开了项目式学习。

【查阅资料】
ⅰ.成分中蛭石和吸水树脂化学性质极为稳定,有保温作用。
ⅱ.使用时,打开包装袋让空气通过无纺布,在食盐的作用下与产品成分中的某些物质发生反应,生成氢氧化铁并放出热量。氢氧化铁不稳定,受热会分解为氧化铁和水。
任务一:认识暖宝宝的主要成分
(1)产品成分中要把铁研磨成铁粉的目的是。
任务二:探究暖宝宝的发热原理
(2)从能量转化角度:暖宝宝的发热过程是将化学能转化为能的过程;某同学建议把无纺布改成塑料袋,该方案是否可行,请说明理由:。
(3)写出氢氧化铁分解反应的化学方程式:。
任务三:探究暖宝宝的最佳原料配比
小组同学设计如下对照实验。
实验组别
铁粉/g
活性炭/g
食盐/g
蛭石/g
水/mL
1
3
0.5
0.5
0.5
1
2
3
0.5
1
0.5
1
3
3
0.5
1
1
1
4
3
0.5
1
1
1.5
5
3
1
1
1
1
利用传感器测定各组实验的氧气浓度和温度变化情况如图所示。
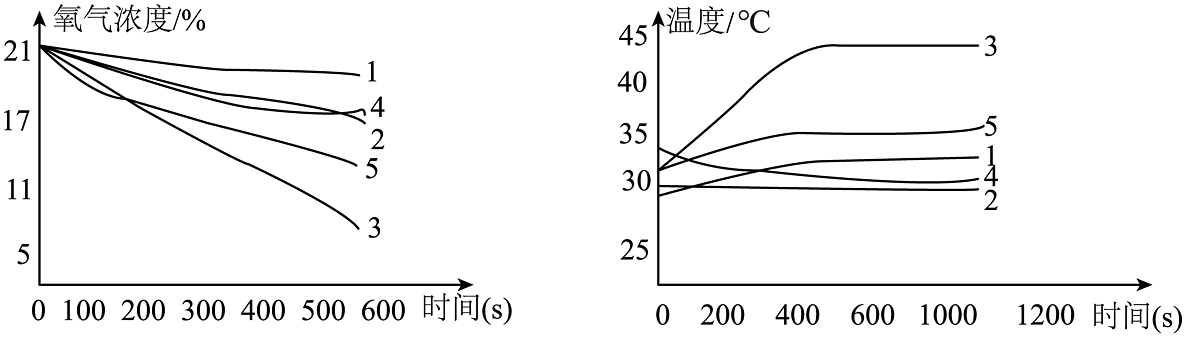
(4)通过对比第组和第组信息,可探究食盐的量会对放热效果造成影响。第4组温度变化不大的原因是。
(5)结合图示判断第组的原料质量比最佳,理由是。
-
2、某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从下图中选择装置进行了氧气的制备实验。
 (1)、仪器①的名称是;(2)、用高锰酸钾制取较纯净氧气反应的化学方程式为 , 选用的发生装置和收集装置是(A—F中选填序号),该装置还缺少的用品是 , 制取过程中需等到(填现象)时才能将导管伸入集气瓶中。(3)、实验室若用双氧水制氧气,反应的化学方程式为。(4)、用G装置收集氧气,气体从(填“a”或“b”)端进入。
(1)、仪器①的名称是;(2)、用高锰酸钾制取较纯净氧气反应的化学方程式为 , 选用的发生装置和收集装置是(A—F中选填序号),该装置还缺少的用品是 , 制取过程中需等到(填现象)时才能将导管伸入集气瓶中。(3)、实验室若用双氧水制氧气,反应的化学方程式为。(4)、用G装置收集氧气,气体从(填“a”或“b”)端进入。 -
3、科学家利用“人造树叶”催化生成乙醇的微观过程如下:
 (1)、反应中,可供给呼吸的物质是(填字母),属于氧化物的有种。(2)、写出该过程反应的化学方程式。(3)、该研究有利于缓解的环境问题是。
(1)、反应中,可供给呼吸的物质是(填字母),属于氧化物的有种。(2)、写出该过程反应的化学方程式。(3)、该研究有利于缓解的环境问题是。 -
4、在漫长的一段时间内,人们认为水是组成世间万物的一种元素,阅读下列材料并回答问题。
【材料1】18世纪,普利斯特里利用锌和稀硫酸制得“可燃空气”,将其与空气混合点燃,容器内壁上出现了水雾。
【材料2】1781年,卡文迪什证实了普利斯特里的发现,并用纯氧代替空气进行实验,证明生成的液体确实是水。
【材料3】1783年,拉瓦锡进行实验,将水蒸气通过灼热的铁管,一段时间后,在出口处收集到一种可燃气体,水的质量减少,铁管的质量增加。至此,“水是由氢元素和氧元素组成”的观点得到了公认。
【材料4】1809年,法国化学家盖吕萨克通过实验确定了每个水分子是由2个氢原子和1个氧原子构成。
(1)、材料1中,“可燃空气”是。(2)、材料2中卡文迪什用纯氧代替空气的原因是。(3)、材料3中经实验测定,足量的水与168g铁反应只生成铁的氧化物固体和8g氢气,结合材料4可知该固体的化学式是。(4)、用如图装置进行电解水的实验。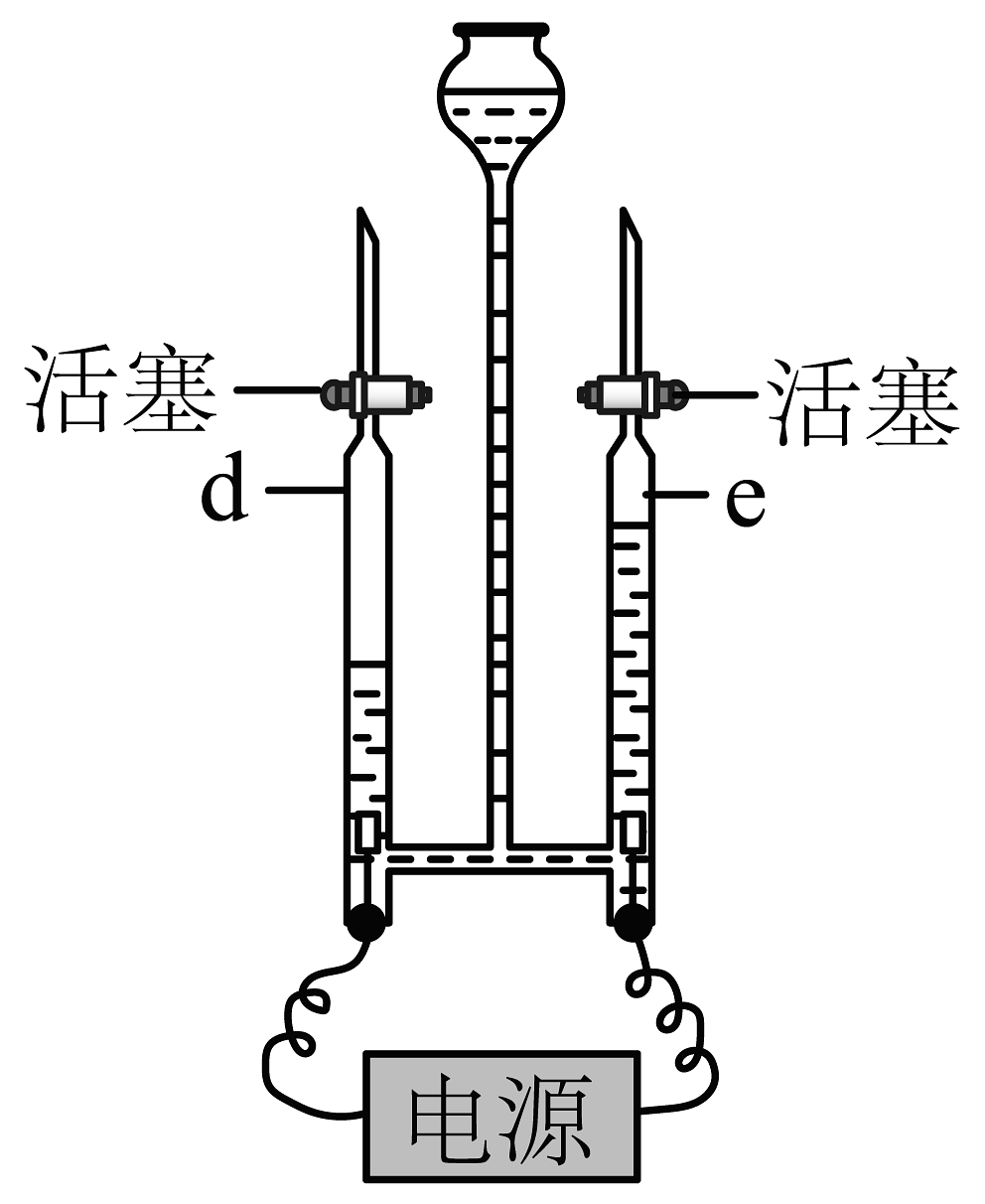
①装置中d端连接的是电源的(填“正”或“负”)极。
②通电后,两端电极上可以观察到的现象是 , 反应的化学方程式为 , 该反应的基本反应类型是。
-
5、“宏观、微观、符号”三重表征是化学独特的表示物质及其变化的方式。

 (1)、根据图1,写出一种由微观粒子X构成的物质(填化学式)。(2)、图2中B为某原子结构示意图,则m的值为 , 在化学反应中容易(填“得到”或“失去”)电子;A~D属于同种元素的是(填标号)。(3)、图3中:
(1)、根据图1,写出一种由微观粒子X构成的物质(填化学式)。(2)、图2中B为某原子结构示意图,则m的值为 , 在化学反应中容易(填“得到”或“失去”)电子;A~D属于同种元素的是(填标号)。(3)、图3中:①溴元素属于(填“金属”或“非金属”)元素,位于元素周期表的第周期;
②溴元素与图2中的B、D元素化学性质相似,原因是;
③溴化镁是一种重要的污水处理剂,其化学式是。
-
6、
分离混合物,是化学上研究物质重要的思路。
Ⅰ.空气的分离

(1)流程中物质①是________。
(2)氧气能和许多物质发生化学反应。请写出一个有氧气参加的反应________(用化学方程式表示)。
Ⅱ.水的净化
小明同学对一瓶浑浊的河水进行净化,其实验过程如图1所示。请回答以下问题。

(3)A物质的名称是________。
(4)下列有关操作①的说法中,正确的有________(填标号)。
a.该实验用到的玻璃仪器有漏斗、烧杯、玻璃棒
b.玻璃棒起到引流的作用
c.若滤液仍然浑浊,可能的原因是漏斗内液面高于滤纸的边缘
d.过滤后的水为纯净物
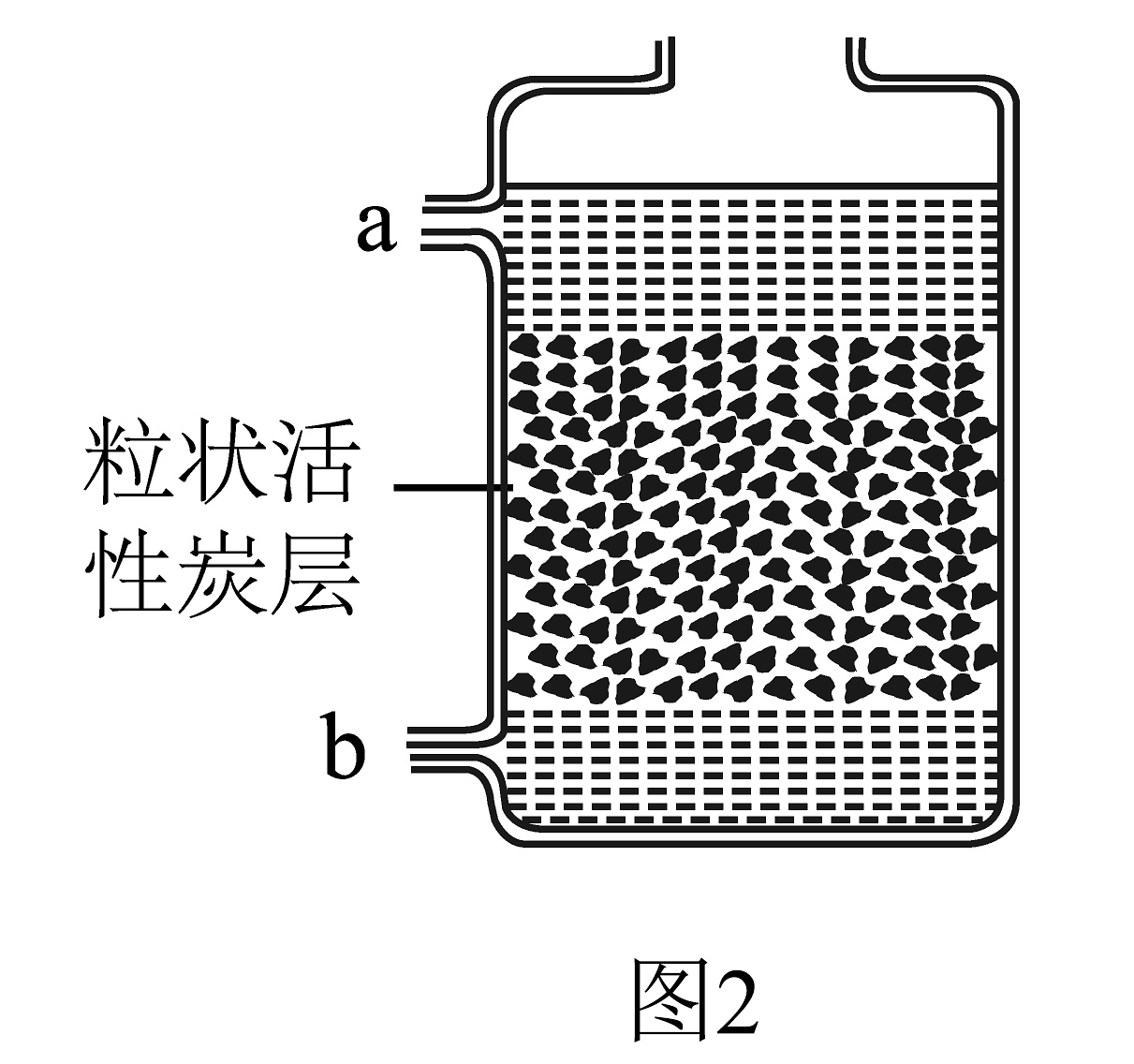
(5)操作②的装置示意图如图2所示,活性炭的主要作用是________,该装置中的入水口是________(填“a”或“b”)端。
【反思】
(6)以上两种分离混合物的流程都是按被分离物质的________不同,选择适当的方法进行分离。
(7)下列有利于保护空气和水资源的做法有______(填标号)。
A. 工厂的烟囱加高排放 B. 农业上提倡大量使用化肥和农药 C. 城市生活污水经处理达标后排放 D. 园林浇灌改大水漫灌为喷灌、滴灌 -
7、化学用语是国际通用语言。(1)、从“微观模型”到“化学符号”:“
 ”表示氧原子“
”表示氧原子“ ”表示氮原子
”表示氮原子微观模型


化学符号
①
②
(2)、从“化学符号”到“文字信息表达”:写出下列符号中数字“2”的意义。①;②;
(3)、从“文字信息表达”到“化学符号”:①两个氢离子;②氦气。
-
8、查阅资料:在密闭的空间内红磷消耗空气中的氧气约至7%时熄灭。柯柯用如图所示装置来测定空气中氧气的含量。加热试管,红磷开始燃烧,待红磷熄灭并冷却至室温后打开弹簧夹。下列关于该实验的说法错误的是
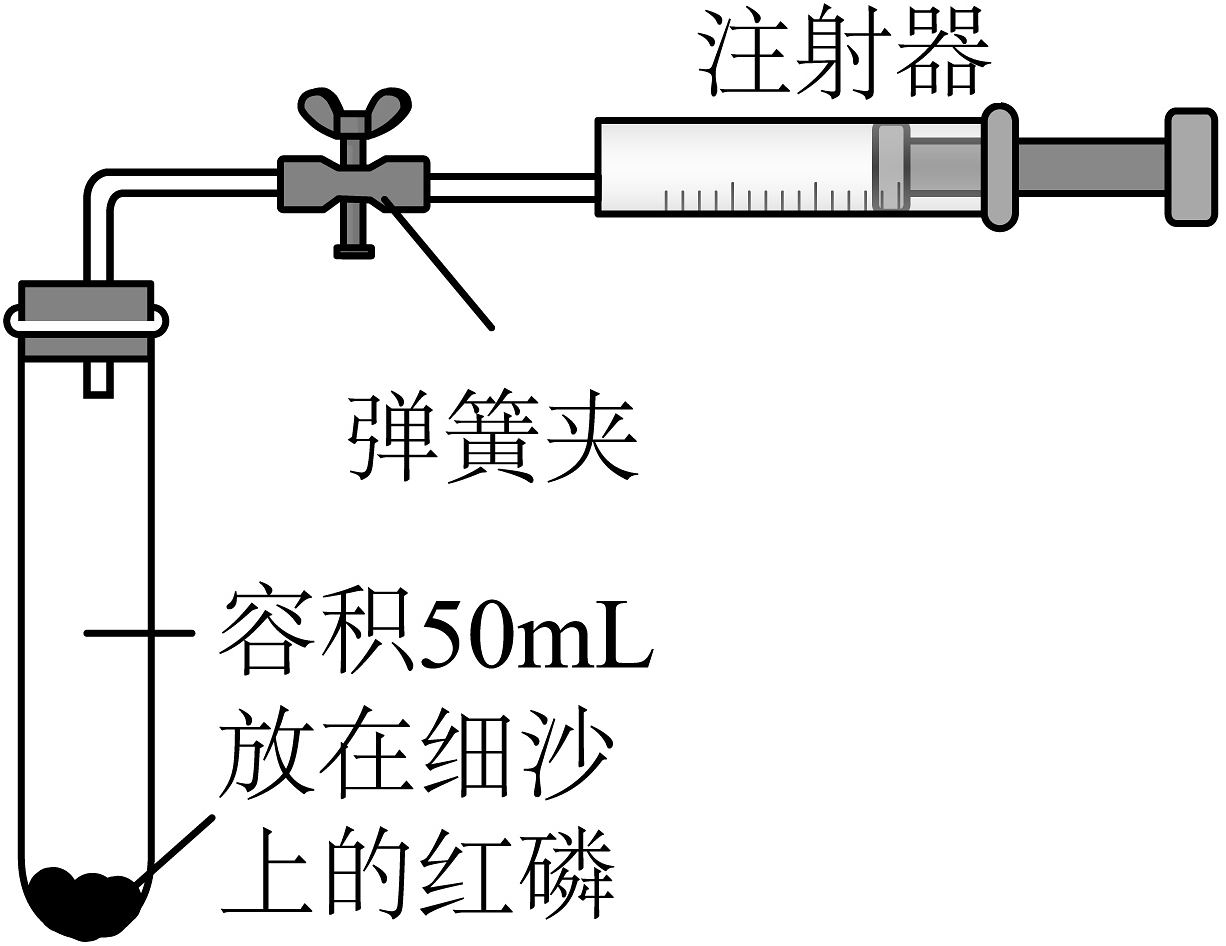 A、试管底部细沙的目的是为了吸收有毒的五氧化二磷 B、要达到实验目的,试管中的红磷不能更换为木炭 C、若要验证实验结束时氧气剩余7%,注射器预装7mL的水不够 D、红磷燃烧停止后打开弹簧夹,要等到注射器活塞不再移动才能读数
A、试管底部细沙的目的是为了吸收有毒的五氧化二磷 B、要达到实验目的,试管中的红磷不能更换为木炭 C、若要验证实验结束时氧气剩余7%,注射器预装7mL的水不够 D、红磷燃烧停止后打开弹簧夹,要等到注射器活塞不再移动才能读数 -
9、一个密闭容器中有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示,下列推理中正确的是
物质
X
Y
Z
Q
反应前的质量/g
8
10
1
21
反应后的质量/g
9
21
待测
9
A、Z与此反应无关 B、反应中Y与Q改变的质量之比为1:1 C、该反应是分解反应 D、X一定为化合物 -
10、鉴别空气、氧气和二氧化碳气体的最佳方法是A、观察气体的颜色 B、伸入燃着的木条 C、闻气体的气味 D、倒入澄清的石灰水
-
11、关于空气、二氧化硫、氧化铜和硫酸这几种物质,下列说法正确的是A、都含有氧分子 B、都不含氧分子 C、都是化合物 D、都含氧元素
-
12、下列关于物质燃烧的现象描述正确的是A、红磷在空气中燃烧产生大量烟雾 B、木炭完全燃烧后生成黑色固体 C、铜在空气中加热生成黑色的氧化铜 D、硫燃烧时生成有刺激性气味的气体
-
13、自来水可用氯气杀菌消毒。氯气中氯元素的化合价是A、 B、 C、0 D、
-
14、下列事实及对这些事实的解释,二者不相符合的是A、汽油挥发总体积变大——分子体积变大 B、夏天钢轨之间的缝隙变小——原子之间有间隔 C、糖是甜的,醋是酸的——不同分子性质不同 D、氧化汞受热分解生成汞和氧气——分子在化学反应中可以再分
-
15、下列物质的性质与用途对应关系,错误的是A、氧气有助燃性——作燃料 B、镁燃烧时发出耀眼白光——作照明弹 C、常温下氮气化学性质稳定——作焊接金属保护气 D、稀有气体在通电时能发出不同颜色的光——作霓虹灯
-
16、实验是学习化学的重要途径。根据下图回答氧气的实验室制取与性质有关问题:

 (1)、反应原理:用高锰酸钾制取氧气的化学方程式为。(2)、注意事项:用装置A和装置B制取氧气,为确保装置不漏气,应先检查装置的;收集满氧气后,为防止水倒吸,应先(填“将导管移出水面”或“熄灭酒精灯”)。(3)、气体收集:用装置C收集氧气,是利用了氧气的密度比空气的性质;检验氧气集满的操作为。(4)、性质验证:将装置A中产生的氧气通向D中红热的木炭,木炭燃烧变旺,说明氧气具有的化学性质是。装置E中发生反应的化学方程式为。(5)、氯酸钾粉末在二氧化锰作催化剂并加热的条件下,可分解生成氯化钾和氧气。若将15g氯酸钾和二氧化锰的固体混合物充分加热,待完全反应后称量剩余物为10.2g,则原混合物中氯酸钾为多少克?
(1)、反应原理:用高锰酸钾制取氧气的化学方程式为。(2)、注意事项:用装置A和装置B制取氧气,为确保装置不漏气,应先检查装置的;收集满氧气后,为防止水倒吸,应先(填“将导管移出水面”或“熄灭酒精灯”)。(3)、气体收集:用装置C收集氧气,是利用了氧气的密度比空气的性质;检验氧气集满的操作为。(4)、性质验证:将装置A中产生的氧气通向D中红热的木炭,木炭燃烧变旺,说明氧气具有的化学性质是。装置E中发生反应的化学方程式为。(5)、氯酸钾粉末在二氧化锰作催化剂并加热的条件下,可分解生成氯化钾和氧气。若将15g氯酸钾和二氧化锰的固体混合物充分加热,待完全反应后称量剩余物为10.2g,则原混合物中氯酸钾为多少克? -
17、探究“分解过氧化氢制氧气的反应中二氧化锰的作用”。
 (1)、实验原理:图2中发生反应的化学方程式为。(2)、实验现象:图1与图3中的现象不同,常温下,图1试管内也产生了氧气,但带火星木条不能复燃的原因可能是什么?(3)、实验结论:二氧化锰可使过氧化氢分解的速率。
(1)、实验原理:图2中发生反应的化学方程式为。(2)、实验现象:图1与图3中的现象不同,常温下,图1试管内也产生了氧气,但带火星木条不能复燃的原因可能是什么?(3)、实验结论:二氧化锰可使过氧化氢分解的速率。 -
18、如下图是测定氧气含量的两种方法,请回答下列问题:
 (1)、写出图2中反应的化学方程式。(2)、图2与图1比较有什么优点?(列举一条)。
(1)、写出图2中反应的化学方程式。(2)、图2与图1比较有什么优点?(列举一条)。 -
19、从分子角度解释下列问题:(1)、湿衣服在阳光下比在阴凉处干得快。(2)、加压时,6000L氧气可装入容积为40L的钢瓶中。
-
20、A、B、C、D四种物质是初中已学过的主要物质,A、C是组成元素完全相同的化合物;B是气体单质;在一定条件下,A分解可生成B和C;C是人体中含量最多的物质。它们之间有如图所示的转化关系(部分物质和反应条件已经略去)。请写出A的化学式;写出B转化为C的化学方程式。
