相关试卷
-
1、合理施用化肥可提高农作物的产量。碳酸氢铵是一种常见的化肥,其化学式为。(1)、碳酸氢铵的相对分子质量是。(2)、碳酸氢铵中氢、氧元素的质量比是。(3)、现有碳酸氢铵,其中氮元素的质量为g。
-
2、
化学小组在开展“铁丝在氧气中燃烧实验”时,发现不易成功。决定对该实验进行更深入的探究,请你一起参与。
活动一:重现课本实验
[实验1]如图1所示,将细铁丝绑上火柴,点燃火柴,用坩埚钳将细铁丝伸入盛有氧气的集气瓶中。

(1)铁丝在氧气中燃烧,写出该反应的文字表达式。
(2)实验中,点燃火柴后,将铁丝伸入盛有氧气的集气瓶中的最佳时机是待火柴快燃尽时,不宜过早,其目的是防止 , 故进行该实验时,宜选择容积为(填“125”或“250”)的集气瓶更容易成功。
活动二:探究铁丝引燃的方式
实验中发现不容易控制铁丝伸入集气瓶的时间,小组同学进行如下改进。
[实验2]如图2所示,实验中,观察到铁丝剧烈燃烧,火星四射。

(3)如果使用已学过的化学试剂来代替火柴,你会使用(写一种)。
活动三:探究铁丝燃烧时长的影响因素
[实验3]如图3所示,从同一长铁丝上分别截取3根长度相同的铁丝,将1根拉直、另2根绕成直径大小不同的螺旋状,下端系上燃着的小木条进行燃烧实验。每种形状的铁丝平行测量3次,所测得的实验数据如图4所示。

(4)实验中发现不管铁丝形状如何,其燃烧时长均在曲线附近,说明燃烧时长与铁丝是否绕成螺旋状(填“有关”或“无关”)。
(5)分析图4可知,铁丝在氧气中剧烈燃烧的时间与集气瓶内氧气的起始浓度的关系是。
(6)对铁与氧气反应的实验,写一个你认为还可进一步探究的问题是。
-
3、化学小组开展氧气性质和制取的跨学科实践活动,请你一起参与。
 (1)、模拟自然界的光合作用。
(1)、模拟自然界的光合作用。将图1装置置于阳光下一段时间,观察到有气泡产生。该收集气体的方法是 , 检验所收集的气体应进行的操作是。
(2)、利用改进后的图2装置进行炭块的燃烧实验。用气卿(能不断鼓入空气的装置)不断地向弯型具支试管中鼓入空气,同时用酒精灯给炭块加热,一段时间后,可观察到炭块呈红热状态;移去酒精灯,停止鼓入空气,再用酒精灯给高锰酸钾加热,观察到炭块剧烈燃烧,发出白光。
①图2中,仪器a的名称是。
②写出加热高锰酸钾发生反应的文字表达式:。
③实验说明,炭块燃烧的剧烈程度与有关。能说明碳与氧气发生反应,生成二氧化碳的实验现象是。
④实验结束时,应先进行的操作是(填字母序号)。
A.停止加热,熄灭酒精灯 B.将导管移出水面
-
4、
化学小组就“空间站的氧气和水从哪里来”的问题进行了探讨,请你参与。
方案一:从地球带上去。
(1)如图所示,空气通过“分子筛”可获得更高浓度的 , 由此可知两种分子的大小:(填“>”或“<”)。

(2)空间站供氧使用特种材料制成的氧气瓶,可充氧气至300倍大气压,一瓶氧气即可供航天员长时间使用,从微观粒子视角分析其原因:。
方案二:在天宫制取。
(3)早期空间站利用二氧化碳与过氧化钠在常温下反应获得氧气,同时生成碳酸钠。写出该反应的文字表达式:。
(4)如图是空间站内的部分物质循环示意图。

①空间站利用太阳能转为电能,水通电发生反应,获得氧气,该反应属于(填“化合”或“分解”)反应。
②结合图示,请你说出一种空间站内获得水的方法:。
-
5、图1是某品牌制氧杯,图2为内部结构示意图。使用时,先在甲杯中加入制氧剂A、制氧剂B,再加入清水,乙杯加入适量清水,放回,旋紧杯盖即可快速供氧。(制氧剂A是过碳酸钠,在水中溶解后转化为碳酸钠溶液和过氧化氢溶液。制氧剂B是二氧化锰。)
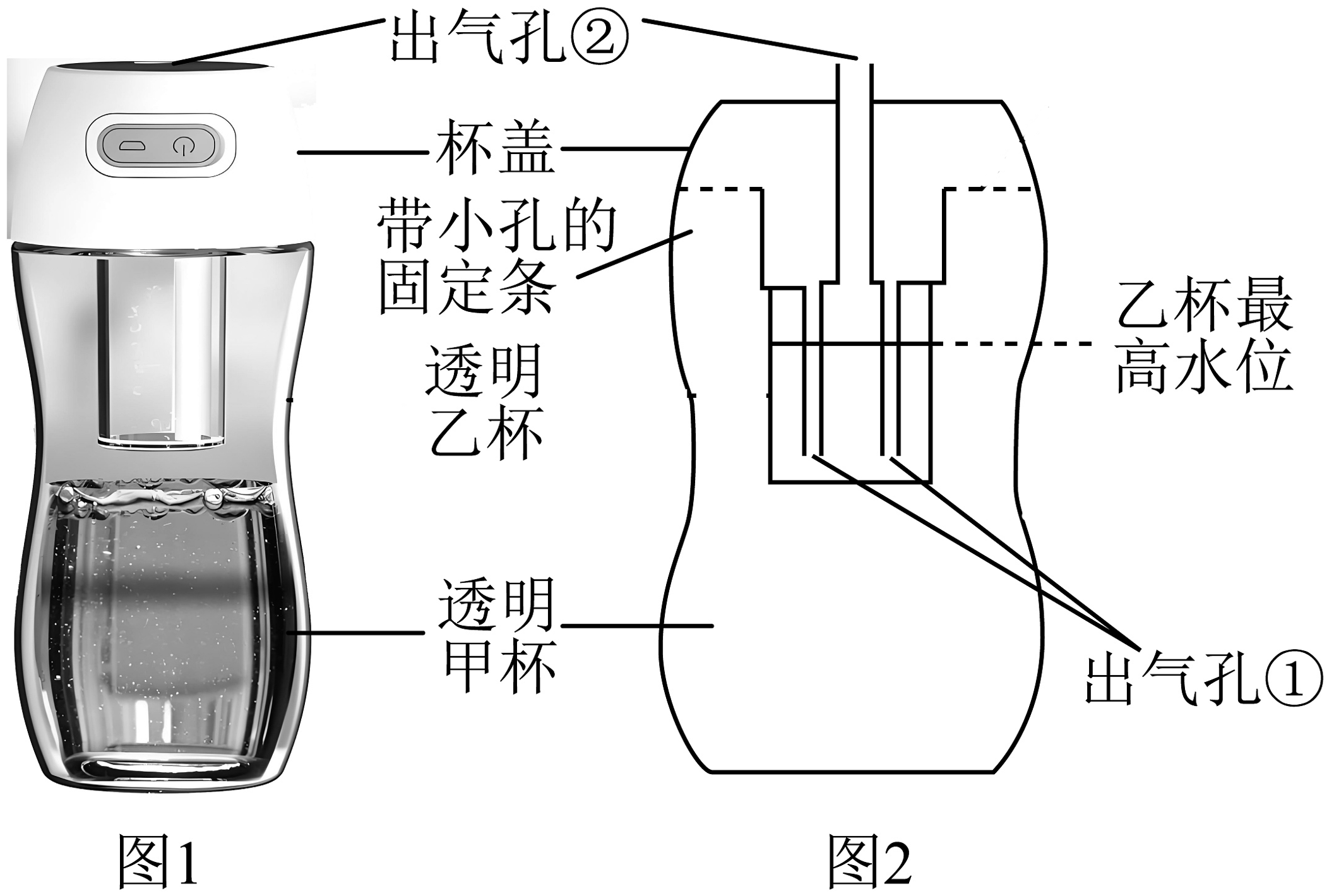 (1)、制氧杯能快速产生氧气的原因是(用文字表达式表示)。(2)、制氧杯使用过程中,手接触制氧杯有温热感,其原因是。(3)、在乙杯中加入清水的作用是(写一种)。(4)、采用透明杯体,当观察到 , 说明反应已结束。(5)、反应结束后,将甲杯中剩余物质进行过滤,所得滤渣(填“能”或“不能”)继续使用。(6)、相比较于大型制氧机、氧气罐供氧,制氧杯的优点是。
(1)、制氧杯能快速产生氧气的原因是(用文字表达式表示)。(2)、制氧杯使用过程中,手接触制氧杯有温热感,其原因是。(3)、在乙杯中加入清水的作用是(写一种)。(4)、采用透明杯体,当观察到 , 说明反应已结束。(5)、反应结束后,将甲杯中剩余物质进行过滤,所得滤渣(填“能”或“不能”)继续使用。(6)、相比较于大型制氧机、氧气罐供氧,制氧杯的优点是。 -
6、“生命吸管”是一种可以随身携带的小型水净化器,其工作原理如图所示。
 (1)、双层纺织网的作用是(填实验操作名称)。(2)、活性炭可以除去水中的色素和异味,是利用其具有性。(3)、碘树脂可杀菌消毒,生活饮用水还可通过来杀灭细菌。(4)、钠离子直径小于0.001微米,“生命吸管”(填“能”或“不能”)淡化海水。生产中常用膜分离技术淡化海水,结合自然界中水的循环,还能用的方法淡化海水。(5)、“生命吸管”使用一定时间后,流速会明显变慢,可能原因是。
(1)、双层纺织网的作用是(填实验操作名称)。(2)、活性炭可以除去水中的色素和异味,是利用其具有性。(3)、碘树脂可杀菌消毒,生活饮用水还可通过来杀灭细菌。(4)、钠离子直径小于0.001微米,“生命吸管”(填“能”或“不能”)淡化海水。生产中常用膜分离技术淡化海水,结合自然界中水的循环,还能用的方法淡化海水。(5)、“生命吸管”使用一定时间后,流速会明显变慢,可能原因是。 -
7、化学与能源密切相关。(1)、核聚变是未来最有希望的能源之一。图1是氢在元素周期表中的部分信息,图2是核聚变的原料之一氚的原子结构模型。

①氢原子的相对原子质量为。
②根据图2分析,图3中能表示氚原子结构示意图的是(填标号)。
③H和T都属于氢元素,是因为它们的相同。
(2)、氢气是理想燃料。①氢气具有可燃性,使用时应注意安全,点燃氢气前要。
②图4是氢气和氧气发生反应的微观模拟示意图,请在横线上补充完整。

-
8、生活中处处有化学。(1)、氮气作食物的保护气,说明氮气的化学性质(填“稳定”或“活泼”)。从宏观角度看,氮气是由组成的。(2)、节日里燃放的烟花中含有镁粉。镁在空气中燃烧的现象是 , 放热,生成白色固体。(3)、食盐,化学名为氯化钠。氯化钠是由(填微粒符号,下同)和构成的。“加碘食盐”中“碘”通常以碘酸钾的形式存在,在中,碘元素的化合价是。
-
9、下列基于实验事实的推理,正确的是A、水通电反应生成氢气和氧气,证明水由氢气和氧气组成 B、往溶液中加入少量 , 迅速产生气泡,可验证是催化剂 C、打开酒精瓶时嗅到酒精的气味,说明微粒在不断运动 D、点燃气体,火焰上方的干冷烧杯的内壁出现水雾,证明该气体一定是氢气
-
10、用如图装置完成测定空气中氧气含量的实验,瓶内空气体积为 , 该装置气密性良好。下列叙述正确的是( )
 A、红磷燃烧时产生大量白色烟雾 B、使用量程为的量筒使数据更精准 C、装置缺少止水夹,无法完成实验目的 D、集气瓶内液面先下降后上升
A、红磷燃烧时产生大量白色烟雾 B、使用量程为的量筒使数据更精准 C、装置缺少止水夹,无法完成实验目的 D、集气瓶内液面先下降后上升 -
11、中国科学家首次从月壤样品中发现新矿物——嫦娥石 , 关于的说法正确的是A、由46个原子构成 B、钙、氧原子个数比为 C、由5种元素组成 D、钙元素的质量分数最大
-
12、硫酸亚铁在工农业生产中有重要作用。在实验室里,某化学兴趣小组利用稀硫酸[硫酸和水的混合物]和废铁屑制取硫酸亚铁。该实验过程测得数据如图所示。提示:反应的方程式

请回答:
(1)、反应结束时,生成氢气的质量为g。(2)、计算参加反应的铁的质量(写出计算过程)。 -
13、
特定人群、环境对氧气的需求不同。如何基于特定需求设计和制作简易供氧器呢?在老师的指导下,同学们开展了下列活动。
【界定任务】
小英同学认为,首先了解制作简易供氧器的供氧原理再确定制取装置。同学们一致认为制作简易供氧器还需要考虑物质变化、能量变化、反应速率、制得氧气的纯度、制氧剂的用量和配比等。根据反应物的状态和反应条件确定发生装置,根据氧气的密度和溶解性等确定收集装置。
【建构模型】
老师提供了以下实验装置,同学们选择装置用过氧化氢分解和加热高锰酸钾的方法获得氧气。
化学是一门以实验为基础的科学。根据下列装置回答问题。

(1)写出①的仪器名称。
(2)写出用装置B制取氧气的化学方程式。
(3)用氯酸钾粉末在二氧化锰做催化剂并加热的条件下,分解生成氯化钾和氧气,可选用的装置组合是(从A-E中选择)
(4)若用F装置收集氧气应从口进入(填a或b)。
【模仿改造】

化学制氧机(原理图见图1)利用过碳酸钠白色固体、二氧化锰黑色粉末产生氧气。过碳酸钠加水溶解会分解生成碳酸钠和过氧化氢。用该制氧机制氧时,在反应仓中加入适量水,再先后加入过碳酸钠和二氧化锰,反应仓内有黑色粉末翻腾,变得浑浊,仓壁变得温热,过滤仓底部导气管口有气泡冒出。
(5)加湿过滤仓不仅可以过滤杂质,还利用氧气溶于水的性质,使氧气变得湿润;而且根据来判断产生氧气的速率。
(6)验证加湿过滤仓导出的气体是氧气的方法:。
【评价反思】
展示环节,小英同学所在小组制作的简易供氧器(如图2)得到了大家的好评,并提出如下修改意见:在导管出口处加装一个带有调气阀的鼻氧管,以提高适用性。
-
14、如图是初中化学常见的探究实验。请回答下列问题:


在“质量守恒定律”的课堂教学中:探究当物质发生化学反应生成新物质时,参加反应的物质的质量总和与生成物的质量总和有什么关系?
甲、乙、丙、丁、戊四个小组的同学分别做了A、B、C、D、E五个实验。他们都进行了规范的操作,准确的称量和细致的观察。
(1)、E实验:该实验的现象为 , 在实验过程中气球的作用是。(2)、乙、丁两组同学得到的结论是:化学反应前后总质量不守恒。老师引导学生分析了B、D两个实验。你认为B实验天平不平衡的原因是。实验D中镁条燃烧的反应方程式是。(3)、通过上述实验,得到的启示是:有气体参加或生成的反应,在验证质量守恒定律时应该在装置中进行实验。 -
15、实验是进行科学探究的重要手段。请根据图示信息完成下列问题:
 (1)、B是简易家用净水器,加入活性炭是利用其性除去水中的颜色和异味。(2)、实验C结束后,打开止水夹,发现进入集气瓶中水的体积小于集气瓶内空气体积的五分之一,可能的原因是(填一条原因即可)。(3)、实验D是电解水的实验,a管链接电源的极,发生反应的化学方程式是。
(1)、B是简易家用净水器,加入活性炭是利用其性除去水中的颜色和异味。(2)、实验C结束后,打开止水夹,发现进入集气瓶中水的体积小于集气瓶内空气体积的五分之一,可能的原因是(填一条原因即可)。(3)、实验D是电解水的实验,a管链接电源的极,发生反应的化学方程式是。 -
16、我国科学家成功合成新型催化剂,能将高效转化为甲醇。这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如图所示。
 (1)、据上图所示,说明在化学反应中,可分而不可分。(2)、甲、乙、丙、丁四种物质中,属于氧化物的有(填化学式)。(3)、写出该反应的化学方程式。(4)、火炬燃料火炬“祥云”的燃料是丙烷 , 火炬“飞扬”的燃料是氢气。写出丙烷充分燃烧生成二氧化碳和水的化学方程式。
(1)、据上图所示,说明在化学反应中,可分而不可分。(2)、甲、乙、丙、丁四种物质中,属于氧化物的有(填化学式)。(3)、写出该反应的化学方程式。(4)、火炬燃料火炬“祥云”的燃料是丙烷 , 火炬“飞扬”的燃料是氢气。写出丙烷充分燃烧生成二氧化碳和水的化学方程式。 -
17、如图是铈元素在元素周期表中的信息以及A、B、C、D四种粒子的结构示意图,请根据图示回答。
 (1)、铈元素的相对原子质量是。(2)、B、C属于不同种元素的原因是。(3)、A、B、C、D四种粒子中具有相对稳定结构的是(填字母),C在化学变化中形成的离子符号为。
(1)、铈元素的相对原子质量是。(2)、B、C属于不同种元素的原因是。(3)、A、B、C、D四种粒子中具有相对稳定结构的是(填字母),C在化学变化中形成的离子符号为。 -
18、化学与生活、生产、科技密切相关。请根据所学化学知识回答下列问题:(1)、劳动节期间,“筑梦”小组进行了“豆腐中的化学”主题研学活动。
制豆腐:小组同学经过“选豆→浸泡→磨浆→过筛→点浆→压制成型”,制得豆腐。“磨浆”属于(填“物理变化”或“化学变化”),“过筛”与实验室中操作的原理相似。
(2)、单晶硅为信息技术和新能源开发提供了基础材料,硅的元素符号为。(3)、是一种常用的复合肥 , 中氮元素的化合价为。(4)、“天宫”核心舱“天和”电推系统中的霍尔推力器腔体采用了氮化硼陶瓷基复合材料。制备氮化硼(BN)的反应如下:则X的化学式为。(5)、氯化钠是由和直接构成的化合物(填化学符号)。 -
19、下列所示的四个图像能够正确反映对应关系的是A、
 红磷燃烧测定氧气含量时的气压变化
B、
红磷燃烧测定氧气含量时的气压变化
B、 加热一定质量的高锰酸钾
C、
加热一定质量的高锰酸钾
C、 加热一定质量高锰酸钾
D、
加热一定质量高锰酸钾
D、 向一定质量双氧水的水溶液中加入二氧化锰
向一定质量双氧水的水溶液中加入二氧化锰
-
20、下列关于化合价的说法正确的是( )A、在Na2O中,钠原子显+1价,氧原子显-2价 B、在O2中,氧元素显-2价 C、非金属元素在化合物中总显负价 D、一种元素在同一种化合物中,可能有几种化合价