-
1、铜是重要的金属资源,它对于改善人类生活、促进人类文明起着重要作用。(1)、铜的认识:生活中常用铜作导线,体现了铜的延展性和性。(2)、铜的冶炼:黄铜矿的主要成分是 , 根据其主要成分的组成元素,推断用黄铜矿炼铜过程中产生形成酸雨的空气污染物是(填化学式)。(3)、铜的锈蚀:铜在潮湿的空气中锈蚀的反应为 , X的化学式为。
-
2、认真阅读下列材料,回答有关问题。
在全球半导体产业的激烈竞争中,中国的芯片技术正逐渐崭露头角。华为发布的新款手机Mate 70 pro中搭载的麒麟9020芯片已经有了向世界展示中国芯片的实力和潜力。
芯片的主要材料由高纯度单晶硅制作,晶态硅具有金刚石晶格,硬而脆,熔点1410℃,沸点 2355℃。自然界中硅常以二氧化硅和硅酸盐的形式存在。
(1)、二氧化硅中硅元素的化合价为:。(2)、自然界中硅常以(填“单质”或“化合物”)的形式存在。(3)、晶态硅具有物理性质有。(任写一条) -
3、物质的鉴别和除杂是重要的实验技能。下列各组物质所用方法选择正确的是
选项
实验目的
实验方法
A
除去 CaO 中的
高温煅烧
B
除去二氧化碳中的一氧化碳
点燃
C
鉴别氯化钠与氢氧化钠固体
取样,加水溶解,测试溶液温度
D
鉴别和
分别点燃,在火焰上方罩一个干燥的烧杯
A、A B、B C、C D、D -
4、中国芯片蚀刻技术国际领先。NF3进行硅芯片蚀刻时的产物均为气体,在蚀刻物表面不留任何残留物。该反应微观示意图如图,下列说法正确的是
 A、结构观:物质丁由2个原子构成 B、守恒观:反应前后原子数目没有增减 C、丁在空气中的质量分数为78% D、定量观:反应中甲和乙的微粒个数比为4:3
A、结构观:物质丁由2个原子构成 B、守恒观:反应前后原子数目没有增减 C、丁在空气中的质量分数为78% D、定量观:反应中甲和乙的微粒个数比为4:3 -
5、高铁酸钾()是一种具有紫色光泽的微细结晶粉末,其氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌、灭藻为一体的新型高效多功能水处理剂。干燥的高铁酸钾在 198℃以下是稳定的,受热易分解为金属氧化物和氧气。下列说法正确的是A、高铁酸钾是一种氧化物 B、高铁酸钾中 K、O 元素质量比为 1:2 C、高铁酸钾中铁元素的质量分数最大 D、保存高铁酸钾时应注意防潮避热
-
6、水是生命之源,如图为H2O的转化和利用。下列说法不正确的是
 A、转化①中水分子间的空隙变大 B、转化②中产生、的体积比为 2:1 C、转化③为置换反应 D、转化④是低碳行动中的重要措施
A、转化①中水分子间的空隙变大 B、转化②中产生、的体积比为 2:1 C、转化③为置换反应 D、转化④是低碳行动中的重要措施 -
7、把少量下列物质分别加入足量水中,充分搅拌,能得到溶液的是A、泥沙 B、蔗糖 C、面粉 D、橄榄油
-
8、在“天宫课堂”第四课“球形蜡烛火焰”科学探究中,航天员用盖子盖在蜡烛火焰上使其熄灭,下列灭火原理与其相同的是A、釜底抽薪 B、用沙土盖灭篝火 C、高压水枪灭火 D、森林起火,砍出隔离带
-
9、中科院研究人员成功合成了一种类似金刚石结构的物质—“T-碳”(化学式为 C)。有关“T-碳”的说法错误的是A、完全燃烧的产物是二氧化碳 B、常温下化学性质稳定 C、由原子直接构成 D、物理性质与石墨相似
-
10、月球堪称“能源矿山”,我国科学家发现月壤中富含丰富的氦(He-3),仅100吨就够全球使用一年,未来有望彻底解决能源危机。氦(He-3)中原子核中质子数为2、中子数为1,下列关于氦(He-3)原子说法正确的是A、原子核外电子数为3 B、氦原子由质子、电子构成 C、地球上、空气中也存在少量氦气 D、氦的相对原子质量为3g
-
11、国家速滑馆又称“冰丝带”,是北京冬奥会最具科技含量的场馆。它的建设采用当前冬季运动场馆最环保的制冰技术二氧化碳跨临界直冷制并技术,通过压力变化是液态二氧化碳汽化实现制冷,下列关于制冷过程的说法中正确的是A、二氧化碳分子的构成没有发生变化 B、二氧化碳分子的大小发生了变化 C、二氧化碳分子的质量发生了变化 D、二氧化碳分子不再运动
-
12、规范的实验操作是完成实验的基本保证。如图所示实验操作正确的是A、倾倒液体
 B、放置收集满的氧气
B、放置收集满的氧气 C、点燃酒精灯
C、点燃酒精灯 D、检验CO2是否收集满
D、检验CO2是否收集满
-
13、我国航空航天事业取得令人瞩目的成就,阅读以下相关主题科普材料,回答问题。
材料一:神舟十三号载3名宇航员在太空执行任务,时长180天,空间站中常用水气整合系统实现的清除和的再生(简易流程如下图),科学家通过缜密计算,为了提供3名宇航员在太空生活所需的 , 至少需从地球带的水进行电解。

材料二:我国探月工程实现“六战六捷”。未来还将探索在月球建设基地的可能,其中一个前提就是在月球上大规模制造 , 在月球上可以电解熔融月壤(含等)制造氧气。
(1)、分析材料一流程可知,可循环利用的化合物有(填物质的化学式),航天员呼吸属于缓慢过程。(2)、请计算电解486kg水能产生氧气的质量(填写具体计算过程)。 -
14、
小圳同学发现,金店里有两种不同的“白金”,单价相差悬殊,小圳同学很好奇,打算对这两种不同的“白金”进行研究。
任务一:鉴别两种“白金”
【查阅资料】
I,市场上所谓的“白金”通常有两种:一种是铜、锌、金、镍(元素符号i)的合金,称为白色金;另一种是铂金,铂是一种银白色的贵重金属,化学性质稳定不与氧气反应,用于制作耐腐蚀的化学仪器及首饰等,俗称白金,元素符号。
部分实验试剂:大小、形状相同的足量的稀盐酸
Ⅱ.都可溶于水
【探究活动一】萱萱结合学习的金属的性质,想知道家中首饰的“白金”是白色金还是铂金,她和兴趣小组的同学一起展开探究活动。
(1)设计实验一:将这两种“白金”样品分别放在陶土网上用酒精灯加热,观察到金属表面________,则这种“白金”样品为白色金。
(2)设计实验二:将这两种“白金”样品放入________中,观察到金属表面冒气泡,则这种“白金”样品为白色金。
(3)设计实验三:将这两种“白金”样品放入硝酸银溶液中,观察到金属表面有银白色物质附着,则这种“白金”样品为白色金。写出其中一个反应的化学方程式________。
任务二:探究的金属活动性顺序
【提出问题】萱萱同学提出:种金属的活动性顺序是怎样的呢?
【作出假设】根据金属活动性顺序,已知活动性
(4)假设①;假设②;假设③________。
【探究活动二】
(5)设计实验,通过三种金属与酸反应的不同现象来探究三种金属的活动性顺序,写出实验步骤________。
【实验观察】
加入金属
反应的现象
金属表面有气泡冒出
金属表面有气泡冒出
无明显现象
【得出结论】
(6)原假设中错误的是________(填序号)。
【反思交流】
(7)上述【探究活动二】没有得出三种金属的活动性顺序,兴趣小组同学需改变思路重新设计实验以达到探究实验的目的。同学们讨论用下列各组试剂来验证的金属活动性顺序。其中一定能达到实验目的的是___________(填字母)。
A. 溶液 B. 溶液、溶液 【归纳总结】通过上述探究过程,我们能够总结出探究金属活动性顺序时应采用适当的探究实验方案,在设计实验方案时,需要考虑选择合适的药才能使探究活动顺利完成。
【拓展应用】
(8)金属材料在生活中应用广泛,同时大量产品更新,会产生很多废弃金属产品。“绿箱子环保计划——废弃手机及配件回收联合行动”已在全国40个重点城市中开展多年。下列有关说法不正确的是___________。
A. 回收废电池可以节约金属资源
B. “绿箱子”上的“ ” 是回收标志
” 是回收标志
C. 回收废电池可以减少环境污染
D. 回收废弃手机中的金属材料没有任何价值 -
15、铂是炼油、石化、汽车工业的常用催化剂。我国铂资源极度匮乏,从二次资源中回收铂的来源之一是工业废催化剂。某废催化剂中含碳、硫、铂、氧化铝等物质,下图是回收铂的工艺流程。

资料:氧化铝和稀硫酸反应的化学方程式为:工业生产中,一般用石灰乳来吸收产生的二氧化硫气体
(1)、焙烧前先将废催化剂粉碎,理由是 , 焙烧的主要目的是。(2)、酸浸中加入过量硫酸的目的是:。(3)、溶液I中溶质的成分为(写化学式)。(4)、金属A为 , 写出金属A与溶液I反应的化学方程式:。(5)、溶液II得到副产物硫酸铝晶体的步骤为:蒸发浓缩,。(6)、该流程存在的不足之处是在焙烧时可能产生气体污染空气,从而导致酸雨的形成,你的改进方法是。 -
16、
某小组以“探秘温室气体的温室效应”为主题开展项目式学习。
【任务一】实验室制取CO2
(1)为制取CO2 , 需将100g36%的浓盐酸稀释至9%,所加蒸馏水(密度为)的体积为。
(2)仪器A的名称是 , 组装一套可控制反应速率的发生装置,应从图中选择的装置组合是 , 实验室常用石灰石与稀盐酸制取CO2 , 反应的化学方程式为。

【任务二】设计实验验证CO2的温室效应
用太阳作为红外辐射源,把手机和热成像仪固定在三脚架上,对准太阳,让太阳在热成像的画面中心,实验装置示意图如下,热成像测量太阳中心点经装有不同种类气体的玻璃瓶测得阻挡后的辐射量数据如表格所示:
实验编号
气体种类
测得阻挡后的辐射量数据/℃
1
空气
82.6
2
CO2
84.0
3
O2
81.6

(3)根据设计的对照实验,得出的结论是当玻璃瓶里是气体时,长波辐射被削弱了很多,说明该气体(填“是”或“不是”)温室气体。
(4)为了增加实验的严谨性,除了控制气体的湿度要一样外,还需控制的因素可能有(任答2点,合理即可)。
(5)依据图-2装置,设计实验证明水蒸气也是一种温室气体,方案为:其他条件相同时,比较 , 测得阻挡后的辐射量数据。
-
17、科普阅读
《天工开物》中对制造染料“蓝靛”的叙述如下:“凡造淀,叶与茎多者入窖,少者入桶与缸。水浸七日,其汁自来。每水浆一石,下石灰五升,搅冲数十下,淀信即结。水性定时,淀沉于底…其掠出浮沫晒干者曰靛花。这里的靛花无法直接染色,先转为可溶性靛白,进入纺织品的纤维,透风后被氧化成靛蓝。
(1)、“水浸七日,其汁自来”“晒干者曰靛花”,相当于实验操作中的、。(2)、“每水浆一石下石灰五升”,该过程生成的氢氧化钙能中和“水浸七日”时发酵生成的酸液发生反应,使酸液酸性减弱,其(填“增大”或“减小”);在测酸液时,小深同学不小心润湿了试纸,其测出来的结果(填“偏大”或“偏小”);(3)、氢氧化钙还能与发酵过程产生的二氧化碳反应,化学方程式为加快沉降速度。(4)、透风的目的是与空气中的接触,使靛白变成靛蓝。(5)、实验时,小深同学对酸液中存在什么粒子使酸碱指示剂变色产生了浓厚的兴趣,稀盐酸中含有哪些微观粒子。 -
18、春晚《满庭芳·国色》节目点燃了国人复古寻色的热潮,其中桃红、凝脂、缃叶、群青、沉香代表红、白、黄、青、黑传统五色。(1)、群青:是一种品贵的高级颜料,古代是用贵重的青金石中研磨制成的。青金石中含、O等元素,从原子结构的角度说明,这些元素最根本的区别是不同。(2)、桃红:用银朱调合,可以得到灿若桃花的颜色。银朱是用硫与汞加热制成的硫化汞,反应前后不变的微粒是(填化学符号)。(3)、凝脂:降低原料中含铁氧化物含量,实现从青瓷到凝脂似玉的白瓷。如图为铁元素的价类二维图,a点表示物质的类别是 , c点的化学式是。
 (4)、缃叶:取色自雌黄(),颜色类似硫磺,在空气中燃烧能产生剧毒的和一种刺激性气味的气体,该反应的化学方程式为。(5)、沉香:代表黑色,以下固体可能为沉香主要成分的是___________(填字母)。A、氧化镁 B、氧化铜 C、五氧化二磷 D、氧化铁(6)、孔雀石主要成分为 , 受热分解生成三种氧化物,其反应的化学方程式为。
(4)、缃叶:取色自雌黄(),颜色类似硫磺,在空气中燃烧能产生剧毒的和一种刺激性气味的气体,该反应的化学方程式为。(5)、沉香:代表黑色,以下固体可能为沉香主要成分的是___________(填字母)。A、氧化镁 B、氧化铜 C、五氧化二磷 D、氧化铁(6)、孔雀石主要成分为 , 受热分解生成三种氧化物,其反应的化学方程式为。 -
19、下列实验方案不能达到实验目的的是
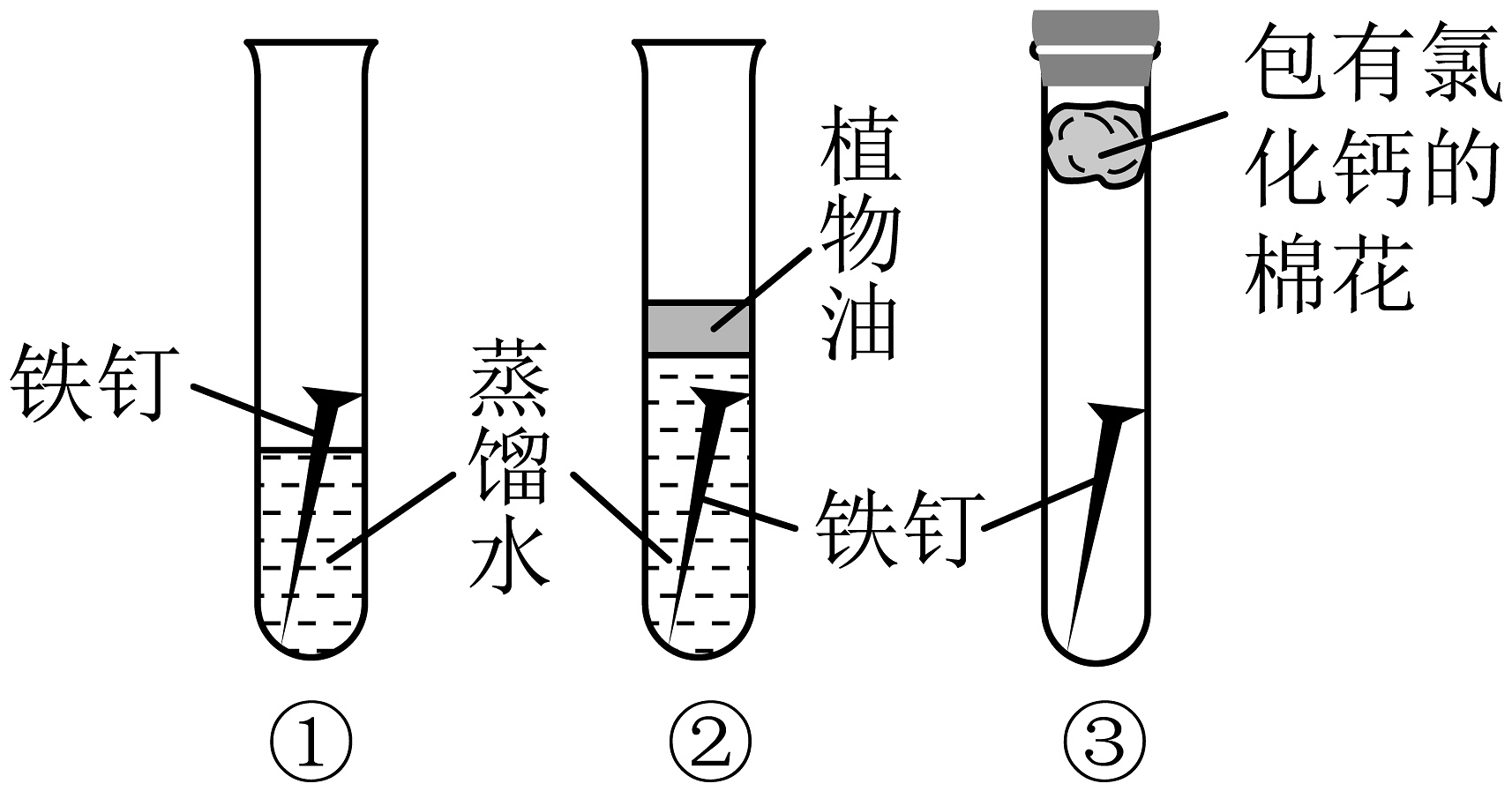



A.探究铁锈蚀的条件
B.探究石蜡中含有碳元素
C.测定空气中的含量
D.探究燃烧的条件
A、A B、B C、C D、D -
20、要使如图装置中的小气球鼓起来,则使用的固体和液体可以是

①石灰石和稀盐酸;②镁和稀盐酸;③氢氧化钠和水;④硝酸铵和水
A、①②③④ B、①②③ C、①②④ D、②③④