-
1、正确的化学实验操作是实验成功和人身安全的重要保证。下列实验操作错误的是A、给烧杯中的液体加热,需要垫上陶土网 B、实验室中没有腐蚀性的药品也不可以品尝 C、取用药品要控制用量,若没有说明用量,固体铺满试管底部即可 D、用滴管吸取液体时,伸入试剂中捏扁橡胶胶帽赶尽气体后再吸液
-
2、“科学思维”是化学学科的核心素养之一、下列解释错误的是A、闻到花香——分子在不断的运动 B、氧气和液氧都能支持燃烧——同种分子化学性质相同 C、食物变质——食物分子的间隔、大小发生变化 D、用水银温度计测量体温——温度升高,原子间隔变大
-
3、规范操作是实验成功和安全的保障。下列实验操作规范的是A、塞紧橡皮塞
 B、加热液体
B、加热液体 C、液体的倾倒
C、液体的倾倒 D、装入粉末药品
D、装入粉末药品
-
4、化学课上老师向硫酸铜溶液中加入氢氧化钠溶液,发现有蓝色沉淀生成,于是有同学思考“加入其它溶液也能有蓝色沉淀生成吗?”这属于科学探究中的A、设计实验 B、提出问题 C、交流反思 D、得出结论
-
5、人类利用化学科学知识在一个“纯天然”的地球上搭建起一个五彩缤纷、美轮美奂的人造世界。下列物质中,不属于用化学方法人工制造的是A、
 金属材料
B、
金属材料
B、 玻璃制品
C、
玻璃制品
C、 塑料制品
D、
塑料制品
D、 棉花纤维
棉花纤维
-
6、
《天工开物》记载古法造纸术的流程是原料浸泡、蒸煮、抄制、烘干。“创新”小组根据记载,利用回收的废纸进行“制造再生纸”跨学科实践活动,在蒸煮时加入了氢氧化钠。造纸后,为处理剩余的废液进行如下探究活动。
【查阅资料】
①BaCl2溶液呈中性;
②碱石灰是氢氧化钠与氧化钙的固体混合物。
【任务一】废液成分分析
【提出猜想】推测废液中含有氢氧化钠和碳酸钠中的一种或两种
【实验设计与实施】
【任务二】废液中碳酸钠含量测定
实验操作
实验现象
实验结论
步骤1:取少量废液于试管中,加入足量的氯化钡稀溶液。
①_______
废液中有Na2CO3
步骤2:取少量步骤1中的上层清液于试管中,滴加②_______
③_______
废液中有NaOH
(1)填写表中的空白①、②、③。
“创新”小组设计了如图所示的实验,取100g废液样品放入装置A的锥形瓶中,先通入一会儿N2 , 然后称量装置C、D的质量,再向锥形瓶中滴加足量稀硫酸,至不再产生气体,继续通一会儿N2后,测得装置C、D共增重2.2g。

(2)锥形瓶中不再产生气体后,需要继续通一会儿N2 , 其原因是。
(3)装置E的作用是。
(4)废液中碳酸钠的溶质质量分数是(写出计算过程,结果保留到0.1%)。
(5)装置B的作用是 , 如果缺少装置B,会使测定的碳酸钠含量(填“偏大”或“偏小”)。
【任务三】废液的处理
(6)为使废液中的碳酸钠转化为氢氧化钠循环利用,需根据废液中碳酸钠的含量,加入一定量的某种物质,该物质与碳酸钠反应的化学方程式是。
-
7、
“扬帆”小组对一瓶久置的NaOH固体的变质情况进行了实验探究。
【提出问题】NaOH变质了吗?
【作出猜想】①没有变质②已经变质
(1)请用化学方程式表示NaOH能变质的原因。
任务一:定性探究该NaOH固体是否变质
【实验活动1】
(2)设计方案进行如表实验:
实验方案
实验现象
实验结论
取少量该NaOH固体样品完全溶于水,加入过量稀盐酸
猜想②成立,依据是(用化学方程式表示)
【反思评价】有的同学提出此实验无法确定该NaOH固体变质程度。
任务二:定量探究该NaOH固体变质程度
【实验活动2】
(3)兴趣小组利用控制变量的方法进行实验,实验数据如表所示。
实验装置
实验序号
分别向左右容器内加入下列物质
温度升高值/℃
溶液pH

1
1.0gNaOH固体。
31.52
13.69
2
agNa2CO3固体。a的数值为。
10.03
11.92
3
1.0g该NaOH固体样品。
15.71
m
【实验结论】
(4)小组同学分析温度升高值数据,确定该NaOH固体变质程度是 , 请推测m的取值范围是。
【反思评价】兴趣小组充分认识到定量研究在化学实验中的重要作用。
【拓展延伸】
(5)生活中的管道疏通剂和炉具清洁剂成分中都含有NaOH,包装标签上应注明的注意事项是(写一条)。
-
8、铁黄(FeOOH)是一种颜料,以某硫铁矿废渣(主要成分 , 含有少量的 , 其余成分不考虑)为原料,制取铁黄,以下是制取工艺流程。
注:铁黄不与水反应,不与水和反应
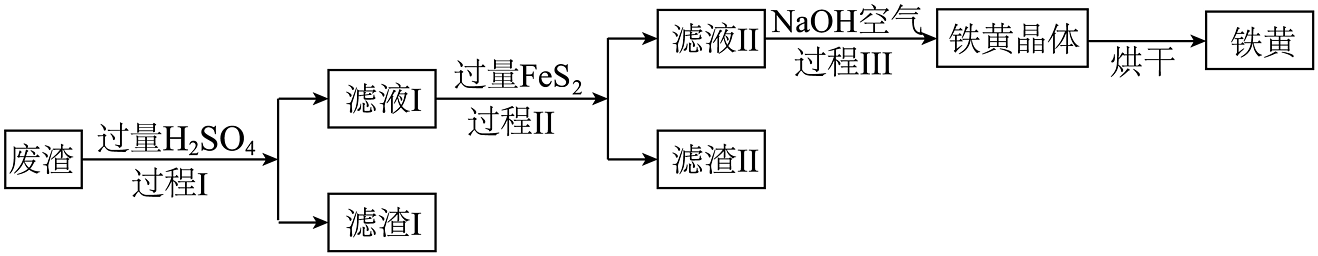 (1)、过程Ⅰ的化学方程式为 , 滤渣Ⅰ中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、过程Ⅲ中的化学方程式为 , 该反应属于反应(填基本反应类型);(4)、①FeOOH随着温度的升高,可以加热分解成 , 写出其反应的化学方程式;
(1)、过程Ⅰ的化学方程式为 , 滤渣Ⅰ中的物质有(填化学式);(2)、过程Ⅱ的操作名称为;(3)、过程Ⅲ中的化学方程式为 , 该反应属于反应(填基本反应类型);(4)、①FeOOH随着温度的升高,可以加热分解成 , 写出其反应的化学方程式;②温度不同时,生成的颜色如下表:
温度/℃
400
700
750
800
颜色
橘红
鲜红
鲜红
暗红
如果思考乐希希同学想获得鲜红的 , 应把温度控制在。
-
9、“宏观-微观-符号”是化学独特的表示物质及其变化的方法。某兴趣小组对盐酸和硫酸的共性和差异性进行以下研究。回答下列问题。(1)、向稀盐酸和稀硫酸中分别滴加石蕊试液,试液变红,说明两种酸溶液中均存在(填微粒符号)。(2)、将表面生锈的铁钉投入到足量稀硫酸中,铁锈逐渐溶解,溶液变黄,铁钉表面产生气泡,该气体为;一段时间后,溶液慢慢变为黄绿色,图1是对溶液变为黄绿色的一种微观解释,参加反应的微粒是(填微粒符号)。
 (3)、分别向两份相同的Ba(OH)2溶液中匀速滴加相同pH的稀盐酸和稀硫酸,观察现象并绘制溶液电导率随时间变化曲线(图2)(电导率能衡量溶液导电能力大小,相同条件下,单位体积溶液中的离子总数越多,电导率越大)。
(3)、分别向两份相同的Ba(OH)2溶液中匀速滴加相同pH的稀盐酸和稀硫酸,观察现象并绘制溶液电导率随时间变化曲线(图2)(电导率能衡量溶液导电能力大小,相同条件下,单位体积溶液中的离子总数越多,电导率越大)。
①图2中曲线1表示向Ba(OH)2溶液中滴加;曲线2反应中的实验现象为。
②该实验说明,不同的酸中,由于不同,酸的性质也表现出差异。
-
10、某兴趣小组借助数字技术探究“稀盐酸与氢氧化钠溶液反应”,图1所示是室温下稀盐酸与稀氢氧化钠溶液反应的实验装置,图2是反应过程中的pH变化曲线。
 (1)、根据图2曲线判断,图1中的溶液B是(填“氢氧化钠”或“盐酸”)。(2)、图2中a点所示的溶液pH7(填“>”“<”或“=”),溶液呈现(填“酸性”“碱性”或“中性”)。(3)、c点所示的溶液中含有的溶质是(填化学式)。(4)、a点到b点pH变化的微观本质是。(5)、该过程发生反应的化学方程式为。
(1)、根据图2曲线判断,图1中的溶液B是(填“氢氧化钠”或“盐酸”)。(2)、图2中a点所示的溶液pH7(填“>”“<”或“=”),溶液呈现(填“酸性”“碱性”或“中性”)。(3)、c点所示的溶液中含有的溶质是(填化学式)。(4)、a点到b点pH变化的微观本质是。(5)、该过程发生反应的化学方程式为。 -
11、化学是推动科技进步和现代社会文明的重要力量,与生活、生产和科技发展息息相关,请回答下列问题。(1)、生活中的化学
①打扫卫生清洗各种器具,可用厨房中的清洗水垢(水垢的主要成分是碳酸钙和氢氧化镁)。
②在治疗胃酸过多症的药物成分中,含有的物质不可以是(填字母)。
A.氢氧化铝 B.碳酸钠 C.氢氧化钠 D.碳酸氢钠
③我国是最早利用天然气的国家。目前天然气作为清洁能源已走入千家万户。天然气的主要成分是甲烷(CH4),写出甲烷在空气中充分燃烧的化学方程式。
(2)、生产中的化学古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰。
①“煤饼烧石成灰”的过程中,能量转化形式是热能转化为能。
②“石”转化为“灰”的反应属于(填基本反应类型)。
③“灰”遇水成浆,该反应的化学方程式为。
-
12、分离提纯是获取物质的重要方法,其思路有两种:一是除去杂质,二是提取目标产物。如图是海水综合利用的部分流程(操作已省略),下列说法不正确的是
已知:该粗盐中含泥沙、MgCl2、CaCl2、Na2SO4等杂质。
 A、流程I中X、Y溶液的顺序不能颠倒 B、流程Ⅱ中的石灰乳不能用烧碱替代 C、流程Ⅱ中提纯氯化镁是通过“提取目标产物”的思路实现的 D、混合物分离提纯的方法是由混合物中各成分的性质差异决定的
A、流程I中X、Y溶液的顺序不能颠倒 B、流程Ⅱ中的石灰乳不能用烧碱替代 C、流程Ⅱ中提纯氯化镁是通过“提取目标产物”的思路实现的 D、混合物分离提纯的方法是由混合物中各成分的性质差异决定的 -
13、利用酸性氯化铜蚀刻废液(含有和)制备碱式碳酸铜的部分工艺流程如图。已知碱式碳酸铜的分解温度为220℃,下列说法错误的是
 A、向蚀刻废液中加入碳酸钠固体反应时,溶液保持不变 B、洗涤固体是为了去除固体表面的杂质氯化钠 C、干燥固体时,在一定范围内温度越高越好,但温度应低于220℃ D、该工艺流程可减少水污染
A、向蚀刻废液中加入碳酸钠固体反应时,溶液保持不变 B、洗涤固体是为了去除固体表面的杂质氯化钠 C、干燥固体时,在一定范围内温度越高越好,但温度应低于220℃ D、该工艺流程可减少水污染 -
14、设计实验方案是科学探究的要素,下列实验方案能达到实验目的的是
选项
实验目的
实验方案
A
除去铁粉中的碳粉
加足量稀盐酸,过滤
B
除去CO中少量的CO2
将混合气体通过足量的氢氧化钠溶液
C
除去氢氧化钠溶液中的碳酸钠
加过量澄清石灰水,过滤
D
鉴别氯化钙溶液和氢氧化钙溶液
分别滴入几滴无色酚酞试液
A、A B、B C、C D、D -
15、某兴趣小组用化学方法制作蛋雕:将蛋壳(蛋壳主要成分CaCO3),在熔化的石蜡中裹上蜡衣,用金属丝划穿蜡衣雕“花”,吸取适量10%的稀盐酸滴在划痕处,一段时间后,放入热水中熔去多余的蜡,做成蛋雕作品,如图所示。关于蛋雕制作的说法正确的是
 A、碳酸钙高温不分解 B、石蜡能与盐酸发生化学反应 C、盐酸有腐蚀性,要做好防护 D、盐酸滴到蛋壳上有氢气生成
A、碳酸钙高温不分解 B、石蜡能与盐酸发生化学反应 C、盐酸有腐蚀性,要做好防护 D、盐酸滴到蛋壳上有氢气生成 -
16、我国化学家侯德榜发明了侯氏制碱法,其部分工艺流程如图。下列说法正确的是
 A、“操作1”为蒸发结晶 B、步骤②中发生分解反应 C、生产中先通入CO2后通NH3 D、“母液”中的溶质只有NH4Cl,可直接用作氮肥
A、“操作1”为蒸发结晶 B、步骤②中发生分解反应 C、生产中先通入CO2后通NH3 D、“母液”中的溶质只有NH4Cl,可直接用作氮肥 -
17、分析推理是化学学习中常用的思维方法。下列分析推理正确的是A、中和反应有盐和水生成,则生成盐和水的反应一定是中和反应 B、由金属阳离子和酸根阴离子构成的化合物属于盐,则盐中一定有金属元素 C、常温下,pH等于7的水溶液呈中性,则显中性的水溶液pH一定等于7 D、活泼金属与盐酸反应有气泡产生,则与盐酸反应有气泡产生的物质一定是活泼金属
-
18、化学源于生活、服务于生活。下列做法中涉及的化学原理不正确的是
选项
做法
化学原理
A
用碳酸镁治疗胃酸过多
碳酸镁能与胃酸发生中和反应
B
用汽油去除衣服上的油渍
汽油能溶解油渍
C
盐酸用于金属表面除锈
盐酸能与某些金属氧化物反应
D
用小苏打烘焙糕点液
NaHCO3受热易分解产生气体
A、A B、B C、C D、D -
19、化学课中老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是A、食醋 B、氯化钠溶液 C、碳酸钠溶液 D、稀盐酸
-
20、下列常见物质的用途,不是利用其化学性质的是A、食醋能除铁锅上的水垢 B、氧化钙可作食品干燥剂 C、铁粉可做食品除氧剂 D、干冰易升华做制冷剂