-
1、I、新能源车因污染小而被大力推广,请你参加社会性议题“汽车能源的变迁”的项目式学习。(1)、传统汽车能源主要来自石油,从物质类别的角度来看,石油属于(选填“纯净物”或“混合物”)。(2)、天然气和乙醇可替代传统汽车能源。乙醇充分燃烧的化学方程式为:。(3)、电池可给新能源汽车提供动力。
①电动汽车的电池放电时,其能量转化为能转化为电能。
②新能源汽车常使用含磷酸亚铁锂(LiFePO4)的锂电池为汽车提供动力。LiFePO4中Li的化合价为。某种锂原子的质量为1.165×10-26kg,碳12原子质量的为1.66×10-27kg,则该锂原子的相对原子质量是(计算结果精 确到0.1)。
③磷酸亚铁锂可用磷酸铁、氢氧化锂和草酸为原料合成,请完成下列化学方程式:2FePO4+6H2C2O4+ 2LiOH=2LiFePO4+ 7CO2↑+5CO↑+7。
(4)、II、同学们利用如图1所示的装置探究水的组成。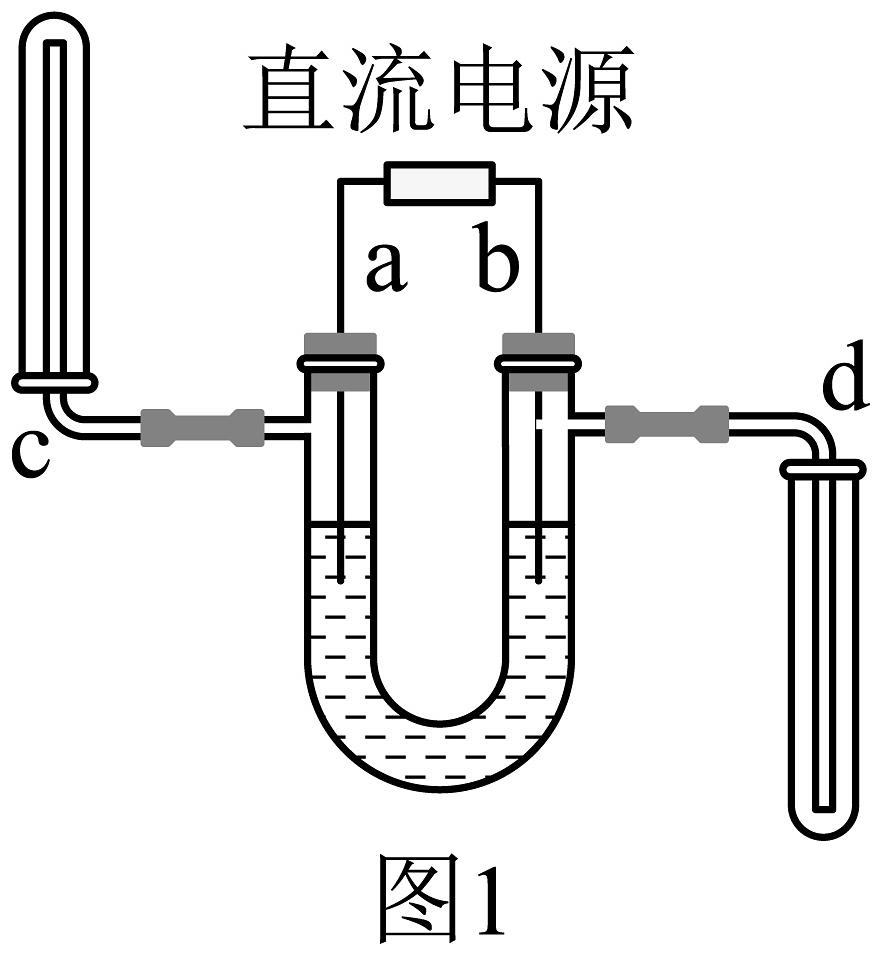
①电源正极为(选填“a” 或“b”)端,电解水发生反应的化学方程式为:。
②c、d管中收集到的气体的质量比为
(5)、在不同温度下,向盛有50g水的烧杯中缓慢加入硫酸铜固体,测得溶液质量与加入硫酸铜质量的变化关系如图2所示。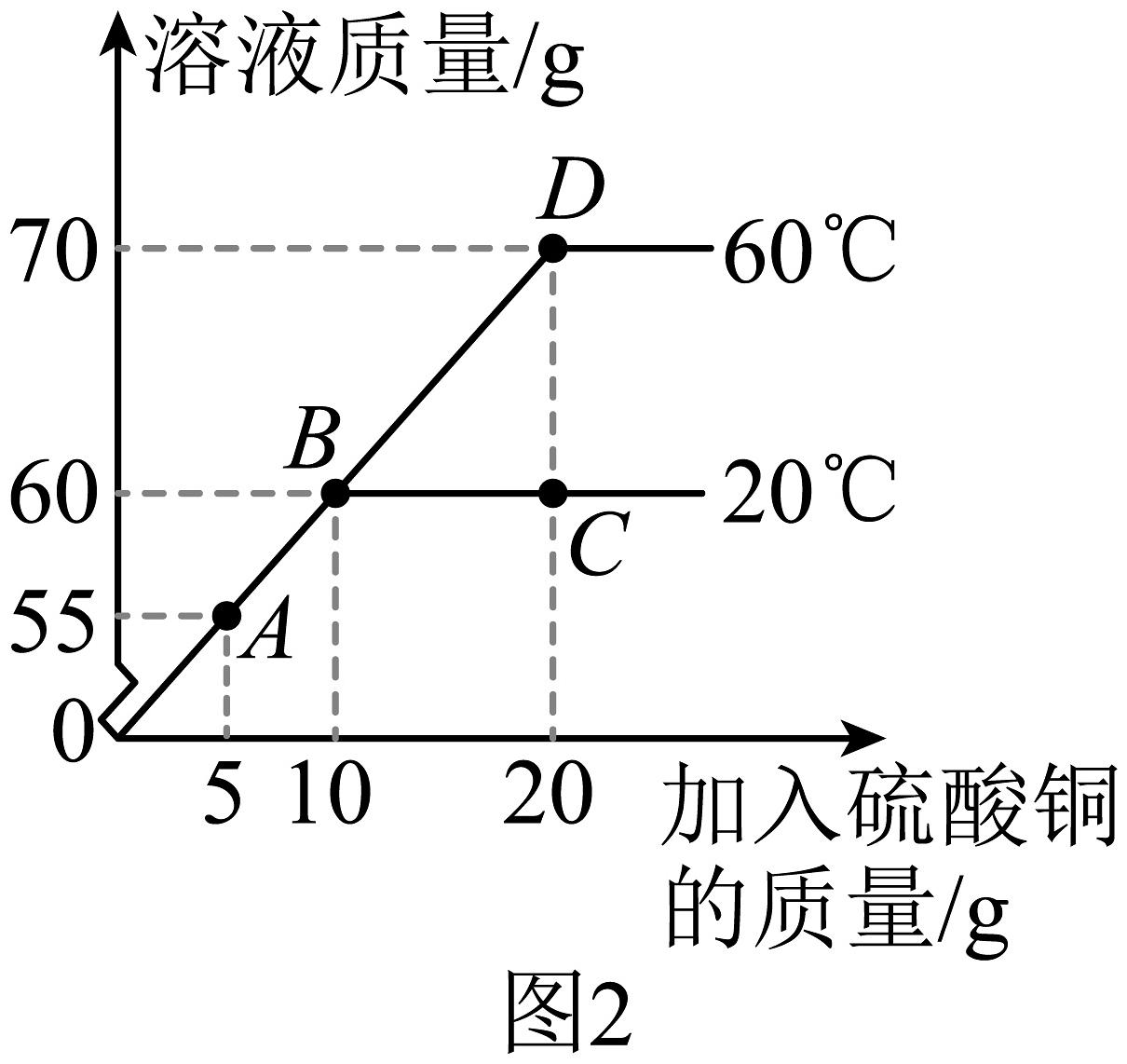
①20℃时硫酸铜的溶解度为
②20℃时,A、B、C三点对应的溶液中属于饱和溶液的是
③C、D两点对应溶液中溶质质量分数的大小关系为。
-
2、工业上可利用黄铁矿(主要成分是Fe2S)煅烧的产物冶炼铁和生产硫酸,其反应方程如下:
①
②
③
④
下列说法不正确的是
A、反应①②③均有元素化合价发生变化 B、反应①②不属于四种基本反应类型中的任何一种,反应③④属于化合反应 C、将5g SO2溶于95g水形成溶液,其溶液的质量分数大于5% D、将100g蒸馏水加入100g 98%的浓硫酸中,可配制200g质量分数为49%的稀硫酸 -
3、同学们设计的下列实验方案(夹持装置已略去),能达到实验目的的是
选项
A
B
C
D
实验目的
探究空气中氧气的含量和铁生锈的条件
比较合金与其成分金属的硬度
验证质量守恒定律
探究CO2与水反应
实验方案



 A、A B、B C、C D、D
A、A B、B C、C D、D -
4、我国研发出一项将甲烷(CH4)转化成乙烷的新技术,涉及的物质种类变化示意图如图所示。下列说法正确的是
 A、该反应的化学方程式为 B、甲烷、乙烷都是最简单的有机化合物 C、该反应中的最小粒子是分子 D、反应前后,催化剂的质量和性质不变
A、该反应的化学方程式为 B、甲烷、乙烷都是最简单的有机化合物 C、该反应中的最小粒子是分子 D、反应前后,催化剂的质量和性质不变 -
5、幸福需要辛勤的劳动来创造。下列劳动项目与涉及的化学知识不相符的是
选项
劳动项目
化学知识
A
冬季向路上的积雪撒盐
盐水使雪的熔点降低
B
用食醋洗去水壶中的水垢
醋可与碳酸钙等发生反应
C
用明矾处理较浑浊的天然水
明矾主要起杀菌消毒的作用
D
用石灰浆粉刷墙壁
石灰浆与CO2反应
A、A B、B C、C D、D -
6、搭载天舟七号货运飞船的长征七号遥八运载火箭在我国文昌航天发射场点火发射。下列火箭发射流程中主要涉及化学变化的是A、关闭舱门 B、燃料注入 C、点火发射 D、瞄准定位
-
7、某同学在试管中加入50.2g过氧化氢溶液(过氧化氢和水的混合物)和1.0g二氧化锰制取氧气,充分反应后称得试管中的剩余物质的质量为49.6g。计算:(1)、最多可制得氧气的质量为g。(2)、50.2g过氧化氢溶液中过氧化氢的质量。
-
8、
蒸汽发蓝可有效防止钢铁制品锈蚀,原理是在高温下铁与水蒸气反应生成一层致密的四氧化三铁保护膜。
(1)铁在空气中锈蚀是铁与共同作用的结果。
(2)蒸汽发蓝还生成一种可燃性气体,该气体可能是。
某兴趣小组对铁与水蒸气反应的产物和影响反应速率的因素进行如下探究。
【查阅资料】①吸水树脂(SAP材料)着火点比棉花高,且吸水性更强。
②四氧化三铁具有磁性,不与硫酸铜溶液反应。
I.验证铁与水蒸气反应的产物
【进行实验】兴趣小组设计如图实验方案,进行实验。

【解释与结论】
(3)点燃两盏酒精灯后,直接用燃着的木条放在导管口处检验产物。该操作可能存在的隐患是(写一点)。与老师探讨后,改用如图实验方案。收集一试管气体后,点燃验证气体成分。

(4)反应后用磁铁将残留固体全部吸出,(填“能”或“不能”)验证生成物是四氧化三铁。
II.探究影响铁与水蒸气反应速率的因素
【进行实验】以材料吸收等量水,控制不同变量,利用上图装置测得收集一试管气体所需的时间,记录如下表:
实验编号
铁粉质量/g
SAP材料与铁粉距离/cm
收集一试管气体所需时间/s
①
0.3
4
42.0
②
0.3
6
33.0
③
0.3
8
41.5
④
0.5
4
42.6
⑤
0.5
6
39.2
⑥
0.5
8
42.1
【解释与结论】
(5)实验①②③的目的是。
【反思与评价】
(6)为证明蒸汽发蓝处理后的钢板防锈效果,往钢板喷洒硫酸铜溶液,若观察到 , 防锈效果良好。
-
9、化学是一门以实验为基础的学科,化学所取得的丰硕成果,与实验的重要作用分不开。结合下列实验装置图回答问题:
 (1)、写出图中有标号的仪器名称:a。(2)、乐乐同学制取一瓶二氧化碳气体,应选择的发生装置为 , 实验室制取二氧化碳气体的化学方程式为。(3)、乐乐同学将制取的二氧化碳气体,按图E进行实验,观察到的现象说明二氧化碳的化学性质是。
(1)、写出图中有标号的仪器名称:a。(2)、乐乐同学制取一瓶二氧化碳气体,应选择的发生装置为 , 实验室制取二氧化碳气体的化学方程式为。(3)、乐乐同学将制取的二氧化碳气体,按图E进行实验,观察到的现象说明二氧化碳的化学性质是。 -
10、新型发光陶瓷是将高科技蓄光材料融入传统陶瓷釉料中,经高温烧制而成。它吸蓄光能后,可在阴暗环境中自行发光,题图为部分生产流程。分析流程,回答问题:
 (1)、研磨胚料的目的是。(2)、若坯料中铁粉没有被除去,则烧制的陶瓷会出现黑点,其原因是(填写化学方程式)。(3)、生产蓄光材料需要在稀有气体环境中进行,利用稀有气体。(4)、在烧制陶瓷的过程中,陶瓷中的受热生成和一种常见的液体,该反应属于反应(填基本反应类型)。
(1)、研磨胚料的目的是。(2)、若坯料中铁粉没有被除去,则烧制的陶瓷会出现黑点,其原因是(填写化学方程式)。(3)、生产蓄光材料需要在稀有气体环境中进行,利用稀有气体。(4)、在烧制陶瓷的过程中,陶瓷中的受热生成和一种常见的液体,该反应属于反应(填基本反应类型)。 -
11、阅读下列材料。
甲醇()作为低碳燃料,在常温常压下为无色液体,具有燃烧高效、排放清洁、可再生等特点,运输及使用相对安全、便捷,是全球公认的新型能源。2023年杭州亚运会首次使用甲醇做火炬燃料,实现了“零碳排放”。甲醇是利用电解水生成的氢气与工业废气捕捉的二氧化碳在一定条件下合成,其原理如图所示。因为甲醇燃烧时生成的二氧化碳与合成甲醇时消耗的二氧化碳达到平衡,所以又被称为“零碳甲醇”。甲醇作为一种能够破解能源安全和“双碳”难题的“超级燃料”,极具开发潜力,是中国能源多样化的“新灯塔”。

依据材料回答下列问题。
(1)、写出甲醇的一条物理性质:。(2)、补全甲醇燃烧的化学方程式:。(3)、参加反应的质量(填“>”或“=”或“<”)生成的甲醇中氢元素质量。 -
12、葡萄酒酿造的工艺流程如图所示。
 (1)、“压榨取汁”类似于实验室中的操作。(2)、发酵是将葡萄汁中的糖分转化成酒精和二氧化碳的过程。通常采用带塞的密闭式不锈钢罐进行发酵,罐内的装液量控制在80%左右。
(1)、“压榨取汁”类似于实验室中的操作。(2)、发酵是将葡萄汁中的糖分转化成酒精和二氧化碳的过程。通常采用带塞的密闭式不锈钢罐进行发酵,罐内的装液量控制在80%左右。①用澄清石灰水检验发酵过程产生的二氧化碳,能观察到的现象为。
②“浸渍发酵”装液时留出一定的空间,目的是(填写字母)。
a.存储气体,缓冲压力
b.提供葡萄酒发酵所需氮气
c.发酵旺盛时避免发酵液的逸出
(3)、用橡木桶陈酿葡萄酒,可以改善葡萄酒的色泽,并带有橡木香气和果香。从微粒的观点解释能闻到香气的主要原因是。 -
13、古人所言:“茶者水之神,水者茶之体”,泡茶之水以山上之水为上佳,以江河之水为次佳,以井口之水为下品。请按要求回答下列问题。(1)、保持水的化学性质的最小微粒是(填微粒名称)。(2)、山泉水中含有微量的氯化镁,氯化镁中阳离子的符号为。
-
14、化学就在我们身边,它与我们的生活息息相关。请按要求从下列物质中选择填空:①氧气;②氮气;③五氧化二磷;④二氧化硫;⑤二氧化碳;⑥矿泉水;⑦氖气。请用这些物质的数字代号填空:(1)、空气中含量最多的气体是;(2)、属于有刺激性气味的有毒气体的是。
-
15、下表所示是验证Zn、Fe、Ag三种金属活动性顺序的4种实验方案,其中“—”表示未进行金属化合物溶液与金属之间的实验,各实验方案中,不能达到实验目的的是
金属化合物溶液
①
②
③
④
ZnSO4溶液
—
Fe
Ag
Fe
FeSO4溶液
Zn
Ag
Zn
—
AgNO3溶液
Fe
—
—
Fe
A、① B、② C、③ D、④ -
16、在日常生活或化学实验中都应加强安全意识。下列做法符合安全要求的是A、白磷弄到了实验桌上,不用理睬它 B、加热后的试管立即用冷水冲洗 C、家中燃气泄漏,立即打开排风扇通风 D、燃着的酒精灯不慎碰到,若洒出的酒精燃烧起来,应立刻用湿抹布扑灭
-
17、物质的性质决定用途。下列有关物质的性质与用途对应关系不正确的是A、氦气密度小且化学性质稳定,可填充飞艇 B、常温下氮气的化学性质不活泼,用于食品防腐 C、石墨能导电,可用作电池的电极 D、金刚石有特殊的光学性质,可用于切割玻璃
-
18、“结构决定性质”是化学的核心观念之一,下图是两种原子的结构示意图,下列说法正确的是
 A、a不容易失去最外层电子 B、a和b元素的本质区别在于质子数不同 C、a、b两种原子对应元素的化学性质相似 D、a、b两种原子对应元素在元素周期表位于不同周期
A、a不容易失去最外层电子 B、a和b元素的本质区别在于质子数不同 C、a、b两种原子对应元素的化学性质相似 D、a、b两种原子对应元素在元素周期表位于不同周期 -
19、维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中,正确的是A、维生素C的相对分子质量为167 B、维生素C中氢元素的质量分数为5.4% C、维生素C中C、H、O三种元素的质量比为9:1:12 D、1个维生素C分子由6个碳原子、6个氢原子、6个氧原子构成
-
20、有一种“可呼吸二氧化碳”电池,放电时吸收二氧化碳,充电时放出二氧化碳。放电时,金属钠和二氧化碳反应生成碳单质和碳酸钠,此反应涉及到的化学用语表示错误的是A、3个二氧化碳分子: B、碳酸钠的化学式: C、碳酸根离子: D、三个氧原子: