-
1、钼(元素符号是)是一种重要的金属,用它制成的金属材料具有良好的机械性能,在工农业生产和国防上都有着广泛的应用。如图是利用钼矿石(主要成分为)制备金属钼的流程图,请据图回答下列问题。
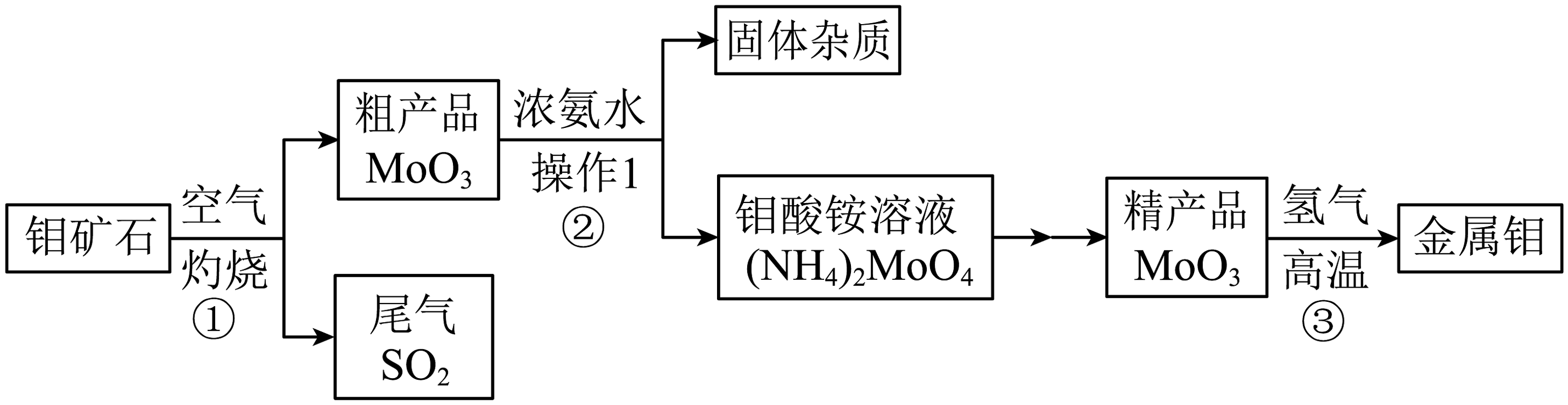 (1)、反应①常将钼矿石粉碎,目的是。(2)、操作1的所需的玻璃仪器有烧杯、漏斗和 , 所填仪器的作用是。(3)、中钼元素的化合价为价。(4)、写出反应③的化学方程式。(5)、步骤①尾气二氧化硫会对空气造成污染,可以用氢硫酸溶液来吸收,发生反应的化学方程式: , X的化学式为。
(1)、反应①常将钼矿石粉碎,目的是。(2)、操作1的所需的玻璃仪器有烧杯、漏斗和 , 所填仪器的作用是。(3)、中钼元素的化合价为价。(4)、写出反应③的化学方程式。(5)、步骤①尾气二氧化硫会对空气造成污染,可以用氢硫酸溶液来吸收,发生反应的化学方程式: , X的化学式为。 -
2、如下图1是我国正在运行和建设的空间站。等物质的循环利用是空间站建设的重要课题。
 (1)、石墨烯、碳纳米管等制成的材料是处理的催化剂,处理前后,该材料的性质不变。(2)、复合氯化铝是净水的一种新型絮凝剂,是其中的一种,若显价,则x=。(3)、如上图2是利用已学过的六种常见物质搭建空间站结构模型,“”表示物质之间可以相互转化,A通电生成F和B,放出大量的热,靠植物的光合作用实现。
(1)、石墨烯、碳纳米管等制成的材料是处理的催化剂,处理前后,该材料的性质不变。(2)、复合氯化铝是净水的一种新型絮凝剂,是其中的一种,若显价,则x=。(3)、如上图2是利用已学过的六种常见物质搭建空间站结构模型,“”表示物质之间可以相互转化,A通电生成F和B,放出大量的热,靠植物的光合作用实现。①写出下列物质的化学式:E , F。
②产生B气体的容器连接电源的(填“正”或“负”)极。
③若反应“”“”“”均属同一种基本反应类型,则该反应类型为。写出反应的化学方程式为。
④通过“天舟”可接送物质,该物质能与D相互转化,则运送的物质是(填字母)。
A. B. C.
-
3、
回答下列问题:
Ⅰ.实验室制取及其性质检验
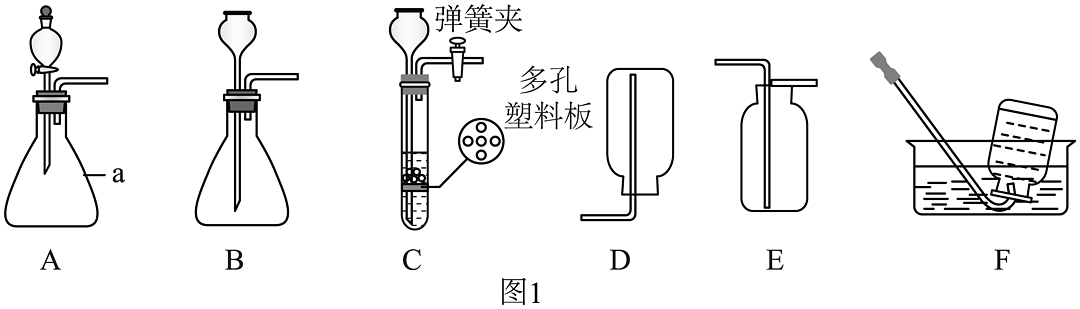
(1)图1中仪器a的名称:________。
(2)用大理石和稀盐酸反应制取 , 反应的化学方程式为________;选择C装置作发生装置的优点是________。收集选用装置________。
(3)用进行性质检验

A.图2装置用于验证二氧化碳的性质。
①实验中观察到A中紫色石蕊布条不变色,B中紫色石蕊布条变红,使其变红的物质是________;
②C中可观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的化学性质是________。
B.图3装置用于验证质量守恒定律。将试管中的盐酸倒入盛有大理石的烧杯中,充分反应后,天平指针会向________(填“左”或“右”)偏转,该实验________(填“能”或“不能)验证质量守恒定律。
Ⅱ.“水草培育”气肥自动补充器,如图4所示。
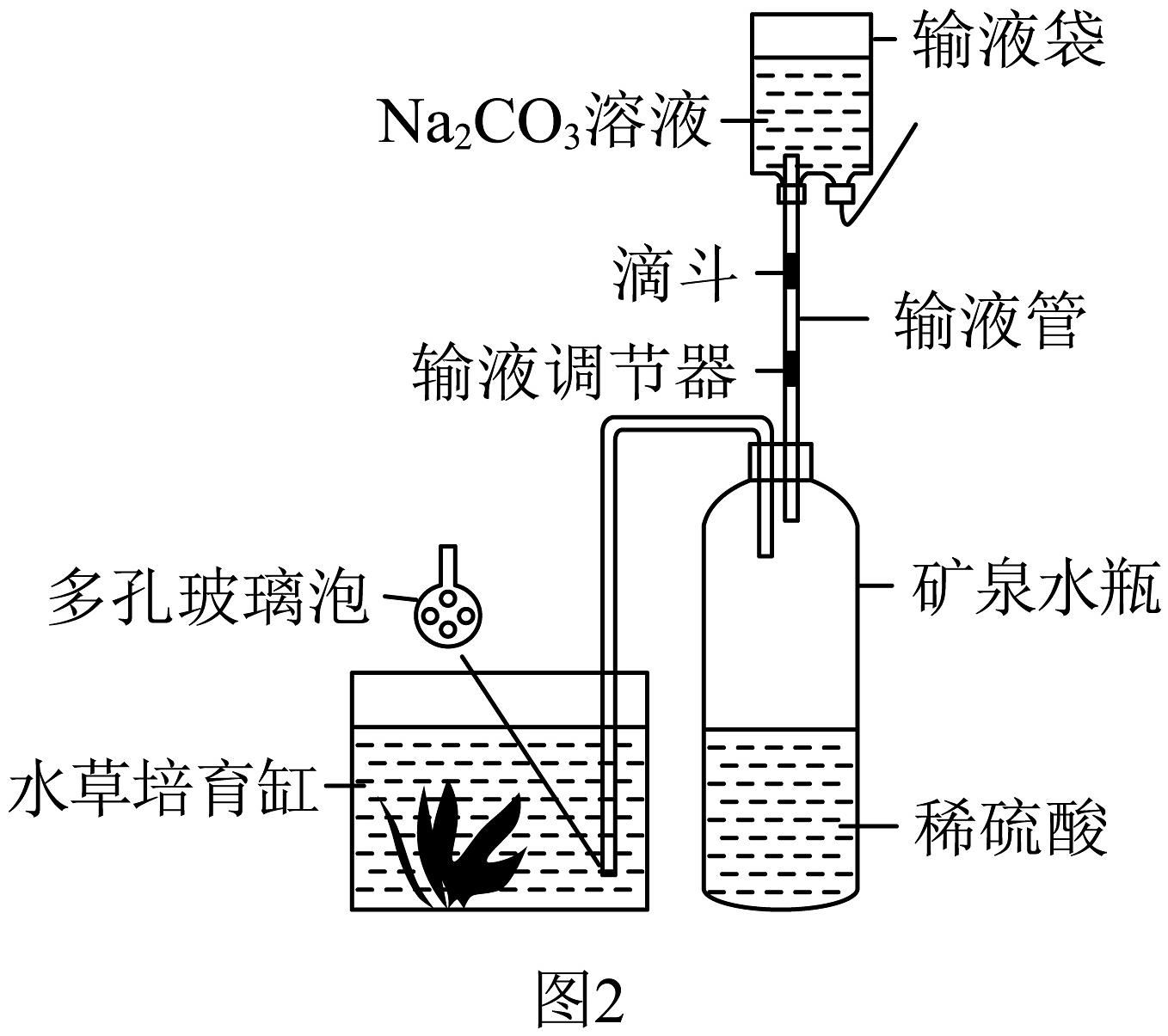
(4)设计原理:采用溶液和稀硫酸反应补充气肥 , 水草需要吸收气肥进行________作用。
(5)动手制作:使用时,将导管放入水草培育缸,调节输液调节器,控制输液袋中溶液的________,导管末端连接多孔玻璃泡的作用是________。
-
4、新能源汽车已经走进了我们的生活,与传统汽车使用化石燃料不同,新能源汽车的能量来源更加多元化,目前主要有以下四种类型。
电动汽车:电池能为电动汽车提供动力,几类电池的部分性能指标如图所示,其中能量密度表示单位体积的电池所具有的能量。
氢内燃车:氢内燃车以氢气为燃料,不排放任何污染物。据测算,氢气完全燃烧可释放的热量,汽油完全燃烧可释放的热量。
乙醇汽车:乙醇汽车以乙醇为燃料,乙醇是可再生能源,可以通过发酵甘蔗、玉米等农作物或粮食收割后剩余的秸秆大量提取。
太阳能汽车:以太阳能电池驱动,低碳环保,真正实现了零排放。
依据上文,回答下列问题。
 (1)、化石燃料属于(填“可再生”或“不可再生”)能源。(2)、依据图可知,镍氢电池优于锂电池的性能指标是。(3)、下列说法正确的是(填字母)。
(1)、化石燃料属于(填“可再生”或“不可再生”)能源。(2)、依据图可知,镍氢电池优于锂电池的性能指标是。(3)、下列说法正确的是(填字母)。a.依据图可知,其他条件相同时,铝空电池提供的能量密度最大
b.农业大国盛产甘蔗和玉米,有利于推广乙醇汽车
c.报废的电动汽车电池,要及时用土进行掩埋处理
(4)、氢气被称为绿色能源,氢气燃烧的化学方程式为 , 但氢能目前还没有被广泛推广使用,原因有(答一点即可)。(5)、太阳能电池需要大量的单质硅,工业上常用二氧化硅和过量的焦炭高温条件下进行制备,该反应的化学方程式为。 -
5、央视栏目《典籍里的中国》展现了中国智慧,如图蕴含了古代净水、酿酒中的原理。
 (1)、“水为食之先”,《熠石篇》中介绍了用明矾使河水变得清澈的技术。明矾中所含铝离子的符号是 , 乙池净水主要利用了木炭的性。(2)、净化后的水用于酿酒,《本草纲目》记载:“其法用浓酒和糟入甄,蒸令气上……其清如水,味极浓烈,盖酒露也。”
(1)、“水为食之先”,《熠石篇》中介绍了用明矾使河水变得清澈的技术。明矾中所含铝离子的符号是 , 乙池净水主要利用了木炭的性。(2)、净化后的水用于酿酒,《本草纲目》记载:“其法用浓酒和糟入甄,蒸令气上……其清如水,味极浓烈,盖酒露也。”①在甑桶中的粮食加入酒曲,发酵酿酒的过程中发生的反应有 , 该反应的基本反应类型为。
②在灶内燃烧木材时,为使燃烧更充分,可采取的措施是。将酒糟放入甄桶中,加热一段时间后,酒坛中收集到清澈的酒精,此法叫(填“过滤”或“蒸馏”)。
③“味极浓烈,盖酒露也”,从微观角度解释其原因是。
④在实验室常用酒精灯加热,酒精燃烧的化学方程式为。
-
6、探究过氧化氢分解速率的影响因素,下列分析正确的是
实验编号
过氧化氢溶液
催化剂()
温度/℃
体积
浓度/%
①
5
5
—
20
②
5
5
二氧化锰粉末
20
③
5
5
二氧化锰粉末
40
④
5
5
氧化铁粉末
20
⑤
5
10
二氧化锰粉末
20
A、①⑤探究有无催化剂的影响 B、②③探究反应温度的影响 C、③⑤探究过氧化氢溶液浓度的影响 D、④⑤探究催化剂种类的影响 -
7、中科院团队在常温、常压和可见光条件下,基于(一种固体催化剂)可合成氨气)。下列叙述正确的是
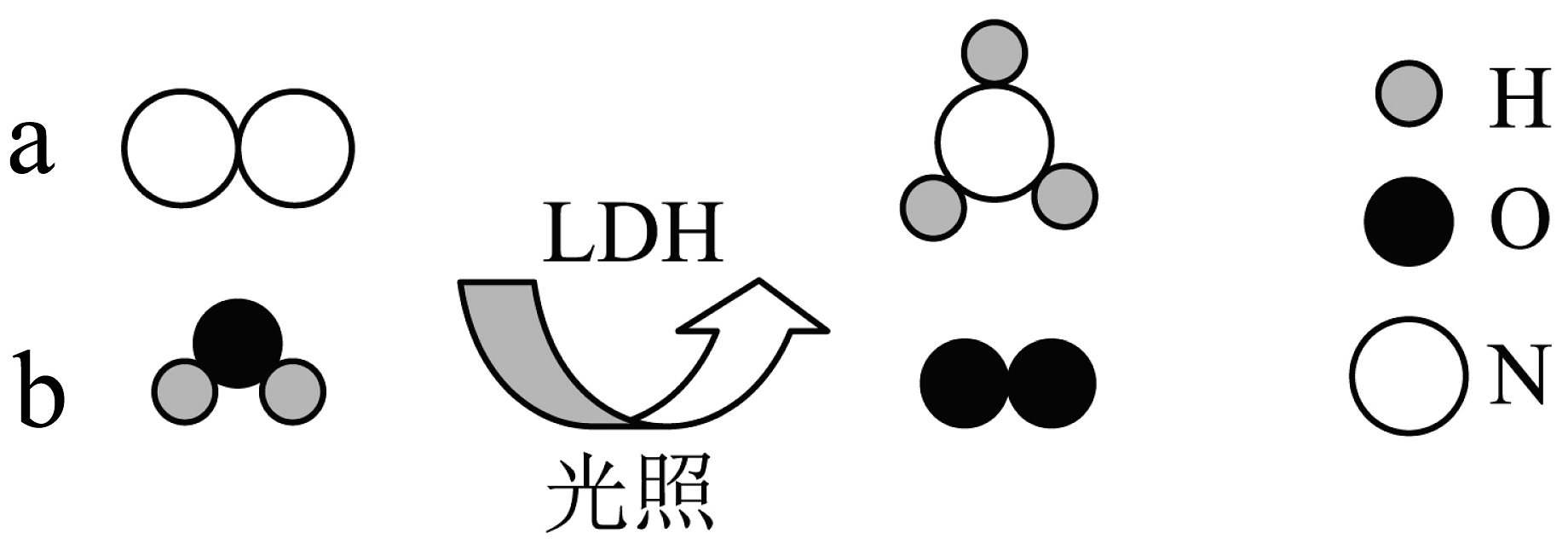 A、反应后氧原子个数增加 B、b的化学式为 C、参加反应的a、b分子个数比为 D、反应后催化剂质量减少
A、反应后氧原子个数增加 B、b的化学式为 C、参加反应的a、b分子个数比为 D、反应后催化剂质量减少 -
8、“劳动是一切幸福的源泉”。下列劳动实践与化学知识没有关联的是
选项
家务劳动项目
化学知识
A
用纱布包裹佐料炖肉
利用了过滤的原理
B
用糯米酿制米酒
糯米发生了缓慢氧化
C
用活性炭等材料制作净水器
活性炭具有消毒杀菌作用
D
用电吹风热风档快速吹干湿衣服
温度越高分子运动越快
A、A B、B C、C D、D -
9、色氨酸是氨基酸中的一种,在人体内含量太低会影响睡眠质量,一般可通过食补黄豆、黑芝麻、海蟹和肉松等得以改善。有关色氨酸的说法正确的是A、碳、氮原子个数比为 B、含有27个原子 C、氢元素质量分数最大 D、由四种元素组成
-
10、下图为碳元素的“化合价—物质类别—转化关系”图,有关说法正确的是
 A、a一定是金刚石 B、可以是高温条件下和碳发生反应 C、d可能是碳酸钙 D、发生化合反应
A、a一定是金刚石 B、可以是高温条件下和碳发生反应 C、d可能是碳酸钙 D、发生化合反应 -
11、市场上有很多“富硒产品”,硒原子的原子结构示意图如图甲,硒元素在元素周期表中的分信息如图乙,下列说法正确的是
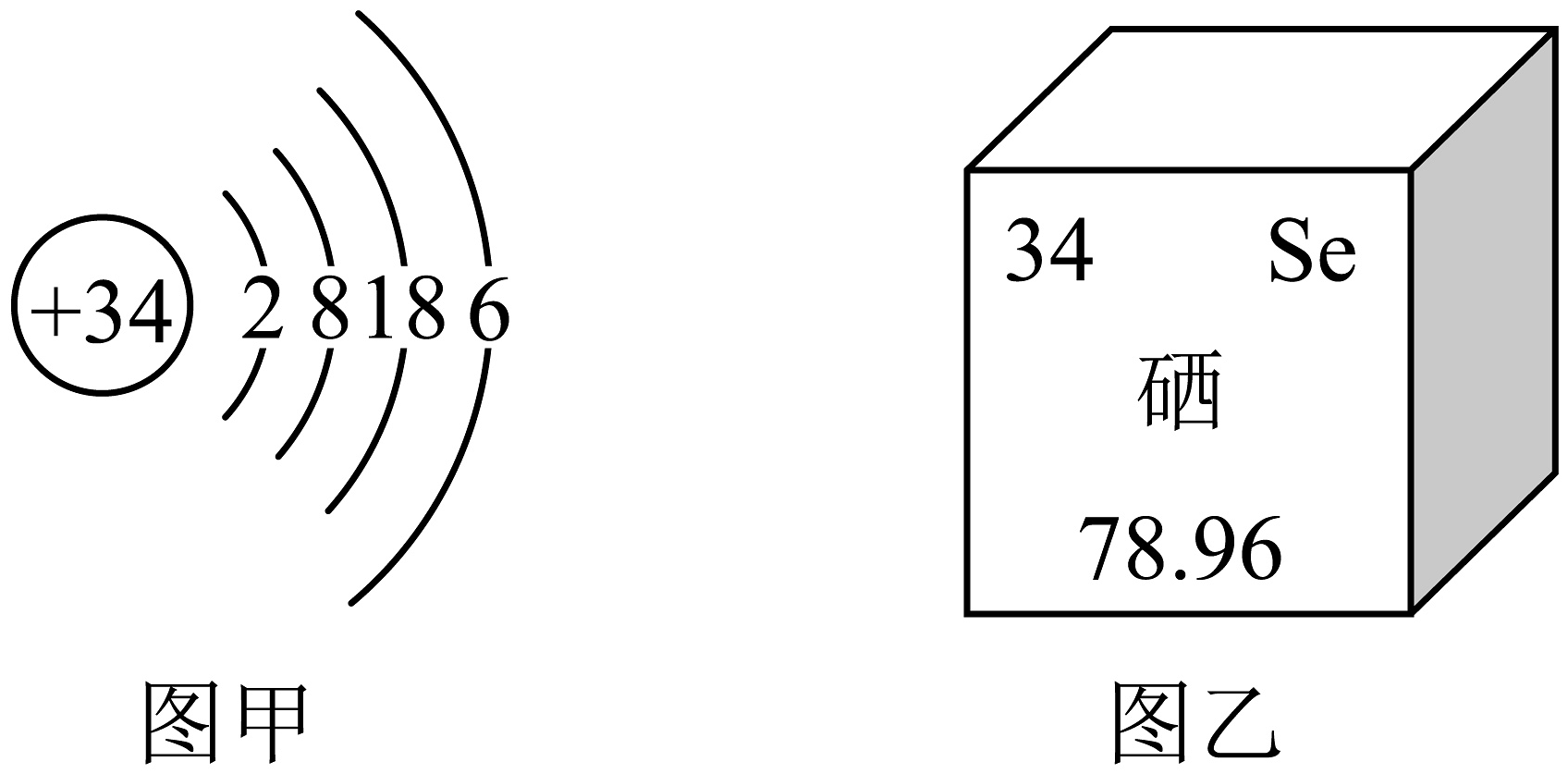 A、硒元素属于金属元素 B、硒原子的最外层电子数为6 C、硒原子的质子数=中子数 D、硒原子的相对原子质量为
A、硒元素属于金属元素 B、硒原子的最外层电子数为6 C、硒原子的质子数=中子数 D、硒原子的相对原子质量为 -
12、《清顶香茶》中记载:“日出卧龙日暮色,月生青顶月茶香”。从微观角度解释煮茶时闻到茶香的原因是A、分子之间的间隔变大 B、分子的总数增大 C、分子可以分解为原子 D、温度升高,分子运动速率加快
-
13、化学用语是学习化学的工具。下列表示2个氮原子的是A、 B、 C、 D、
-
14、规范的操作方法是实验安全和成功的重要保证。下列实验操作正确的是A、连接仪器
 B、检验氢气纯度
B、检验氢气纯度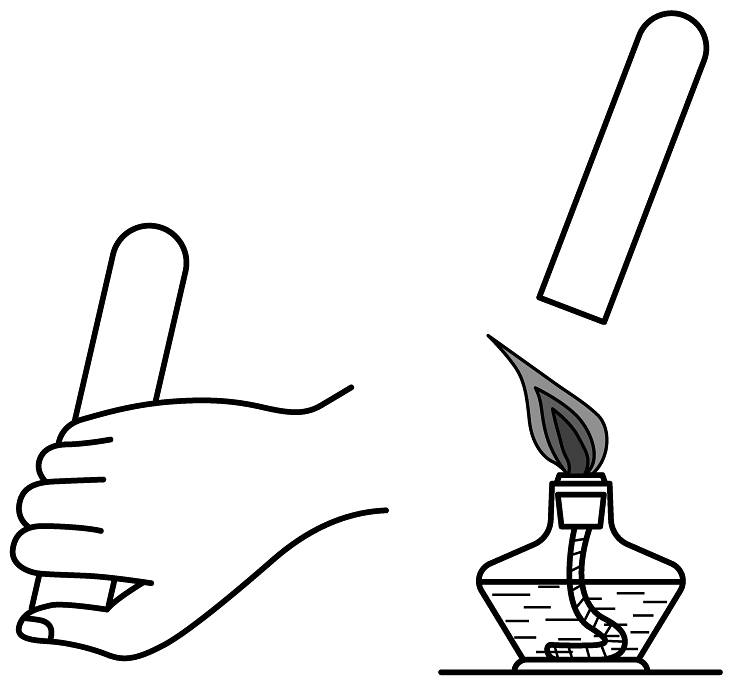 C、过滤
C、过滤 D、移走蒸发皿
D、移走蒸发皿
-
15、山西八路军太行纪念馆收藏了许多革命文物,有草鞋、彩陶罐、石雕方砚、木板漆画等,制作这些物品的过程中,与物质化学性质有关的是


A.编织草鞋
B.烧制陶罐


C.雕刻石器
D.锯断木板
A、A B、B C、C D、D -
16、广东有许多优秀的民间制作工艺,下列工艺制作过程涉及化学变化的是




A.雕刻核雕
B.剪窗花
C.酿酒
D.缝制刺绣扇子
A、A B、B C、C D、D -
17、广西“三月三”假期间,小明外出踏青时带回一些石灰石。他利用这些石灰石做了如下实验:取15.0g样品于烧杯中,向其中加入50.0g稀盐酸,恰好完全反应,进行的实验及数据如下图所示(杂质不参与反应且不溶于水)。

请回答问题并计算:
(1)、15.0g石灰石样品中碳酸钙的质量为g。(2)、所用稀盐酸的溶质质量分数。(写出具体计算过程) -
18、
食品添加剂是为改善食品色、香、味等品质,以及为防腐和加工工艺的需要而加入食品中的人工合成或天然物质。
任务一:了解食品添加剂的种类
【信息检索】国家《食品添加剂使用标准》中批准可以使用的部分食品添加剂整理如下:
食品添加剂类别
主要作用
常见的食品添加剂
着色剂
赋予食品诱人的色泽
胡萝卜素、柠檬黄素等
防腐剂
防止食品变质,延长保质期
苯甲酸钠、山梨酸钾等
增味剂
改善食品的口味
乳酸、甜蜜素等
膨松剂
使食品松软酥脆、口感更好
碳酸氢钠、碳酸钠等
(1)从物质类别上分析,碳酸氢钠属于(填“酸”“碱”或“盐”)。
任务二:探究膨松剂的主要成分
同学们在劳动实践课上制作面点时加入某膨松剂,他们对该膨松剂的主要成分产生了兴趣。
【提出问题】该膨松剂含有碳酸钠还是碳酸氢钠?
【查阅资料】
①碳酸氢钠与氢氧化钙溶液反应产生白色沉淀。
②溶质质量分数小于0.83%的碳酸氢钠溶液中加入0.1%的氯化钙溶液无现象。
【进行实验】
(2)甲同学取少量样品于试管中,倒入足量稀盐酸,观察到的现象,认为该膨松剂的主要成分是碳酸氢钠。
【交流讨论】
(3)乙同学认为甲同学的结论不严谨,理由是(用化学方程式解释)。
(4)丙同学认为选择(填字母序号)配制适宜溶质质量分数的溶液进行实验,可知该膨松剂的主要成分是碳酸氢钠。
A. 氯化钙固体 B. 氢氧化钙固体 C. 硝酸钾固体 【反思总结】通过以上探究,同学们建立了“性质→方案→推理”的鉴别思维。
【拓展提升】
同学们设计创新实验方案,鉴别未知白色固体是碳酸氢钠还是碳酸钠。通过AI查阅资料得知:20℃时,碳酸氢钠和碳酸钠的溶解度分别是9.6g和21.5g;碳酸氢钠受热易分解成碳酸钠、水和二氧化碳,碳酸钠受热不易分解。
(5)根据上述资料提供的信息设计一种实验方案:(写出实验操作、现象及结论)。
任务三:认识食品添加剂的作用
不使用防腐剂的食物容易变质。丙酸钙是世界卫生组织推荐使用的一种新型食品防腐剂,在对食品保鲜的同时,还能为人体提供所需钙质。
【测试与分析】
(6)分别将不添加丙酸钙和添加丙酸钙的面包置于温度28℃、相对湿度为72%的恒温箱中,测得霉菌数量与存放时间的变化如图所示,分析图像可得出的结论是(答一点即可)。

(7)我国对食品添加剂有严格的规定用量,只要合理使用就不会对人体造成伤害。在食品生产中,以下关于食品添加剂合理使用的做法正确的是。
A. 担心食品变质,超量添加防腐剂 B. 为增加饮料甜度,添加大量甜蜜素 C. 为让蛋糕颜色更鲜艳,随意增加色素用量 D. 根据《食品添加剂使用标准》,按规定用量添加膨松剂制作面包 -
19、如图所示为实验室常见气体制备装置,请回答问题:
 (1)、仪器①的名称是________。(2)、实验室用高锰酸钾制取氧气,应选择的发生装置是(填装置序号),反应的化学方程式为 , 若用装置E收集氧气,观察到时可以开始收集。(3)、选择装置C收集二氧化碳,是因为二氧化碳具有的性质。若用装置D干燥二氧化碳,可在装置D内装入的液体是(填名称)。(4)、选择装置B作为实验室制取氢气的发生装置,装置B中存在的一处错误是________。
(1)、仪器①的名称是________。(2)、实验室用高锰酸钾制取氧气,应选择的发生装置是(填装置序号),反应的化学方程式为 , 若用装置E收集氧气,观察到时可以开始收集。(3)、选择装置C收集二氧化碳,是因为二氧化碳具有的性质。若用装置D干燥二氧化碳,可在装置D内装入的液体是(填名称)。(4)、选择装置B作为实验室制取氢气的发生装置,装置B中存在的一处错误是________。 -
20、柠檬酸钙[化学式为Ca3(C6H5O7)2]是一种安全的食品补钙剂。兴趣小组以鸡蛋壳(主要成分为CaCO3)为主要原料制备柠檬酸钙,其实验流程如下:

查阅资料:Ⅰ.柠檬酸钙微溶于水,难溶于乙醇。
Ⅱ.醋酸钙[化学式为Ca(CH3COO)2]和柠檬酸反应生成柠檬酸钙和醋酸(CH3COOH)。
(1)、过滤操作中玻璃棒的作用是________。(2)、实验前先将鸡蛋壳碾碎的目的是________。(3)、根据题目信息,写出碳酸钙与醋酸反应的化学方程式________。(4)、洗涤柠檬酸钙最适宜的试剂是___________(填字母序号)。A、水 B、乙醇 C、稀醋酸(5)、上述实验流程中可循环利用的物质是________。